Превращения белков в технологическом потоке
4. Превращения белков в технологическом потоке
В процессе технологической обработки пищевых продуктов существенным изменениям подвергаются белки, влияющие на органолептические свойства, биологическую ценность, структурно-механические и другие показатели качества продуктов.
Глубина физико-химических изменений белков зависит от вида продукта, характера внешних воздействий, концентрации белков. К основным изменениям белков пищевых продуктов при различных видах технологической обработки относятся: денатурация и деструкция.
Денатурация белков – это нарушение нативной пространственной структуры белковой молекулы под влиянием различных внешних воздействий, сопровождающееся изменением их физико-химических и биологических свойств. При этом нарушаются вторичная и третичная структуры белковой молекулы, а первичная, как правило, сохраняется.
Денатурация белков происходит при нагревании и замораживании пищевых продуктов под действием различных излучений, кислот, щелочей, резких механических воздействий и других факторов.
При денатурации белков происходят следующие основные изменения:
- резко снижается растворимость белков;
- теряется биологическая активность, способность к гидратации и видовая специфичность;
- улучшается атакуемость протеолитическими ферментами;
Рекомендуемые материалы
- повышается реакционная способность белков;
- происходит агрегирование белковых молекул;
- заряд белковой молекулы равен нулю.
Потеря белками биологической активности в результате тепловой денатурации приводит к инактивации ферментов и отмиранию микроорганизмов.
В результате потери белками видовой специфичности пищевая ценность продукта не снижается.
Рассмотрим наиболее распространенную тепловую денатурацию белковых молекул, сопровождаемую разрушением слабых поперечных связей между полипептидными цепями и ослаблением гидрофобных и других взаимодействий между белковыми цепями. В результате этого изменяется конформация полипептидных цепей в белковой молекуле. Например, фибриллярные белки изменяют свою эластичность, у глобулярных белков развертываются белковые глобулы с последующим свертыванием по новому типу. Прочные (ковалентные) связи белковой молекулы при этом не нарушаются. Глобулярные белки изменяют растворимость, вязкость, осмотические свойства и электрофоретическую подвижность.
Для большинства белков температура денатурации составляет 45 - 60°С. Однако встречаются белки и термостабильные, например, a-лактоглобулин молока и a-амилазы некоторых бактерий. Повышенная устойчивость белков к нагреванию часто обусловливается наличием в их составе большого количества дисульфидных связей. Однако степень денатурирующего воздействия температуры на белки зависит и от их влажности, реакции и солевого состава среды и присутствия небелковых соединений. Например, температура денатурации белков сои и подсолнечника существенно понижается в присутствии кислот жирного рада, в кислой и влажной среде, но повышается в присутствии сахарозы и крахмала.
Тепловая денатурация белков является одним из основных физико-химических процессов, лежащих в основе выпечки хлеба, печенья, бисквитов, пирожных, сухарей, сушки макаронных изделий, получения экструдатов и сухих завтраков, варки, жарения овощей, рыбы, мяса, консервирования, пастеризации и стерилизации молока. Данный вид превращений относится к полезным, так как он ускоряет переваривание белков в желудочно-кишечном тракте человека (облегчая доступ к ним протеолитических ферментов) и обусловливает потребительские свойства пищевых продуктов (текстуру, внешний вид, органолептические свойства). В связи с тем, что степень денатурации белков может быть различной (от незначительной до полного изменения расположения пептидных цепей с образованием новых ковалентных –S–S-связей), то и усвояемость полимеров может не только улучшаться, но и ухудшаться.
Деструкция белков. При нагревании пищевых продуктов выше 100°С происходит разрушение макромолекул денатурированных белков. На первом этапе изменений от белковых молекул могут отщепляться такие летучие продукты, как аммиак, сероводород, диоксид углерода и другие соединения. Накапливаясь в продукте и окружающей среде эти вещества участвуют в образовании вкуса и аромата готовой пищи.
При температуре от 60°С до 100°С со значительной скоростью протекает взаимодействие белков с восстанавливающими сахарами, сопровождающееся образованием карбонильных соединений и темноокрашенных продуктов – меланоидинов (реакция Майяра). Сущность реакций меланоидинообразования заключается во взаимодействии группы –NH2 аминокислот с гликозидными гидроксилами сахаров (Н2). Сахароаминные реакции являются причиной не только потемнения пищевых продуктов, но и уменьшения в них сухого вещества и потерь незаменимых аминокислот (лизина, треонина). Меланоидины понижают биологическую ценность изделий, так как снижается усвояемость аминокислот из-за того, что сахароаминные комплексы не подвергаются гидролизу ферментами пищеварительного тракта. К тому же количество незаменимых аминокислот уменьшается. Это уменьшение происходит не только за счет взаимодействия их с восстанавливающими сахарами, но и за счет взаимодействия между собой функциональных групп –NH2 и –СООН самого белка. Реакции протекают с образованием внутренних ангидридов, циклических амидов и w–e изопептидных связей.
Среди продуктов термического распада белков встречаются соединения, придающие им мутагенные свойства. Термически индуцированные мутагены образуются в белоксодержащей пище в процессе ее обжаривания в масле, выпечки, копчения в дыму и сушки. Мутагены содержатся в бульонах, жареной говядине, свинине, домашней птице, жареных яйцах, копченой и вяленой рыбе. Некоторые из них вызывают наследственные изменения ДНК, и их воздействие на здоровье человека может быть от незначительного до летального.
Так, гетероциклические ароматические амины (ГАА) по мнению ряда ученых – самые сильные мутагенные соединения, известные в настоящее время.
Они формируются в ходе термической обработки пищевого сырья и полуфабрикатов главным образом животного происхождения, как правило, при температуре выше 150°С. Исследователями доказано мощное мутагенное воздействие указанных соединений на микроорганизмы и выраженный канцерогенный эффект в опытах на животных. Есть основания полагать, что именно ГАА ответственны за определенную часть онкологических заболеваний человека.
Как показывают результаты исследований, наиболее важные факторы формирования мутагенных химических веществ – температура и продолжительность процесса кулинарной обработки.
Мутагенная активность мясного фарша, жаренного основным способом при 200°С, примерно в 2 раза выше, чем у такого же образца, но жаренного при 150°С.
Кроме того, уровень мутагенов существенно увеличивается в случае продолжительность процесса более чем 10 мин.
В модельных опытах показано, что при прогревании смеси креатина (всегда имеется в мясе, рыбе), глицина (аланина) и глюкозы при 130°С обнаруживается высокая мутагенная активность. Изъятие хотя бы одного компонента из данной смеси приводит к полной утрате мутагенных свойств. Делается вывод о роли трех главных предшественников (аминокислот, углеводов и креатина) в образовании пищевых мутагенов. Предполагается, что в образовании ГАА участвуют реакции Майера (меланоидинообразования), реакции распада по Стреккеру (с образованием альдегидов и других летучих продуктов); креатин преобразуется в его гетероциклическую форму - креатины, которые далее участвуют в реакциях формирования конденсированных мутагенных гетероциклических аминов. На рисунке 4.2 приведены формулы ГАА:
Рисунок 4.2
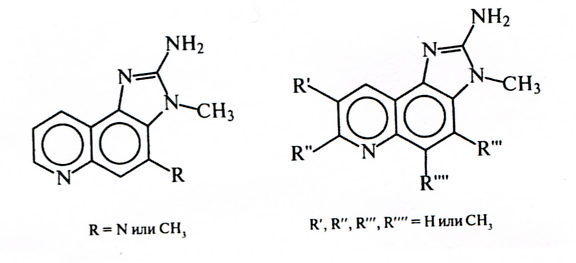
Токсические свойства белков при термической обработке выше 200°С или при более низких температурах, но в щелочной среде, могут обусловливаться не только процессами деструкции, но и реакциями изомеризации остатков аминокислот из L- в D-форму. Присутствие D-изомеров понижает усвояемость белков.
В сильнощелочных средах, особенно при высоких температурах, некоторые остатки аминокислот претерпевают ряд специфических превращений. Так, аргинин превращается в орнитин, цитруллин, мочевину и аммиак, а цистеин – в дегидроаланин с выделением сероводорода:
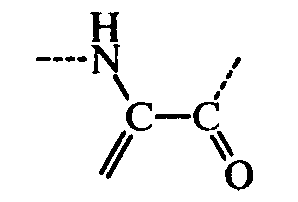
Реакционноспособный дегидроаланин конденсируется с остатками лизина, орнитина и цистеина боковых цепей и образует межмолекулярные поперечные связи в белках:
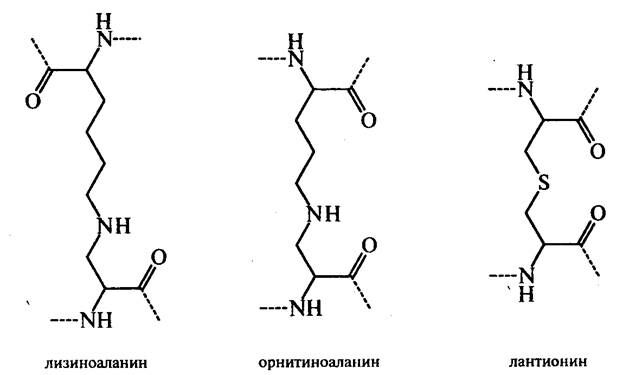
В реакцию конденсации могут вступать остатки аргинина, гистидина, треонина, серина, тирозина и триптофана. Питательная ценность белков с новыми поперечными связями ниже, чем у белков с нативной структурой, поэтому образование их в технологических процессах производства пищевых продуктах нежелательно. К тому же в опытах на крысах показано, что образование, например, лизиноаланина стимулирует нефрокальциноз, диарею и облысение.
Обработка сырья растворами щелочей широко используется при получении изолятов и концентратов белков. Чем выше значение рН, температура и время обработки, тем ниже содержание незаменимых аминокислот в белке. Например, при повышении рН раствора с 8,5 до 12,5 при экстракции белка из пшеничных отрубей количество лизина в нем уменьшается на 40%, треонина – на 26%, а валина – на 24%. Мягкие температурные режимы предохраняют от образования в больших количествах нежелательных аминокислотных фрагментов. В то же время среди специалистов обсуждается вопрос о введении предельно допустимых концентраций лизиноаланина (например, 300 мг на 1 кг) в целях обеспечения безопасности белоксодержащей пищи.
Агрегирующая и комплексообразующая способность белков пшеницы является одним из важных показателей, обеспечивающих им ведущую роль в формировании клейковины в процессе ее отмывания из муки и тестоведения.
Параметры агрегации белков сильных пшениц, характеризующиеся более «плотной» пространственной упаковкой структуры, выше по сравнению со слабыми, имеющими более «рыхлую» организацию молекул. Процесс образования белковых агрегатов по ходу технологического процесса приготовления изделий из муки интенсивнее у крепкой клейковины, чем у слабой. Наиболее высокие показатели агрегации наблюдается у a- и g-компонентов глиадина, наименее – у w-компонентов.
Агрегирующая способность белков взаимосвязана с особенностями аминокислотного состава. Так, суммарный глиадин с более повышенной агрегирующей способностью содержит меньше заряженных групп, а w-глиадины, обладающие низкой степенью агрегации, богаты пролином, фенилаланином, амидогруппами и полярными аминокислотными остатками. Это определяет высокую способность их к взаимодействию с другими компонентами муки и, прежде всего с липидами и липидоподобными соединениями (дигалактозилдиглицерид). Комплексообразование последнего с w-глиадинами за счет водородных связей обусловливает газоудерживающую способность теста и объем хлеба.
С повышением рН от 4,0 до 9,1 агрегация белков злаковых культур (пшеницы, ржи, ячменя) повышается. Чем больше концентрация нейтральных солей, тем агрегирующая способность белков выше.
Степень участия того или иного фактора в изменении агрегативного состояния белков, а с ним и реологических свойств теста и качества хлеба, зависит от исходных физико-химических свойств и структурных особенностей белков муки, технологических факторов процесса (температура, степень механического воздействия, рН среды и т.д.), химической природы и количества дополнительного сырья, улучшителей и пищевых добавок.
Обратите внимание на лекцию "1 Иммунопрофилактика и иммунотерапия".
Огромное значение для изменения свойств и агрегативного состояния белков в ходе технологического процесса приготовления теста имеет дисульфидно-сульфгидрильный обмен:
P1S-SP2 + P3SH ® P1S-SP3 + P2SH
Считают, что лабильность дисульфидных связей обеспечивает образование новых прочных межмолекулярных связей и релаксацию (ослабление) напряжения структур клейковины при замесе теста.
Сильная мука, содержащая крепкую клейковину, требует дльше времени замеса, так как она содержит больше дисульфидных связей и меньше SH-групп, чем слабая.
В процессе созревания муки при ее отлежке, а также под влиянием окислителей типа броматов, улучшение реологических свойств клейковины объясняется увеличением содержания S–S-связей и уменьшением, соответственно, SH-групп. В присутствии восстанавливающих агентов (сульфит натрия) реологические свойства клейковины ухудшаются, как это имеет место в прорастающем зерне или в процессе приготовления теста из зерна, пораженного клопом-черепакой. Во всех случаях показатели качества и реологические характеристики теста взаимосвязаны с изменением в соотношении S–S-связей и SH-групп в белках.
В результате действия протеолетических ферментов в технологическом потоке производства пищевых продуктов белковые вещества так же претерпевают ряд существенных изменений. Так, на стадии солодоращения при производстве пива в эндосперме ячменя наблюдается гидролиз глобулина (эдестин), альбумина (лейкозин), проламина (гордеин) и глютелина с накоплением азотистых соединений с более низкой молекулярной массой (пептиды, аминокислоты). В результате в зерне накапливается растворимая, коагулируемая и аминная формы азота, тогда как в зародышевом листке и ростках зерна, наоборот, увеличивается количество белкового азота за счет процессов синтеза.



















