Электрохимические сенсоры и биосенсоры
2.6 Электрохимические сенсоры и биосенсоры
2.6.1. Потенциометрические биосенсоры
Это наиболее простые по конструкции потенциометрические биосенсоры. Таких биосенсоров очень много, поскольку рН-электрод можно
использовать в любой системе, в которой в результате химических превращений меняется рН. Ниже мы приводим три примера использования биосенсоров, в которых на мембране рН-электрода иммобилизова
ны ферменты. Попутно заметим, что аналогичным образом ферменты
можно иммобилизовать и в затворе рН-чувствительного полевого
транзистора.
Определение пенициллина. Определение пенициллина основано на изменении рН в ходе превращения пенициллина под действием пенициллиназы:
пенициллин -» пенициллоат + Н+
Определение глюкозы. В ходе превращения глюкозы под действием глюкозооксидазы образуется глюконовая кислота, что приводит к уменьшению рН раствора:
глюкоза + О, -» глюконовая кислота + Н202
Определение мочевины. Первым потенциометрическим биосенсором для клинической диагностики был биосенсор на мочевину [Guillbault and Kuan, 1987]. Его действие основано на гидролизе мочевины под действием уреазы из черных бобов:
Рекомендуемые материалы
CO(NH2)2 + 2Н20 -> 2NH4+ + С032_
2.6.2. Биосенсоры с аммиак-чувствительными
электродами
С помощью аммиак-чувствительного электрода можно следить за лю-
быми превращениями, в ходе которых образуется аммиак.
Определение мочевины. Как видно из приведенного выше уравнения реакции, при гидролизе мочевины образуется аммиак. За его содержанием можно следить с помощью электродов, чувствительных либо к ионам аммония, либо к газообразному аммиаку. В последнем случае раствор должен быть щелочным. В одном из наиболее удачных биосенсоров на мочевину используется аммиак-чувствительный электрод, на полипропиленовой мембране которого иммобилизована уреаза. Он характеризуется низким пределом обнаружения (10-6 М), быстрым временем регенерации,позволяющим делать 20 проб в час со стандартным отклонением
± 2,5 %, и довольно широким линейным диапазоном (от 5-10-5 до
10-2М).
Определение креатинина. При деаминировании креатинина под действием креатиназы также образуется аммиак:
креатинин -» NH3 + креатин
Аммиак-чувствительный электрод, на полипропиленовой мембра-
не которого иммобилизовали креатиназу, сохраняет стабильность на
протяжении 8 месяцев и позволяет провести 200 измерений. Его предел
обнаружения составляет 8-10-6 М.
Определение фенилаланина. Под действием фенилаланинаммиаклиазы из фенилаланина образуется аммиак и транскоричная кислота:
L-фенилаланин -» NH3 + транскоричная кислота
Разработан сенсор на фенилаланин, который характеризуется
очень высокой селективностью, но медленно регенерирует и имеет
узкий линейный диапазон.
Определение аденозина. При деаминировании аденозина под действием адениндезаминазы образуются инозин и аммиак:
аденозин -» NH3 + инозин
В биосенсоре на аденозин адениндезаминазу адсорбировали на поверхности аммиак-чувствительного электрода, а затем сшивали
глутаровым альдегидом.
Определение аспартама. Аспартам под действием L-аспартазы также претерпевает превращения с образованием аммиака:
Аспартам -» NH3 + С6Н5СН2СН (C02H) NHCOCHCHC02H
2.6.3. Биосенсоры с СО2-чувствительными
электродами
Известно несколько примеров использования в биосенсорах ИСЭ, чувствительных к углекислому газу.
Определение мочевины. Мочевина гидролизуется с образованием аммиака и углекислого газа. В кислом растворе за выделяющимся углекислым газом можно следить с помощью соответствующего газового электрода.
Определение оксалата. Определение оксалата в моче имеет клиническое значение при диагностике оксалурии. Под действием оксалатадекарбоксилазы оксалт распадается на С02 и формиат:
Оксалат → 2С02 + формиат
Однако оксалатадекарбоксилаза ингибируется фосфатом и сульфатом, которые обычно присутствуют в моче. Вместо нее можно использовать оксалатоксидазу, в присутствии которой из оксалата образуются С02 и перекись водорода:
Оксалат → 2С02 + Н202
Впрочем, оксалатоксидаза также ингибируется некоторыми
анионами.
Определение дигоксина. Онределение концентрации дигоксина проводят с помощью конкурентного иммуноферментативного анализа. В анализе используют полистирольные шарики с иммобилизованным на них дигоксином, которые легко отделить от испытуемого раствора. В зависимости от содержания диоксина в растворе с шариками связывается разное количество антител
против дигоксина, меченных пероксидазой. Количество связанной пероксидазы можно определить после добавления к суспензии шариков
перекиси водорода и пирогаллола по количеству образующегося С02:
Н202 + пирогаллол → С02
2.6.4. Биосенсоры с иодид-селективными
электродами
Определение глюкозы. Как уже говорилось, в присутствии глюкозооксидазы глюкоза окисляется с образованием перекиси водорода. Если в смеси при этом присутствуют пероксидаза и йодид-ионы, то перекись водорода идет на окисление последних с образованием йода.
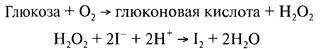
По скорости потребления иодид-ионов, измеряемой с помощью
иодид-селективного электрода, можно судить о концентрации Н202, а
значит, и глюкозы.
Определение фенилаланина. В биосенсоре для определения фенилаланина на поверхности йопид-селективного электрода в полиакриламидном геле иммобилизована L-аминооксидаза (L-AO) и пероксидаза. Принцип работы этого биосенсора сходен с предыдущим.
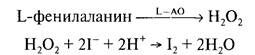
Впрочем, он менее селективен, чем биосенсор на основе аммиакчувствительного электрода.
Определение эстрадиола. Определение эстрадиола проводят с помощью конкурентного иммуноанализа с применением йодид-селективного электрода. На поверхности электрода адсорбирована желатиновая мембрана с иммобилизованными в ней антителами против 17(3-эстрадиола. Электрод помещают в раствор, в котором присутствует смесь свободного эстрадиола и эстрадиода, меченного пероксидазой (рис. 5.5а). Чем меньше концентрация
свободного эстрадиола, тем больше меченного эстрадиола связывается
с мембраной. При добавлении в раствор Н202 и I- в качестве субстрата
пероксидазы в мембране электрода происходит ферментативное окисление йодид-ионов с образованием йода. При этом возникающий на
йодид-селективном электроде потенциал пропорционален количеству
связанной пероксидазы, а значит, обратно пропорционален логарифму
концентрации эстрадиола (рис. 2.19).
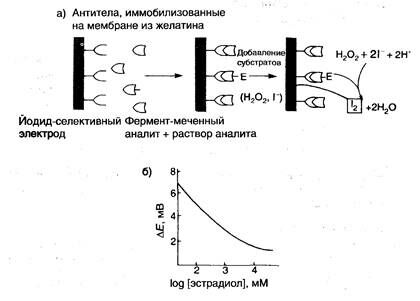
Рис. 2.19. Определение 17-эстрадиола с помощью йодид-селективного электрода:
а) схема анализа;
б) калибровочная кривая, отражающая зависимость электродного
потенциала от концентрации аналита
2.6.5. Биосенсоры с Аg2S-чувствительными электродами
Определение цистеина. Определение цистеина с помощью Ag2S-чувствительных электродов может быть основано на неферментативном восстановлении цистеина и цистин, который образует с ионами Ag+ нерастворимый сульфид.
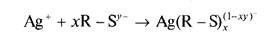
Более специфичное определение цистеина основано на его восста-
новлении под действием р-цианоаланинсинтетазы:
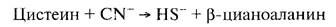
Однако в этом случае цианидионы создают помехи на электроде.
2.6.6. Амперометрические биосенсоры
Определение глюкозы. Примерно в половине статей, посвященных разработке биосенсором, описываются биосенсоры для определения глюкозы. Дело тут не только
в клинической значимости подобного анализа. Накопленный опыт позволяет на примере определения глюкозы сравнивать разные типы сенсоров и оценивать новые разработки.
Основные способы получения аналитического сигнала в глюкозных биосенсорах суммированы на рисунке 2.20. Все они основаны наиспользовании глюкозооксидазы.
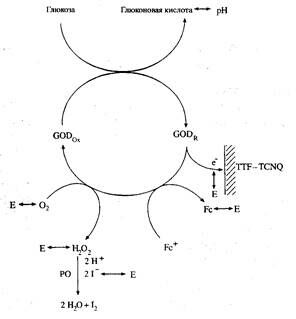
Рис. 2.20 Способы получения аналитического сигнала при окислении
глюкозы глюкозооксидазой (GOD)
I. В качестве продукта реакции окисления глюкозы образуется глюконовая кислота, что дает возможность в качестве аналитического сигнала использовать изменение рН:
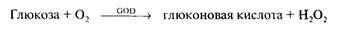
2. В некоторых типах электродов может происходить реокисление
восстановленной формы глюкозооксидаз:
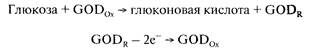
Это позволяет использовать в качестве аналитического сигнала величину анодного тока.
3. В ходе окисления глюкозы потребляется кислопод:
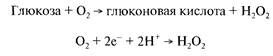
По уменьшению его концентрации, определяемой с помощью элек-
трода Кларка, можно определять концентрацию глюкозы.
4. Если катод в электроде Кларка сделать анодом, поменяв поляр-
ность включения электрода-трансдьюсера, то при потенциале +0,6 В
будет происходить окисление перекиси водорода:
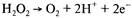
5. Образующаяся при окислении глюкозы перекись водорода в
присутствии пероксидазы (РО) окисляет йодид-ион до йода. В этом
случае концентрацию глюкозы можно определять, измеряя концентра-
цию йодид-иона с помощью йодид-селективного электрода:
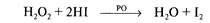
6. В качестве окислителя можно использовать не кислород, а меди-
итор, например, ферроцен (Fc):
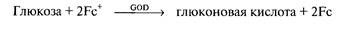
Определение лактата. Содержание лактата в крови — важный показатель интенсивности мышечной деятельности. В основе определения лактата биосенсорами могут лежать четыре разные реакции. В двух из приведенных ниже примеров в качестве окислителя лактата выступает кислород, а в двух другихмедиаторы.

Определение холестерина. Полагают, что повышенный уровень холестерина в крови коррелируетс риском ишемической болезни сердца.
Биосенсоры на холестерин могут быть основаны на использовании
именно таких пар ферментов. В одном из них (рис. 2.21) задействована
система сопряжения, включающая NAD+/NADH, диафоразу и ферро
цен в качестве медиатора. В другом (рис. 2.22) используется система е
пероксидазой и ферроценом. Наконец, в третьем биосенсоре используется тонкая электрохимическая ячейка, в которой происходит прямой перенос электронов с холестериноцсидазы на ферроцен.
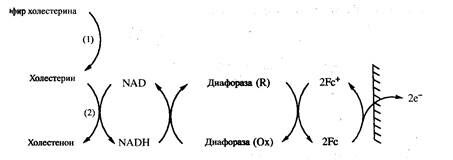
Рис. 2.21. Система сопряжения в биосенсоре на холестерин, включающая NAD+/NADH, диафоразу и ферроцен в качестве медиатора:
1) холестеринэстераза;
2) холестериндегидрогеназа
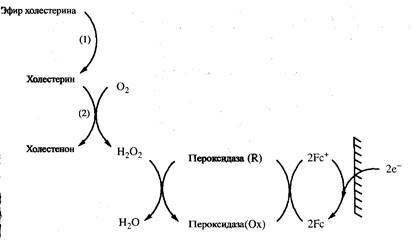
Рис. 2.21. Система сопряжения в биосенсоре на холестерин, включающая окисление холестерина кислородом с образованием перекиси
водорода, пероксидазу и ферроцен:
1) холестеринэстераза;
2) холестериноксидаза
Определение фосфата. Для определения фосфата также можно воспользоваться глюкозным биосенсором. В основе метода лежит тот факт, что фосфат ингибирует щелочную фосфатазу (АР) - фермент, катализирующий превращение глюкозо-6-фосфата в глюкозу.
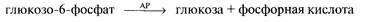
Таким образом, сравнивая количество образующейся глюкозы в
отсутствие и в присутствии ингибитора, можно определить
концентрацию фосфата.
Определение крахмала. Разработан биосенсор для определения крахмала, схема которого представлена на рисунке 2.23.
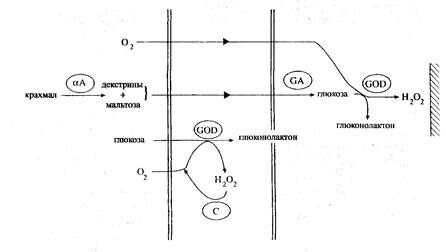
Рис. 2.23. Схема работы двухмембранного биосенсора для
определения крахмала с элиминацией свободной
глюкозы:
аА — а-амилаза;
GOD — глюкозооксидаза;
С — каталаза;
GA — глюкоамилаза
Сенсор основан на измерении концентрации перекиси водорода,
образующейся при окислении глюкозы кислородом в присутствии глю-
козооксидазы. Для того чтобы понять, как работает биосенсор, рас-
смотрим показанные на рисунке ферментативные процессы. Под дей-
ствием а-амилазы крахмал разрушается с образованием декстринов и
мальтозы. Мальтоза же под действием иммобилизованной в биосенсо-
ре глюкоамилазы превращается в глюкозу, которая затем и окисляется
глюкозооксидазой с образованием перекиси водорода.
Биосенсор сконструирован таким образом, чтобы устранить помехи, создаваемые глюкозой, присутствующей в качестве примеси в опре-
деляемом растворе. Для этого в биосенсоре имеются две мембраны.
Глюкоамилаза и глюкозооксидаза иммобилизованы с внутренней сто-
роны первой мембраны в приэлектродном пространстве. С внутренней
стороны второй мембраны иммобилизованы глюкозооксидаза и ката-
лаза. Первый из ферментов катализирует окисление глюкозы, попада-
ющей в межмембранное пространство, а второй — окисление перекиси
водорода с образованием кислорода. Таким образом, ни глюкоза, ни
перекись водорода в качестве примесей не попадают в приэлектродное
пространство.
Определение этанола. Для определения уровня этанола в крови разработано несколько типов биосенсоров.
В одном из них в качестве биологического материала используется
суспензия бактерий — Acetobacter xylinium или Trichosporon brassicae. Оба
вида бактерий катализируют аэробное окисление этанола в уксусную
кислоту:
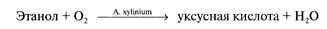
За реакцией следят с помощью кислородного электрода. В биосен-
сорах описанного типа, разработанных в Японии, бактерии иммобили-
зованы методом капсулирования. Линейный диапазон подобных
биосенсоров составляет 5—72 мМ.
В биосенсорах другого типа окисление этанола в уксусную кислоту
происходит под действием алкогольдегидрогеназы (ADH), а электроны
переносятся на электрод через систему сопряжения, включающую
пары NAD'/NADH и [Fe(CN)6]37[Fe(CN)6]4 (рис. 2.24).
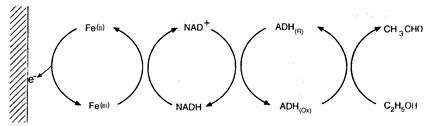
Рис. 2.24. Схема сопряженных реакций в биосенсоре для
определения этанола, включающая алкоголь-
дегидрогеназу, систему NAD+/NADH и [Fe(CN)6]3-/4-
Определение аспирина. Аспирин оказывает терапевтический эффект, когда его концентрация и крови составляет 1,1 —1,2 мМ.
Традиционно уровень аспирина контролируют спектрофотометры
по образованию окрашенного комплекса салициловой кислоты с
Fe3+. (В салициловую кислоту аспирин превращается в организме под
действием эстераз печени).
Однако этот метод неспецифичен. Другой метод определения сали
циловой кислоты основан на ее специфическом окислении в катехол п
присутствии бактериального фермента — NADH-зависимой салит i
латгидроксилазы. На основе этого метода автором данной книги разра
батывается биосенсор, в котором катехол окисляется на печатном грл
фитовом электроде.
Обратите внимание на лекцию "10 Условные графические изображения".
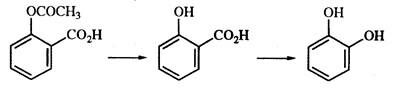
Рис. 2.25. Гидролиз ацетилсалициловой кислоты
(аспирина) и последующее превращение
салициловой кислоты в катехол под действием
салицицилатгидроксилазы
Определение парацетамола (н-ацетил-п-аминофенола). Парацетамол сегодня широко употребляют в качестве обезболивающегоЦ| средства. Однако его передозировка ведет к необратимому поражению печени. По этой причине необходимо иметь метод быстрого опре-
деления концентрации парацетамола в крови, для чего очень удобно
было бы использовать биосенсор. В принципе парацетамол может лег-
ко окисляться на угольно-пастовом электроде, но такой электрод сам
но себе неселективен. Для придания ему селективности можно исполь-
юпать фермент арилациламидазу, который катализирует превращение
парацетамола в п-аминофенол. Последний может окисляться на элек-
троде в хинонимин при значительно меньшем потенциале, чем сам па-
рацетамол. В качестве электрода в этом случае можно использовать пе-
чатный графитовый электрод. Схема реакций, иллюстрирующая оба
способа определения парацетамола, представлена на рисунке 2.26.
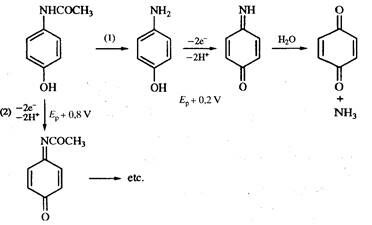
Рис. 2.26. Определение парацетамола:
1) за счет его ферментативного гидролиза (под действием
арилациламидазы) и последующего окисления п-аминофенола на
печатном графитом электроде;
2) за счет прямого окисления парацетамола на угольно-пастовом
электроде



















