Обратимые реакции
Обратимые реакции.
Химические реакции, имеющие принципиальную возможность протекания в прямом и обратном направлениях называются обратимыми. Обратимость химической реакции и обратимость термодинамического процесса не являются одинаковыми понятиями. Обратимый термодинамический процесс – процесс, величина т/д потециалов которого близка к нулю. При этом изменения в системе почти не происходят. Обратимая реакция остается обратимой даже в случае, если т/д функции не равны нулю и система претерпевает изменение в определенном направлении. При этом скорость прямой реакции во много раз больше скорости обратной реакции, но обратная реакция имеет место быть, хотя система претерпевает изменения в «прямом» направлении.
А+В = С+D
Скорость прямой реакции по веществу А будет:
–d[A]/dt = k1[A][B]
Скорость обратной реакции по веществу А будет:
d[A]/dt = k2[C][D]
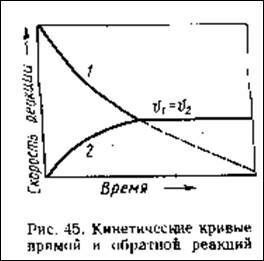
Скорость прямой реакции уменьшается по мере расходования реагентов, скорость обратной реакции при этом увеличивается. Таки образом:
общая скорость реакции в любой момент равна разности скоростей прямой и обратной реакции:
Рекомендуемые материалы
–d[A]/dt = k1[A][B] – k2[C][D]
Обязательно наступает момент, когда скорости реакций уравниваются. Этому условию соответсвует уравнение:
Лекция "Командообразование" также может быть Вам полезна.
k1[A][B] = k2[C][D]
Тогда
k1/k2 = [C][D]/[A][B] = Кр – константа равновения.
Состояние, при котором скорости прямой и обратной реакции равны называют состоянием динамического равновесия.