Влияние температуры на скорость реакции. Энергия активации. Теория Аррениуса
Влияние температуры на скорость реакции. Энергия активации. Теория Аррениуса.
Существует эмпирическое правило, утверждающее, что скорости всех элементарных реакций увеличиваются в 2-4 раза при повышении температуры на 10оС.
Изменение скорости сложных реакций не может быть предварительно определено без оценки температурных зависимостей составляющих элементарных реакций. Особенно это касается обратимых реакций, в которых коэффициенты температурной зависимости обратной реакции могут быть больше соответствующих коэффициентов прямой реакции. В этом случае, повышение температуры приведет, против ожидания, к снижению скорости прямого процесса. В отдельных случаях, причиной резкого снижения скорости реакции может послужить изменение активности катализатора.
Химическое взаимодействие происходит тогда, когда реагирующие молекулы вступают в непосредственный контакт при взаимном соударении. Однако, не все соударения эффективны, но лишь те, в которых участвуют молекулы с определенным избытком кинетической энергии. Такие соударения – эффективные, а минимально необходимый избыток кинетической энергии – энергия активации. Таким образом:
Энергия активации равна разности между наименьшим избыточным запасом энергии, необходимым для взаимодействия, и средней энергией молекул.
Согласно распределению молекул по скоростям Максвелла – Больцмана, в любой системе всегда присутствует нескорое количество молекул, обладающих необходимой для реакции избыточной энергией. Их количество возрастает примерно в 2-4 раза при повышении температуры на 10 оС.
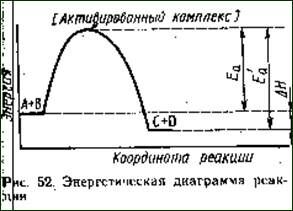
Однако величина энергии активации всегда меньше энергии химической связи. Избыточная энергия активации необходима для создания нестабильной промежуточной частицы – активированного комплекса. Активированный комплекс – нестабильная частица с распределением химических связей промежуточным между исходными веществами и продуктами. Активированный комплекс стабилизируется путем разрушения либо в исходные вещества, либо – в продукты реакции. Процесс разрушения имеет вероятностный характер и преобладание того или иного пути разрушения будет определяться соотношением термодинамических характеристик продуктов и исходных веществ, кинетикой процессов разрушения, наличием катализаторов и проч. Особенно хорошо зарекомендовала себя теория активированного комплекса в органической химии, где механизм реакции как правило подтверждается обнаружением, выделением и изучением структуры промежуточных частиц. Таким образом активированный комплекс - это промежуточная частица, характерная как для прямой, так и для обратной реакции. Тепловой эффект реакции может быть представлен как разность энергий активаций реакций в прямом и обратном направлениях:
Рекомендуемые материалы
DН = Еапр - Еаобр
Таким образом, для прохождения экзотермической реакции в прямом направлении требуется, чтобы Еапр<Еаобр. Если же реакция эндотермична (DН>0), необходима энергетическа «накачка» системы, тогда Еапр>Еаобр
Энергия активации связана с константой скорости реакции:
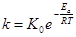
Люди также интересуются этой лекцией: 15 Ряды функций комплексного переменного.
где к – константа скорости реакции;
К0 – предэкспоненциальный множитель, зависящий от характера рассматриваемой реакции;
Еа – энергия активации;
R – универсальная газовая постоянная;
Т – абсолютная температура.
Предэкспоненциальный множитель К0 характеризует выгодную для реакции пространственную ориентацию взаимодействующих молекул и связан с вероятностью нахождения молекул в необходимой для реакции пространственной ориентации орбиталей, т.е. К0 характеризует стерический (пространственный) фактор и не зависит от температуры.




















