Спектр излучения атома водорода. Правила отбора квантовых чисел. Серии излучения атома водорода
Спектр излучения атома водорода. Правила отбора квантовых чисел. Серии излучения атома водорода
Атом водорода (Z = 1) имеет наиболее простой линейчатый спектр излучения. Частоты спектральных линий для атома водорода и водородоподобных атомов определяются по формуле: v = Rv(1/n2 – 1/n'2), где Rv = Z2me4/8ε02h3 = 3,29 · 1015 с-1 – постоянная Ридберга.
Также эта формула может быть записана через длину волны λ: 1/λ = Rλ(1/n2 – 1/n'2), где Rλ = 1,097 · 107 м-1.
Правила отбора – правила, которые на основе законов сохранения квантовых чисел устанавливают допустимые процессы с участием микросистем (молекул, атомов, ядер, элементарных частиц). Любая микросистема характеризуется определённым набором квантовых чисел. В изолированном состоянии эти квантовые числа у микросистемы остаются неизменными, поскольку являются проявлением соответствующих законов сохранения. Так электрический заряд или полный угловой момент  (момент количества движения) изолированной системы не изменяются, так как существуют законы сохранения электрического заряда и углового момента.
(момент количества движения) изолированной системы не изменяются, так как существуют законы сохранения электрического заряда и углового момента.
В нагретом до высокой температуры водороде можно наблюдать характерный линейчатый спектр. Все спектральные линии группируются в серии в зависимости от того, на какой энергетический уровень переходят электроны.
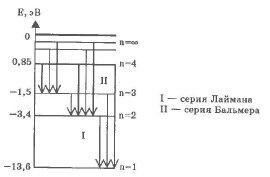
Переходы в первые возбужденные состояния на второй энергетический уровень с верхних уровней образуют серию Бальмера (n = 2), при переходе на первый энергетический уровень с n = 1 образуют серию Лаймана.




















