Diplom98_1 (645656), страница 2
Текст из файла (страница 2)
Кальциевый насос эндоплазматического ретикулума. Во многих эукариотических клетках, наряду с Са2+ насосом плазмалеммы, существует кальциевый насос сарко(эндо)плазматического ретикулума (SERCA). В настоящее время описано по крайней мере 3 различных изоформы SERCA-насосов в клетках млекопитающих. SERCA1-подтип сосредоточен исключительно в быстрых скелетных мышцах, SERCA2-насосы широко распространены в других тканях. Значимость SERCA3-насосов менее ясна (13). Белки SERCA2-насосов разделяются на две различные изоформы: SERCA2а, характерные для кардиомиоцитов и гладких мышц, и SERCA2b, характерные для тканей мозга. Предполагается, что насосы SERCA различными способами регулируются цитоплазматической и интралюминальной концентрациями Са2+: Увеличение [Ca2+]i активирует захват ионов кальция в ЭР, в то время как увеличение свободного кальция внутри ЭР ингибирует насосы SERCA (12). Насосы SERCA эффективно и селективно блокируются тапсигаргином в наномолярных концентрациях (37) и микромолярными концентрациями циклопиазоновой кислоты. Однако, тапсигаргин вызывает также блокаду потенциал - управляемых кальциевых каналов плазмалеммы, как это показано на клетках коркового слоя надпочечников и на сенсорных нейронах (Shmigol et al., 1995), поэтому его следует использовать с некоторой осторожностью.
2.1.5Кальциевые обменники
Дополнительным механизмом, ответственным за вывод ионов кальция из цитоплазмы, является натрий-кальциевый обменник, который выводит Са2+, используя энергию натриевого электрохимического градиента. Наличие Na+- Са2+ обменника было показано в различных типах возбудимых и невозбудимых клеток; в клетках нервной системы он был обнаружен в конце 60-х годов (9). В нейронах моллюска, помещенных в среду с пониженным натрием (т.е. с обратным натриевым градиентом), наблюдалось увеличение [Ca2+]i, что является результатом работы обменника в инвертированной форме. Однако, вклад Na+- Са2+ обменника в регуляцию [Ca2+]i в нейронах млекопитающих до сих пор не оценен. В некоторых работах было показано, что обменник принимает незначительное участие в удалении цитоплазматического Са2+, в то время как в других работах представлены данные о том, что обменник играет существенную роль в переносе Са2+ через мембрану (57).
2.1.6Са2+-связывающие органеллы
Кроме быстрого связывания цитозольного Са2+ внутриклеточными Са2+-связывающими белками, ионы кальция, попадающие в цитозоль, могут аккумулироваться аппаратом Гольджи или клеточным ядром, захватываться митохондриальными Са2+ депо, имеющими достаточно невысокое сродство к Са2+, или быстрыми депо, связанными с ЭР или СР, имеющими высокое сродство к Са2+. Однако если [Ca2+]i превышает 0,5 мкмоль/л, наблюдается существенное перераспределение [Ca2+]i в область митохондрий. Буферные системы митохондрий принимают участие в удалении избыточного Са2+ из цитоплазмы в клетках кишечника, некоторых типах нервных клеток (59) и в секреторных клетках после повышения [Ca2+]i, стимулированного агонистами. Связывание кальция митохондриями обеспечивается активностью систем, расположенных на внутренней митохондриальной мембране. Са2+ поступает в митохондрии по электрохимическому градиенту; разность потенциалов, обеспечивающая транспорт кальция, создается переносом электронов во время клеточного дыхания и связанного с ним переносом протонов. Перенос электронов по дыхательной цепи является основным механизмом, обеспечивающим энергетику транспорта кальция. Подавление дыхательной цепи карбонил-цианид-м-хлорофенил-гидразоном (СССР) эффективно блокирует аккумуляцию кальция митохондриями (41).
2.2Влияние АТФ на кальциевый гомеостаз
Последние исследования показали, что АТФ занимает прочное место в ряду нейромедиаторов центральной и периферической нервной систем (Burnstock 1990). Не вызывает сомнения, что АТФ является не только важнейшим внутриклеточным метаболитом, но и служит важным объектом межклеточного взаимодействия.
2.2.1Строение и свойства АТФ
Рисунок 1. Строение молекулы АТФ
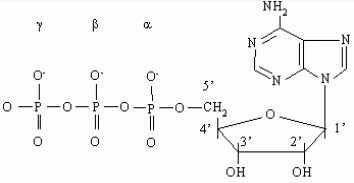 АТФ (см. рис.1) представляет собой нуклеотид и как всякий нуклеотид состоит из трех компонентов: азотистого основания, сахара пентозы и фосфата. В качестве азотистого основания в нуклеотидах присутствуют производные пурина и пиримидина. Фосфаты соединены в полифосфатную цепь, количество которых в естественных нуклеотидах не превышает трех. Однако синтезированы нуклеотиды, содержащие линейные цепи из более чем 3-х фосфатов, к примеру аденозинтетра- и аденозинпентафосфаты.
АТФ (см. рис.1) представляет собой нуклеотид и как всякий нуклеотид состоит из трех компонентов: азотистого основания, сахара пентозы и фосфата. В качестве азотистого основания в нуклеотидах присутствуют производные пурина и пиримидина. Фосфаты соединены в полифосфатную цепь, количество которых в естественных нуклеотидах не превышает трех. Однако синтезированы нуклеотиды, содержащие линейные цепи из более чем 3-х фосфатов, к примеру аденозинтетра- и аденозинпентафосфаты. Названия нуклеотидов, содержащих в качестве сахара рибозу, складываются из названия соответствующего нуклеозида, приставки, обозначающей количество фосфатных групп в нуклеотиде и слова фосфат. Для наиболее распространенных нуклеотидов приняты сокращенные названия, например АТФ для аденозинтрифосфата, ГТФ - для гуанозинтрифосфата, ИМФ - инозинмонофосфата.
В области нейтральных значений pH нуклеиновые основания и рибоза в растворе не заряжены (Мартин, Мариам, 1982). Нуклеотиды, из-за наличия фосфатов, представляют собой сильные кислоты. АТФ содержит четыре ОН группы, способные к ионизации, три из которых имеют pKa ниже 3, а pKa четвертой - 6,5 (Ленинджер, 1976). Таким образом, при pH 7,4 подавляющее большинство молекул АТФ представляют собой четырехзарядные анионы АТФ4- , кроме того, в растворе присутствует небольшое количество АТФ3-.
2.2.2Номенклатура и субклассификация пуринорецепторов.
Первое разделение пуринорецепторов на Р1 и Р2 типы основывалось на следующем критерии: нуклеозиды такие как аденозин активировали Р1 пуринорецепторы, в то время как АТФ стимулировала Р2 пуринорецепторы, а метилксантины (кофеин, теофиллин) являются селективными антагонистами Р1 пуринорецепторов. Также Р1 пуринорецепторы связаны с аденилатциклазой, а активация Р2 пуринорецепторов может приводить к выработке простогландинов (Burnstock 1978).
2.2.3Р1 пуринорецепторы.
В 1979 году (Van Calker et al 1979) показали, что аденозиновые, Ð1 - пуринорецепторы можно подразделить на две группы. Рецепторы одной из них обладали очень высоким сродством к аденозину (константа диссоциации Кd = 3 - 10 нМ). При взаимодействии аденозина с этой группой рецепторов наблюдалось ингибирование аденилатциклазы и, следовательно, уменьшался уровень внутриклеточного цАМФ. Этот класс рецепторов был назван А1 -рецепторами (Ri рецепторы по (Londos et al 1980)). Аденозиновые рецепторы, относящиеся ко второй группе, имели более низкое сродство к аденозину (Кd комплекса аденозина с рецептором 5-10 мкМ). Активация этого типа рецепторов приводила к стимуляции аценилатциклазы. Эти рецепторы Ван Колкер назвал А2-рецепторами (Ra рецепторы по (Londos et al 1980)). Были обнаружены также и мощные антагонисты для А1 - R-N6-Фенилизопропиладенозин (R-PIA). Для А2 более сильным антагонистом был 5’-N-этилкарбоксамидаденозин (NЕСА). Также существуют работы, в которых описываются аденозиновые рецепторы, не связанные с аденилатциклазой эти пуринорецепторы было предложено назвать А3 (Ribeiro and Sebastiao 1986). Предпосылкой к разделению А2 пуринорецепторов на А2а и А2b подтипы стало открытие разного сродства NECA к Р1 пуринорецептору, - высокого в стриатуме (А2а) и низкого в фибробластах (А2b) (Bruns et al 1986).
2.2.4Р2 пуринорецепторы
Накопленные фармакологические доказательства, как-то: тип ответа, порядок активности агонистов, десенситизация, вызываемая АТФ и ее структурными аналогами, послужили основой для первого субделения Р2 пуринорецепторов. В 1985 году Бернсток и Кеннеди (10) указали на неоднородность популяции Р2-пуринорецепторов. Этот вывод был сделан исходя из того, что в некоторых тканях (например продольная мышца слепой кишки) АТФ вызывал расслабление гладких мышц, а в других (мышечная стенка мочевого пузыря) - сокращение. Первый подтип рецепторов был обозначен как Р2у, а второй - Р2х. Для Р2х пуринорецепторов наиболее активным агонистом был , - метилен АТФ (,-мАТФ), а для Р2у - 2 - метилтио АТФ (2-МеSАТP). Так как порядок активности лигандов может зависеть от скорости их гидролиза до неактивных соединений, которая может значительно различаться в зависимости от ткани, более четким доказательством для подразделения Р2 - рецепторов на подтипы служит наличие селективных блокаторов. Сейчас известны селективные антагонисты как для Р2х, так и Р2у-рецепторов для Р2х - ,-мАТФ (десенситизирующее действие), арилазидаминопропионил АТФ (АНАПП3), пиридоксалфосфат-6-азофенил-2’,4’-дисульфидная кислота (PPADS), сурамин и другие; для Р2у пуринорецепторов - реактив голубой 2, сурамин. В 1986 году Гордон (23) предложил выделить из класса Р2 пуринорецепторов еще два подтипа Р2t и Р2z. Первый рецептор располагается в тромбоцитах и управляет их агрегацией. Он, в отличие от всех остальных подтипов P2 - рецепторов, активируется АДФ, и блокируется АТФ. Р2z рецепторы расположены в тучных клетках. В них АТФ в очень больших концентрациях (> 100 мкМ), а точнее четырехзарядный анион АТФ4-, вызывал кальцийзависимую секрецию гистамина. Другие пуриновые нуклеотиды, включая негидролизуемые аналоги АТФ, не активировали рецептор. Также был обнаружен неселективный антагонист данного типа рецепторов DIDS - аналог PPADS (Soltoff et al 1993). В 1991 году O’Connor предложил так называемый нуклеотидный рецептор одинаково чувствительный как к АТФ, так и к УТФ, но не чувствительный к 2 - MeSATP. Этот рецептор получил обозначение Р2u. Возможным антагонистом данного рецептора является сурамин. Также было обнаружено, что аденин динуклеотид полифосфаты также присутствуют в фармакологической периферии (Hoyle 1990). Hildermann (1991) индентифицировал сайт связывания для диаденозин тетрафосфата ( Ap4A) в мозге крысы, который получил название дипуринергического рецептора, а позднее Р2d (Pintor et al 1993). Антагонисты данного вида пуринорецепторов пока не обнаружены.
| пуринорецепторы | |||||||||||||||||||||||||||||
| Р1 - пуринорецепторы | Р2 - пуринорецепторы | ||||||||||||||||||||||||||||
| A1 | A2a | A2b | A3 | P2x | P2y | P2t | P2z | P2u | P2d | ||||||||||||||||||||
Таблица 1. Классическая схема субклассификации пурино-рецепторов.
2.2.5Реклассификация пуринорецепторов.
Из - за всевозрастающих трудностей и несогласований в классической схеме классификации Ð2 пуринорецепторов и увеличивающемся числе подтипов рецепторов, стало очевидным, что классическая схема требует пересмотра. В 1994 году Abbracchio and Burnstock предложили новую схему классификации Р2 - пуринорецепторов. Из всех Р2 - пуринорецепторов они вычленили три основных семейства: Р2Х семейство, связанное с ионотропными каналами, которое включало четыре подтипа; Р2У - связанное с активацией G - белков, включающее семь подтипов и семейство Р2Z - семейство неселективных пор. Их гипотеза основывалась в основном на изучении литературных источников и анализе фармакологического профиля новообнаруженныж агонистов. В дальнейшем теория подтвердилась клонированием различных подтипов Р2 - пуринорецепторов. В настоящее время семейство Р2Х насчитывает шесть, а Р2У - семь подклассов. Благодаря интенсивным исследованиям, практически не остается сомнений в том, что данные семейства будут расти и дальше (Collo et al 1996).
| Р2 - пуринорецепторы | ||||||||||||||||||||||||||||||||||||||||
| P2Z - неселективные поры | ||||||||||||||||||||||||||||||||||||||||
| Р2Х - семейство ионотропных рецепторов | Р2У - семейство метаботропных рецепторов | |||||||||||||||||||||||||||||||||||||||
| Р2Х1 | Р2Х2 | Р2Х3 | Р2Х4 | Р2Х5 | Р2Х6 | Р2У1 | Р2У2 | Р2У3 | Р2У4 | Р2У5 | Р2У6 | Р2У7 | ||||||||||||||||||||||||||||
Таблица 2. Современная классификация Р2 типа пуринорецепторов.
3.ОБЪЕКТ И МЕТОДЫ ИССЛЕДОВАНИЙ
3.1Подготовка препарата
Исследования проводились на пирамидальных нейронах моторной области новой коры в тонких срезах мозга, выделенного из 14 дневных крыс. После декапитации мозг помещался в холодный солевой раствор (0 - 40С). Процедура от начала декапитации до выделения мозга длилась не более 60-90 секунд. Затем мозг закреплялся полиакриламидным клеем на подложке вибротома (Campden, Campden Instruments LTD, U.K.); камера вибротома заливалась холодным солевым раствором. Срезы нарезались сагитально толщиной 250 - 300 мкм; скорость подачи лезвия - 1 см/с с частотой 10 Гц. После приготовления срезы помещались в раствор постоянно насыщаемый карбогеном (5% СО2 + 95% О2). Перед загрузкой флуоресцентным красителем срезы инкубировались в постоянно оксигенируемом растворе 30 минут при температуре 32 градуса. Окраска среза осуществлялась в течении 30 - 35 минут в СО2 насыщенном термостате при температуре 35 градусов. После окраски срезы отмывались 1 - 1,5 часа в постоянно оксигенируемом растворе при комнатной температуре. Все эксперименты проводились при температуре 32 градуса.
3.2Характеристики кальциевого зонда

















