Патогенез злокачественных опухолей
1. Патогенез злокачественных опухолей. Клеточные и молекулярные механизмы канцерогенеза
Согласно господствующему в онкологии мнению в подавляющем большинстве случаев в основе злокачественного перерождения клеток лежат мутации. Однако, далеко не каждая мутация приводит к появлению клона опухолевых клеток. Более того, по мнению ряда исследователей до 95% повреждений ДНК клеткам удается «залечить» за счет деятельности репаразных систем[1]/ . Если же повреждение ДНК не удается исправить, «в запасе» у клетки имеются и другие дополнительные генетически обусловленные программы предупреждения образования клона малегнизированных клеток. Во-первых, в клетке может запуститься программа апоптоза – программированной клеточной гибели, «самоубийства клетки», а во-вторых, программа, блокирующая клеточный митоз, то есть опять же механизм, препятствующий размножению опухолевой клетки.
Прежде чем более подробно рассмотреть как сам патогенез злокачественных опухолей, так и механизмы, препятствующие появлению клонов малегнизированных клеток, остановимся хотя бы кратко на том, как регулируется сам процесс митоза, так как «опухоль – это патологический процесс, характеризующийся безудержным размножением клеточных элементов».
6.1. Регуляция митотического цикла клетки
Запуск цикла клеточного деления начинается с присоединения молекулы росткового фактора к соответствующему клеточному рецептору. Факторов роста (регуляторов пролиферации) чрезвычайно много. Как правило, это полипептиды, состоящие из 40 – 50 аминокислот. Наиболее известны из них EGF (epidermal growth factor – эпидермальный фактор роста), PDGF (platelet-derived growth factor – тромбоцитарный фактор роста), инсулиноподобные ростовые факторы – IGF-I, IGF-II, ростовой фактор фибробластов и другие. Условно к ростовым факторам, а точнее – к «антиростовым» факторам, можно отнести такие вещества как «фактор некроза опухолей» - TNF, трансформирующий фактор роста – TGF-b, интерфероны, которые, соединяясь с соответствующими рецепторами, подавляют пролиферацию.
Было показано, что инсулиноподобные факторы роста, в частности, IGF-I, играют значительную роль в канцерогенезе и увеличение их концентрации в крови служит своеобразным маркером предрасположенности к развитию онкологических заболеваний. Так у мужчин увеличение концентрации фактора IGF-I напрямую связано с возможным образованием рака предстательной железы.
Соединение ростовых факторов с рецепторами инициирует сложный каскад реакций фосфорилирования, в результате чего в конечном итоге митогенный сигнал достигает генетического аппарата клеточного ядра. В последнем благодаря действию транскрипционных факторов активируется группа генов, ответственных за митоз клетки. В результате, через синтез РНК и, в последующем, через синтез белков, происходит синтез и репликация ДНК, что и определяет начало митоза.
Клеточный (митотический) цикл начинается с фазы G1 – подготовки к синтезу ДНК. За ней следуют фазы S – фаза синтеза ДНК и фаза G2 – постсинтетическая (Рис. 2). Завершается цикл митозом клетки. На протяжении цикла следует выделить особый период – так называемую точку «рестрикции R», когда для клетки «решается» вопрос – войдет ли она в следующий цикл деления, или останется в покое.
Рекомендуемые материалы
Весьма важными являются и еще два момента в жизни клетки, вошедшей в митотический цикл. Это так называемые «контрольные пункты» (checkpoints): на границе фазы G1/S и на границе фазы G2/митоз. На уровне контрольных пунктов проверяется целостность ДНК, отсутствие ее мутаций и делеций. У клеток, имеющих поврежденную ДНК, клеточный цикл блокируется, или клетка вступает в стадию апоптоза. И в том, и в другом случае предупреждается возможность передачи по наследству вредных для клеточной популяции признаков в частности таких, как способность клетки к безудержному размножению без явления созревания, то есть предупреждается возможность злокачественной трансформации клетки.
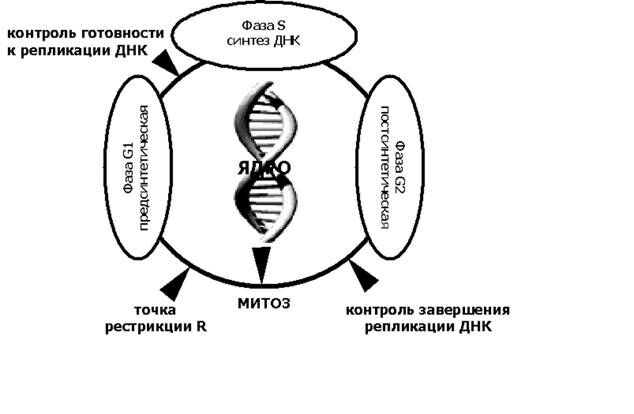
Рис. 2. Схема регуляции митотического цикла клетки (по А.В.Лихтенштейн, В.С.Шапот).
Пояснения в тексте.
В регуляции митотического цикла важную роль играют циклины (Рис. 3). Циклины – это белки, обеспечивающие переход клетки из одной фазы митотического цикла в другой. Иначе говоря, точкой приложения циклинов являются основные пункты контроля над допуском клетки к синтезу ДНК и завершением репликации ДНК и входом клетки в митоз. Циклины вступают в действие только в том случае, если «надзирающие системы» клетки «уверены» в том, что геном клетки не претерпел каких либо мутаций и ее потомство не будет иметь вредных для организма качеств.
Рождаясь в строго определенные периоды митотического цикла, циклины сами по себе не способны оказывать какого-либо влияния на переход клетки из одного предмитотического состояния в другое. Эту роль играют различные протеинкиназы, которые без соединения с соответствующим циклином неактивны. Активированные же протеинкиназы способны индуцировать специфические процессы, обеспечивающие митоз (например, дезинтеграцию ядерной мембраны, конденсацию хроматина и т.п.).
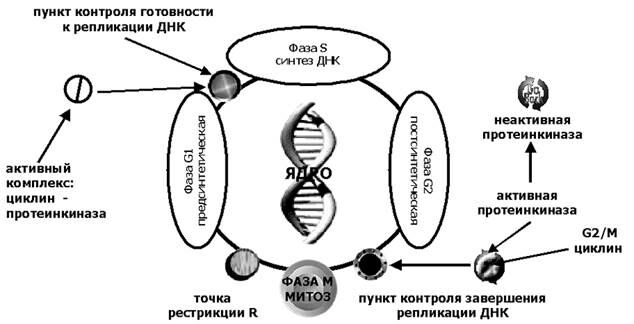
Рис. 3. Роль циклинов в регуляции митотического цикла (по А.В.Лихтенштейн, В.С.Шапот).
Пояснения в тексте.
Выделяют три основные класса циклинов: G1/S-циклины, необходимые для перехода клетки в фазу синтеза ДНК; S-циклины, обеспечивающие прохождение клеткой фазу синтеза ДНК, и G2/M-циклины, непосредственно переводящие клетку в состояние митоза.
Для нормального функционирования митотического цикла важно не только своевременное появление циклинов, но и их исчезновение, что обеспечивается их деградацией или блоком синтеза. Если циклины своевременно не исчезают, переход клетки из одной фазы митотического цикла в другую блокируется.
6.2. Роль онкобелков, факторов роста и опухолевых белков-супрессоров в малегнизации
клетки
В 80-е годы в онкологии было сформулировано понятие о протоонкогенах, то есть об участках (последовательностях) ДНК нормальных клеток, гомологичных вирусным онкогенам. Переход (трансформация) нормального для клетки гена – протоонкогена в онкоген возможен в результате мутации или другого повреждения клетки (Рис. 4). В норме протоонкогены – это «акселераторы» клеточного деления, обеспечивающие смену одной фазы клеточного цикла на другую за счет образования активного циклин-киназного комплекса, без помощи которого невозможно перевести клетку в фазу синтеза ДНК и, далее, в фазу репликации ДНК и осуществления собственно митоза. При этом нормальный митотический цикл, обеспеченный дея-
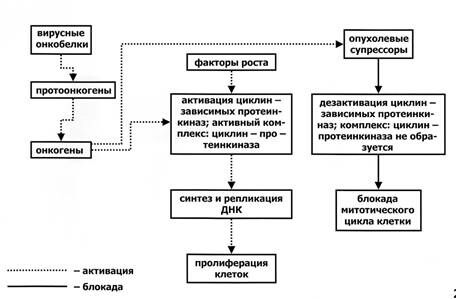
Рис. 4. Роль онкобелков, факторов роста и опухолевых белков-супрессоров в малегнизации
клетки (пояснения в тексте).
тельностью протоонкогенов, развертывается только в течение того времени, пока на клетку действует митотический сигнал, воспринимаемый клеткой через рецептор ростового фактора.
В случае же повреждения протоонкогена каким либо фактором, кодируемый им белок (или – белки), обеспечивающий передачу митотического сигнала, продолжает вновь и вновь бесконтрольно «раскручивать» митотический цикл, а клетка безудержно пролиферировать. Иначе говоря, протоонкоген трансформируется в онкоген.
Однако каждая клетка организма имеет свой «контрольный механизм», не позволяющий развиться состоянию безудержной пролиферации. Это, прежде всего, наличие в клетке опухолевых белков-супрессоров, которые способны блокировать клеточный цикл на уровне нескольких «контрольных пунктов». Другим способом, позволяющим предотвратить неконтролируемую пролиферацию и малигнизацию клетки, является апоптоз – программированная гибель клетки.
6.3. Апоптоз – защитная реакция на возможное злокачественное перерождение
клетки
Апоптоз («программированная гибель клетки») – это мощная защитная система организма, реализуемая на клеточном уровне, и способная предотвратить появление «потомства» клетки, обладающего вредными для организма качествами (Рис. 5). Понятие «вредное качество» в полной мере относится к возможности возникновения в организме клеток, получивших в ре-
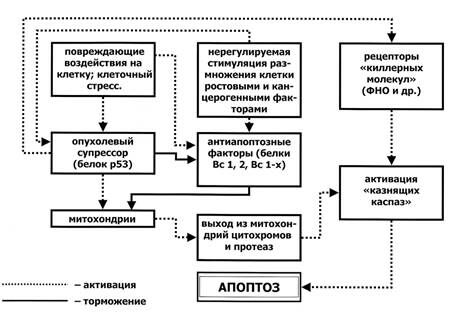
Рис. 5. Апоптоз – защитная реакция на возможное злокачественное перерождение клетки
(пояснения в тексте).
зультате мутаций способность к безудержному размножению без явления созревания, то есть клеток злокачественных опухолей.
Повреждение генома клетки, в том числе и ее малигнизация, может быть вызвана различными факторами. Во-первых, это всевозможные повреждения клетки (воспаление, гипоксия, тепловая травма, радиационные повреждения и т.п.). Во-вторых, - это нерегулируемое воздействие на клетку всевозможных факторов роста, а также различных канцерогенов (включая вирусные канцерогены). Защита клетки от злокачественного перерождения обеспечивается семейством опухолевых супрессоров (белков), главную роль среди которых играет белок р53, который и является основным инициатором апоптоза.
Инициация апоптоза осуществляется двумя путями: за счет дополнительного образования клеточных рецепторов к так называемым «киллерным молекулам», благодаря чему эти рецепторы активно соединяются с молекулами фактора некроза опухолей (ФНО-a) и другими «антиростовыми» веществами, а также за счет воздействия (через ряд посредников) на митохондрии и увеличение проницаемости их мембран для цитохромов и некоторых протеаз (более подробно эти механизмы описаны в главе учебника «Патофизиология клетки»).
В первом случае сигнал от возбужденных рецепторов через несколько исполнительных механизмов клетки обеспечивает активацию так называемых «казнящих каспаз», благодаря которым происходит фрагментация ДНК, разрушение цитоскелета клетки и, в конечном итоге, ее деструкция. Во втором случае – вышедшие из митохондрий цитохромы и протеазы, так же способствуют активации «казнящих каспаз», чем в свою очередь интенсифицируют апоптоз.
Информация в лекции "3.1 Начало разложения феодально-крепостнического строя" поможет Вам.
Напомним, что одновременно с механизмом запуска апоптоза в клетке, подвергнувшейся повреждению, запускается и антиапоптотический механизм. Развитию апоптоза препятствуют антиапоптотические белки группы Bcl 2, Bcl-x. Полностью все нюансы их действия до сих пор не известны, однако, есть данные о том, что эти белки, встраиваясь в мембраны митохондрий, препятствуют образованию в ней каналов, через которые в протоплазму клетки выходят цитохромы и протеазы.
Таким образом, малигнизация клетки может быть предотвращена только в том случае, если механизмы запуска и осуществления апоптоза будут превалировать над антиапоптотическими механизмами.
6.4. Генетические предпосылки канцерогенеза
Мы уже убедились в том, что мутагенные воздействия на клетки организма могут быть весьма разнообразными. В их число входят радиационные повреждения генома клетки, воздействие на нее вирусов и химических канцерогенов, чрезмерные атаки на клетку со стороны ростовых факторов, наконец, «клеточный стресс», возникающий в результате повреждающего действия свободных радикалов. При этом в нормальной клетке мутировать могут протоонкогены, превращающиеся в онкогены, а также гены противоопухолевых супрессоров и гены, ответственные за деятельность репаразных систем. В результате клетка теряет способность исправлять повреждения молекулы ДНК, утрачивает возможности блокировать митотический цикл, а нарастающие изменения генома (например, амплификация[2]/ патологических генов) вызывает появление у клетки свойств морфологического и метаболического атипизма. Схематично эти процессы изображены на Рис. 6.
[1]/ Репаразная система клетки обеспечивается участием нескольких ферментов: эндонуклеазы, вырезающей поврежденный участок ДНК; эндонуклеазы, разрушающей этот поврежденный участок; ДНК-полимеразы, синтезирующей восстановляемую последовательность нуклеотидов по матрице комплементарной цепи ДНК и лигазы, встраивающей вновь синтезированный участок в поврежденную цепь ДНК
[2]/ Амплификация (применительно к опухолевым клеткам) – увеличение числа копий генов в клетке за счет патологического копирования определенных последовательностей ДНК



















