Часть 6
СПЕЦИФИЧЕСКИЕ ПУТИ ОБМЕНА ОТДЕЛЬНЫХ АМИНОКИСЛОТ.
Эти пути обмена определяются различиями в строении радикалов аминокислот /АК/, поэтому они разнообразны и многочисленны. Вступая в эти специфические реакции, АК-ты принимают участие во многих важных процессах:
а) в синтезе гормонов и нейромедиаторов,
б) в синтезе простетических групп сложных белков - хромопротеинов и нуклеопротеинов,
в) в синтезе сложных липидов,
г) синтезе веществ, содержащих макроэргическую связь и являющихся источником энергии для клеток,
д) в обезвреживании токсических веществ.
Вступая в эти процессы, АК-ты участвуют в них как всей своей молекулой, так и своими отдельными фрагментами (или группировками). Ими являются аминогруппа (NH2) и одноуглеродные фрагменты: -СН3, -CH2-, -С=О, -СН= , -СН2ОН.
Одноуглеродные фрагменты образуются из простейших аминокислот - глицина, серина, аланина и треонина под действием ферментов, коферментом которых является тетрагидрофолиевая кислота/ТГФК/. ТГФК - производное витамина Вс (фолиевой кислоты), она образуется из фолиевой кислоты в результате ее восстановления с помощью НАДФН2. Одноуглеродный фрагмент, соединенный с ТГФК называют активным одноуглеродным фрагментом или " активный С1".
Рекомендуемые материалы
ОБМЕН ГЛИЦИНА И СЕРИНА.
Это заменимые аинокислоты, которые превращаются друг в друга.
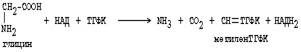
Основным путем распада глицина является его распад на СО2, Н2О и метилен-ТГФК (активный С1):
|
|
Из метилен-ТГФК могут образовываться все другие формы активного С1: формил-ТГФК, метил-ТГФК, метен-ТГФК, оксиметил-ТГФК в результате реакций окисления или восстановления метилен-ТГФК.
Активный С1, образовавшийся из глицина участвует в синтезе пуриновых азотистых оснований. Кроме того, глицин всей своей молекулой участвует в синтезе гема гемоглобина и других гемопротеинов, в синтезе пуриновых азотистых оснований, в синтезе парных желчных кислот (гликохолевая кислота), в синтезе креатина, в синтезе трипептида глютатиона. Также глицин в печени участвует в обезвреживании бензойной кислоты, которая превращается в гиппуровую кислоту: 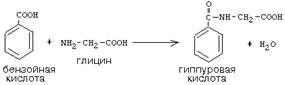
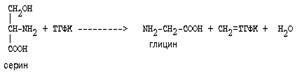
Основным путем распада серина является его превращение в метилен-ТГФК и глицин:
|
|
Всей своей молекулой серин участвует в синтезе сложных липидов - фосфолипидов. Он участвует в синтезе фосфатидилсерина, который декарбоксилируется и превращается в фосфатидилэтаноламин, который после метилирования превращается в фосфатидилхолин. В реакции метилирования участвует активная форма метионина - S-аденозилметионин.
Серин в составе белков-ферментов участвует в формировании каталитического центра фермента, например, в сериновых протеазах: трипсине, химотрипсине и др. Также серин участвует в формировании гидратной оболочки белков, потому что является полярной аминокислотой.
ОБМЕН СЕРУСОДЕРЖАЩИХ АМИНОКИСЛОТ: МЕТИОНИНА И ЦИСТЕИНА.
Метионин - это незаменимая аминокислота, а цистеин - заменимая.
|
|
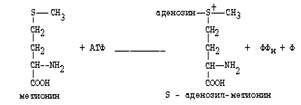
Главной особенностью обмена метионина является то, что из него тоже образуется активный С1 в виде СН3-группы, которая участвует в различных синтезах. Однако, этот активный С1 образуется без участия ТГФК. Чтобы стать источником СН3- группы, метионин подвергается активации с участием АТФ. В результате этой реакции от АТФ отщепляются все три остатка фосфорной кислоты, а аденозин присоединяется к атому серы метионина. Так образуется активная форма метионина - S- аденозил-метионин.
S-аденозил-метионин участвует в реакциях трансметилирования. Наиболее важный из них синтез фосфатидилхолина из фосфатидилэтаноламина, обезвреживание биогенных аминов с участием О-метилтрансфераз, синтез адреналина из норадреналина, синтез ацетилхолина из холина и Ацетил-КоА, синтез креатина, который в виде креатинфосфата является резервной формой макроэргических связей и участвует в обеспечении нервной ткани и работающей мышцы АТФ.
Синтез креатина.
|
|
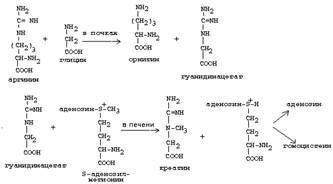
В синтезе креатина участвуют и другие аминокислоты - аргинин и глицин. В почках из аргинина и глицина образуется гуанидинацетат, который метилируется в печени с участием S-аденозил-метионина и в результате образуется креатин:
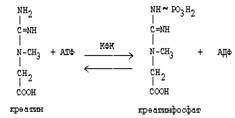
Гомоцистеин участвует в синтезе амикислот - цистеина (гомоцистеин + серин). Креатин подвергается фосфорилированию с участием АТФ, в результате образуется соединение с макроэргической связью - креатинфосфат. Это обратимая реакция, которая катализируется ферментом креатинфосфокиназой (КФК).
|
|
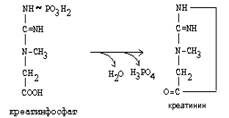
Эта реакция интенсивно идет в мышцах, особенно, в сердечной мышце, и в ткани мозга. Креатинфосфат активно синтезируется в покое и распадается при мышечной работе. Это наиболее быстрый способ регенерации АТФ. Креатин, образовавшийся из креатинфосфата распадается до креатинина, который является конечным продуктом и выводится с мочой. В сутки выводится 1-2 грамма креатинина. Это количество креатинина прямо пропорционально мышечной массе, поэтому у мужчин креатинина в моче больше, чем у женщин. Креатинин не реабсорбируется из первичной мочи, поэтому его количество во вторичной моче характеризует объем клубочковой фильтрации.
|
|
При поражении мышечных клеток и нарушении ткани мозга креатинфосфокиназа появляется в крови, это является диагностическим признаком. Известно, что КФК имеет три изофермента - кардиальный, церебральный и мышечный, появление их в крови позволяет определить поражение соответствующего органа. Появление в крови кардиального изофермента является ранним диагностическим признаком инфаркта миокарда.
ОБМЕН ЦИСТЕИНА.
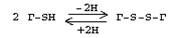
Это заменимая аминокислота, она синтезируется из серина, гидроксильная группа которого замещается SН-группой, которую поставляет гомоцистеин. Цистеин в составе белков-ферментов своей -SН группой участвует в образовании каталитического центра (тиоловые протеазы), а также участвует в образовании дисульфидных связей, которые принимают участие в формировании третичной и четвертичной структуры белков. Также цистеин необходим для синтеза трипептида глютатиона, который состоит из цистеина и глютаминовой кислоты. Молекула глутатиона условно обозначается как (Г-SН). Глютатион способен легко окисляться и восстанавливаться:
|
|
Окисляясь, глютатион предохраняет от окисления другие вещества, например, двухвалентное железо гемоглобина в эритроцитах:
|
|
Восстанавливается глютатион с помощью НАДФН2 с участием фермента глютатионредуктазы.

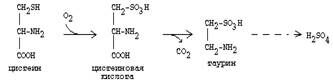
Цистеин подвергается и распаду, при этом он окисляется и декарбоксилируется, в результате образуется таурин, который участвует в образовании парных желчных кислот (таурохолевая и др.) в печени.
|
|
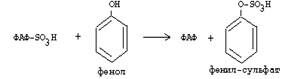
Серная кислота, которая образуется из таурина, участвует в обезвреживании токсических веществ в печени.
|
|
Так обезвреживаются продукты гниения белков в кишечнике - индол, скатол, фенол и крезол. В этих процессах серная кислота участвует в своей активной форме в виде 3’-фосфоаденозин-5’-фосфосульфата (ФАФC), которая образуется с участием АТФ.
ОБМЕН АРГИНИНА
Аргинин - частично незаменимая аминокислота. Она образуется в ходе синтеза мочевины в печени из карбомоилфосфата при участии аспарагиновой кислоты и орнитина. Аргинин участвует в синтезе креатина в почках, являясь донором гуанидиновой группы в образовании гуанидинацетата. В составе белков аргинин как полярная положительно заряженная аминокислота участвует в образовании ионных связей и в формировании гидратной оболочки белков.
Информация в лекции "16. Проблема острых кишечных инфекций" поможет Вам.
ОБМЕН ДИКАРБОНОВЫХ АМИНОКИСЛОТ - ГЛУТАМИНОВОЙ И АСПАРАГИНОВОЙ
Эти аминокислоты вступают в многочисленные химические реакции, с которыми Вы уже знакомы и поэтому они играют главную роль в обмене аминокислот.
1. Они участвуют в реакциях синтеза заменимых аминокислот и следовательно в коррекции аминокислотного состава белков, а, значит, в коррекции аминокислотного состава клеток организма.
2. Участвуют в реакциях обезвреживания аммиака и других токсичных продуктов азотистого обмена.
3. Превращаясь в альфа-кетокислоты (альфакетоглутарат и ЩУК), они принимают участие во взаимосвязи обмена белков с обменом углеводов и жиров.
4. Дикарбоновые аминокислоты и их амиды (глутамин и аспарагин) участвуют в реакциях синтеза почти всех азотсодержащих соединений клеток (нуклеотидов, нуклеиновых кислот, аминосахаров и аминопроизводных липидов). В этих реакциях синтеза они являются донором азота в виде NН2-группы, или участвуют всей своей молекулой.