Общие сведения о горении
ОБЩИЕ СВЕДЕНИЯ О ГОРЕНИИ
Горение представляет собой процесс окисления, или взаимодействия горючего вещества с кислородом воздуха. Окислителями в процессе горения могут быть также хлор, бром, азотная кислота, бертолетова соль, пероксид натрия и некоторые другие вещества.
Для возникновения и развития процесса горения необходимы горючее вещество, окислитель и источник зажигания, инициирующий реакцию между горючим и окислителем.
Горючее и окислитель должны находиться в определенных соотношениях друг с другом.
Горение, как правило, происходит в газовой фазе, поэтому горючие вещества, находящиеся в конденсированном состоянии для возникновения и поддержания горения должны подвергаться газификации (испарению, разложению), в результате чего они образуют газообразную горючую смесь.
В зависимости от агрегатного состояния горение бывает гомогенным и гетерогенным.
Гомогенное горение характерно для горючих смесей, в которых компоненты находятся в газообразном состоянии. Причем если компоненты предварительно перемешаны, то такое горение называют кинетическим. Если компоненты предварительно не перемешаны, то происходит диффузионное горение.
Гетерогенное горение, характеризуется наличием поверхности раздела фаз в горючей системе.
Рекомендуемые материалы
Горение различается также по скорости распространения пламени:
1. Дефлаграционное горение (несколько метров в секунду)
2. Взрывное горение (до сотен метров в секунду)
3. Детонационное (скорость детонации несколько тысяч метров в секунду)
Различают: ламинарное и турбулентное.
Ламинарное горение характеризуется послойным распространением фронта пламени по свежей горючей смеси.
Турбулентное горение характеризуется перемешиванием слоев потока и повышенной скоростью сгорания.
В зависимости от соотношения горючего и окислителя горючие смеси подразделяются на:
1. Бедные - содержащие в избытке окислитель по сравнению со стехиометрическим соотношением компонентов.
2. Богатые - содержащие в избытке горючее.
Стехиометрическое отношение - исходное соотношение компонентов горючей смеси, при сгорании которой ни один из исходных компонентов не остается в избытке в продуктах реакции.
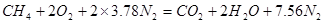
Расчет стехиометрического содержания горючего вещества для наиболее распространённых углеводородов и их производных осуществляется по формуле:
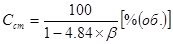
Стехиометрический коэффициент равен: 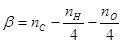
здесь nс, nн, n0 — соответственно числа атомов С, Н и О в молекуле горючего.
Для СН4: 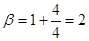
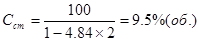
Реальные пожары характеризуются, как правило, диффузионным, гетерогенным, турбулентным и дефлаграционным горением.
Взрывное горение происходит при утечке горючего газа из трубопроводов или испарении разлитой жидкости, при содержании горючей пыли в воздухе.
Горение может осуществляться в двух режимах:
1. В режиме самовоспламенения, заключающемся в самопроизвольном возникновении пламенного горения предварительно нагретой до некоторой критической температуры горючей смеси (называемой температурой самовоспламенения) и проявляющегося в одновременном (в виде вспышки) сгорании всей горючей смеси;
2. В режиме распространения волны горения (распространения фронта пламени) по холодной смеси при ее локальном зажигании (воспламенении) внешним источником.
Пламя — это видимая зона горения, в которой наблюдаются свечение и излучение тепла. Возникшее в результате воспламенения пламя само становится источником потока тепла и химически активных частиц в прилегающие слои свежей горючей смеси.
Для изучения распространения волны горения поставим опыт. Поместим гомогенную горючую смесь в стеклянную трубку, открытую с одного конца и воспламеним ее источником зажигания у открытого конца. Тепло из зоны реакции благодаря теплопроводности распространяется на исходную холодную смесь и нагревает ее.
Свежая горючая смесь и продукты сгорания разделены узкой зоной, называемой фронтом пламени, представляющим собой тонкий сферический слой (толщиной менее 10-6 м), где происходит прогрев горючей смеси и быстрая химическая реакция. Тепло из зоны реакции благодаря теплопроводности распространяется на исходную холодную смесь и нагревает её. Происходит также диффузия продуктов реакции и активных радикалов из зоны реакции в исходную смесь и исходной смеси в зону реакции. Таким образом, зона реакции перемещается в направлении исходной горючей смеси. Такое ламинарное горение называется нормальным.
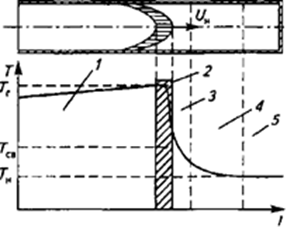
Рис. 1. Изменение температуры перед фронтом пламени и за ним:
1 — зона продуктов горения; 2 — фронт пламени; 3 — зона самовоспламенения;
4 — зона предварительного прогрева; 5 — исходная смесь.
Скорость перемещения пламени по неподвижной смеси вдоль нормали к его поверхности — нормальной скоростью распространения пламени Uн. Величина Uн, являясь физико-химической константой горючей смеси, представляет собой минимально возможную величину, которая не зависит от условий, а определяется лишь химическим составом горючей смеси и соотношением горючего и окислителя.
При закрытой трубке продукты горения давят на фронт пламени и стенки, увеличивая скорость его перемещения. Суммарная скорость такого перемещения называется видимой скоростью.
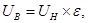
где  ., ε – степень расширения продуктов сгорания; ТГ и TН — температуры горения и начальная; η – отношение числа молей продуктов сгорания к числу молей исходной смеси (для углеводородных горючих веществ значение η близко к единице).
., ε – степень расширения продуктов сгорания; ТГ и TН — температуры горения и начальная; η – отношение числа молей продуктов сгорания к числу молей исходной смеси (для углеводородных горючих веществ значение η близко к единице).
При воспламенении горючей смеси в длинной трубе в результате расширения продуктов сгорания возникают волны сжатия; фронт пламени вместе с горючей смесью вовлекается в быстрое движение со скоростью, в 10—20 раз выше чем величина  .
.
Дальнейшее развитие процесса связано с турбулизацией потока газа перед фронтом пламени и увеличением скорости распространения пламени. В конечном счёте, возникают условия для адиабатического самовоспламенения горючей смеси – т.е. детонации.
Таким образом, при детонации пламя распространяется не в результате теплопроводности, а вследствие ударной волны, приводящей к быстрому нагреву и самовоспламенению смеси. За ударной волной возникает зона быстрой реакции; вместе они образуют детонационную волну, которая распространяется со скоростью 1,5—3,5 км/с.
В случае диффузионного горения, схема которого показана на рис., пламя как бы стоит на месте, а в него втекают с одной стороны (область а) горючие пары, а с другой стороны (область в) — воздух. Наиболее характерным примером диффузионного пламени является горящая свеча.
Схема диффузионного ламинарного горения:
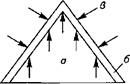
а — зона горючих паров;
б — зона горения;
в — окружающая среда (воздух).
Важнейшей особенностью процесса горения является самоускоряющийся характер химического превращения, переходящего в реакцию горения. Такой процесс возникновения горения называется самовоспламенением. Самовоспламенение может быть тепловое и цепное. При тепловом самовоспламенении причиной ускорения реакции окисления и возникновения горения является превышение скорости выделения тепла над скоростью теплоотвода, а при цепном — превышение вероятности разветвления цепей над вероятностью их обрывов.
Теории механизмов самоускоряющихся превращений при горении разработаны лауреатом Нобелевской премии академиком Н. Н. Семеновым.
При низкой температуре Т0 реакция между горючим и окислителем практически не протекает, так как отсутствуют активные молекулы. Для того чтобы они появились и началась реакция окисления, нужно горючую смесь нагреть до более высокой температуры Т1.
Возникшая при этом реакция окисления сопровождается выделением тепла, за счет чего горючая смесь нагревается. Скорость выделения тепла q1 будет пропорциональна скорости реакции окисления и теплоте сгорания смеси:
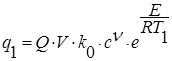
где Q — теплота сгорания горючего вещества; V — объем горючей смеси; к0 — пред экспоненциальный множитель; с — концентрация горючего в смеси; ν — суммарный порядок реакции; е — основание натурального логарифма; Е — энергия активации; R — универсальная газовая постоянная; Т1 – температура стенок сосуда.
Как только температура горючей смеси превысит температуру стенок сосуда и внешней среды Т1 и поднимется до Т2 сразу возникает теплоотвод от горючей смеси и внешней среды через стенки сосуда.
Скорость теплоотвода равна:
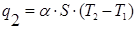
где α — коэффициент теплоотдачи от горючей смеси к стенкам сосуда; S — общая поверхность стенок сосуда; Т2 — температура горючей смеси; Т1 — температура стенок сосуда.
График зависимости скоростей тепловыделения (q1) и теплоотвода (q2) от температуры (Т) горючей смеси:
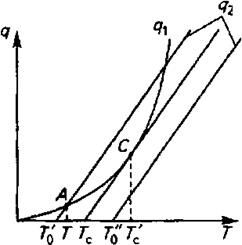
При создавшейся разности температур Т1 и Т2, нагрев горючей смеси будет зависеть от соотношения скорости тепловыделения q1 и теплоотвода q2.
1. Если q1 > q2, то горючая смесь, окисляясь саморазогревается.
2. Если q1 = q2, то горючая смесь окисляется при постоянной температуре, но горения не происходит.
Информация в лекции "2.2. Свойства гидростатического давления" поможет Вам.
Угол наклона прямой теплоотвода зависит от численного значения множителя (αS). При температуре стенки, а значит, и начальной температуре горючей смеси То’’ q1 > q2 следовательно, происходит саморазогрев горючей смеси до возникновения горения, т. е. самовоспламенение. При температуре же стенки Tо’ саморазогрев горючей смеси происходит только до температуры Т (точка А), B (точка А) q1=q2, выше этой температуры нагревание невозможно, т.к. q1<q2.
Границей между областями неограниченного и ограниченного разогрева горючей смеси является прямая теплоотвода при температуре стенки Тс. Эта прямая касается кривой тепловыделения в точке С, где существует неустойчивое тепловое равновесие. Даже незначительное повышение температуры Тс’ вызовет прогрессивный саморазогрев смеси, приводящий к самовоспламенению.
Следовательно, температурой самовоспламенения является та минимальная температура горючей смеси, при которой начинается саморазогрев, приводящий к возникновению горения.
Температура самовоспламенения горючей смеси обычно относится к горючему веществу. Она не является постоянной для одного и того же горючего вещества и зависит от его концентрации, давления, от размеров, формы и материала сосудов и других факторов. Определяется температура самовоспламенения экспериментальным путем при нормальном давлении и стехиометрической концентрации горючих газов или паров в воздухе.
При цепном самовоспламенении причиной ускорения реакции окисления является превышение скорости разветвления цепей над скоростью их обрыва.
Чисто цепное самовоспламенение — довольно редкое явление, так как оно протекает при таких низких давлениях (значительно ниже 0,1 МПа).





















