Идеальный и реальный газы
Вопрос № 1: Идеальный и реальный газы:
1. Уравнение состояния идеального газа (три формы записи)
Идеальный газ – это газ, молекулы которого рассматриваются как материальные точки, между которыми отсутствуют силы взаимодействия.
Реальный газ – газ, в котором между молекулами действуют силы притяжения и отталкивания.
Уравнение состояния:
Для фиксированной массы можно записать: 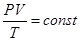
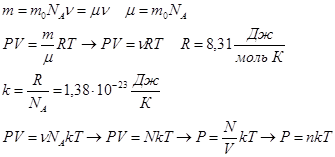
Нормальными – называются условия, при которых давление составляет 101325 Па или 105 Па, температура – 273 К. Число Авогадро = 6,02 1023 моль-
Уравнение состояния для одного моля:
Рекомендуемые материалы
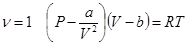
Лекция "1.3 Распределения Гиббса" также может быть Вам полезна.
Уравнение состояния для произвольной массы:
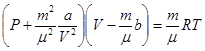
a – добавка, необходимая для учёта взаимодействия молекул реального газа.
б – добавка, учитывающая реальные объемы молекул реального газа.
Внутренняя энергия системы:
 – то есть полная энергия системы равна сумме кинетической энергии системы, как единого целого, потенциальной энергии молекулярного взаимодействия, энергии электронных оболочек и энергии взаимодействия нуклонов в ядре.
– то есть полная энергия системы равна сумме кинетической энергии системы, как единого целого, потенциальной энергии молекулярного взаимодействия, энергии электронных оболочек и энергии взаимодействия нуклонов в ядре.



















