В каком виде частицы дисперсной фазы находятся в коллоидных растворах
Итак, используя один из многочисленных методов получения дисперсных систем можно синтезировать практически любое вещество в коллоидном состоянии. Как Вы уже знаете, образующиеся при этом очень мелкие частицы обладают избытком энергии по сравнению с массивными объектами. Возникает вопрос, а в каком виде частицы дисперсной фазы находятся в коллоидных растворах?
Обладая избыточной энергией, мелкие частицы стремятся ее понизить за счет процессов адсорбции молекул или ионов из дисперсионной среды либо за счет диссоциации молекул или ионных группировок, расположенных на поверхности частиц дисперсной фазы (процесс агрегации как возможный путь понижения свободной энергии здесь учитывать не будем). В результате вокруг каждой частицы формируется ионная атмосфера. Частица с ионной атмосферой является структурной единицей коллоидного раствора и называется мицеллой. Мицеллярное строение наиболее характерно для золей, суспензий и эмульсий.
Рассмотрим образование мицеллы на примере золя AgI.
При синтезе золя по реакции AgNO3 + NaI → AgI + NaNO3 при соблюдении определенных условий синтеза (разбавленные растворы, интенсивное перемешивание) AgI формируется не в виде осадка, образованного крупными частицами, а в виде высокодисперсных (наноразмерных) частиц, которые называют агрегатами. Избыточная энергия образовавшихся частиц приводит к тому, что на них стремятся адсорбироваться молекулы воды и присутствующие в растворе ионы.
В общем случае при синтезе реагенты берутся не в строго эквивалентных соотношениях. Пусть в реакционной смеси имеется избыток AgNO3 по сравнению со стехиометрическим количеством. В результате реакции все имеющееся в системе количество иодид-ионов удаляется из раствора и переходит в нерастворимое соединение. Тогда в растворе остаются только ионы NO3-, Ag+ и Na+. Возникает вопрос, какие же именно ионы будут адсорбироваться на агрегате AgI? Теоретически, любые ионы, чей химический потенциал в растворе выше их потенциала в твердых частицах, будут стремиться адсорбироваться на поверхности агрегата. Однако логично предположить, что наиболее «охотно» будут адсорбироваться именно те ионы, которые будут образовывать наиболее прочную связь с ионами, входящими в состав агрегата. Очевидно, что такими ионами являются ионы, которые способны достраивать на поверхности частицы кристаллическую решетку нерастворимого соединения (насыщать оборванные связи на поверхности частицы). Описанная закономерность известна как правило Панета-Фаянса. В результате достраивания решетки между адсорбированными ионами и агрегатом образуются прочные химические связи со значительной долей ковалентности. В данном примере такими ионами могут быть только ионы Ag+. В общем случае, достроить решетку нерастворимого соединения способны не только ионы, входящие в состав соединения, но и другие ионы, которые близки по свойствам и размерам (изоморфны) адсорбирующимся ионам (например, ионы Mg2+ и Sr2+ изоморфны ионам Ca2+, а ионы I- и Br- изоморфны иону Cl-). Ионы NO3- и Na+, присутствующие в рассматриваемой реакционной системе наряду с ионами Ag+, способны притягиваться к агрегату лишь за счет электростатического взаимодействия (особенно слабого с учетом того, что агрегат электрически нейтрален), и, соответственно, уступают место ионам Ag+ на поверхности агрегата.
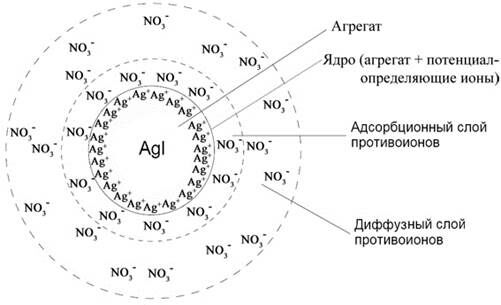
[AgI]m – агрегат
[AgI]m nAg+ – ядро
Информация в лекции "4 Схема линейной цепи однопутной РПБ ГТСС" поможет Вам.
{[AgI]m nAg+ (n-x)NO3-}x+ – коллоидная частица
{[AgI]m nAg+ (n-x)NO3-}x+ xNO3- – мицелла.
Таким образом, ионы Ag+ прочно связываются с агрегатом и, будучи заряженными, придают заряд и агрегату (равный произведению заряда иона на количество ионов). Поэтому такие ионы называются потенциалопределяющими (ПОИ); т. е. они определяют заряд ядра (ядром мицеллы называют агрегат с потенциалопределяющими ионами).
Ядро мицеллы имеет значительный заряд и притягивает из раствора противоположно заряженные ионы (противоионы). В данном случае это ионы NO3-. Противоионы в мицелле образуют два слоя, которые различаются по силе их притяжения к ядру – относительно плотный адсорбционный слой противоионов (в котором реализуется достаточно сильное электростатическое взаимодействие противоионов с зарядом ядра) и более удаленный от ядра диффузный слой («размытый») (в котором противоионы притягиваются к ядру намного меньше вследствие ослабления (экранирования) заряда ядра противоионами адсорбционного слоя). Противоионы адсорбционного слоя вместе с ядром образуют единую структуру относительно постоянного состава – коллоидную частицу.
Важно отметить, что в результате теплового движения или под действием электрического поля ионная структура коллоидной частицы не изменяется, т. е. ядро и противоионы адсорбционного слоя (коллоидная частица) движутся вместе. Коллоидная частица имеет заряд, меньший, чем заряд ядра, т. к. заряд ядра частично компенсирован зарядом противоионов. Заряд коллоидной частицы имеет большое значение для протекания многих процессов с участием дисперсных систем и, в частности, является фактором их агрегативной устойчивости, т. к. одноименно заряженные частицы отталкиваются за счет электростатического взаимодействия, что препятствует их агрегации. Совокупность противоионов диффузного («размытого») слоя компенсируют заряд коллоидной частицы и вместе они образуют электрически нейтральную мицеллу.
Мицеллы являются структурными единицами дисперсной фазы золей, которые часто называют коллоидными растворами. Это исторически сложившееся название. Необходимо помнить различие между истинными (молекулярными, ионными) и коллоидными растворами.



















