Законы Фарадея
Законы Фарадея
Законы Фарадея являются количественными законами электролиза.
Первый закон Фарадея:
Масса вещества, выделяющегося на электродах, прямо пропорциональна количеству прошедшего через раствор электричества
 .
.
Второй закон Фарадея:
При прохождении через расплав или раствор электролита 96500 Кл электричества на электродах выделяется 1 моль эквивалента вещества.
 - электрохимический эквивалент вещества.
- электрохимический эквивалент вещества.
 - объединённый закон Фарадея.
- объединённый закон Фарадея.
Рекомендуемые материалы
Поляризация при электролизе
Поляризация при электролизе складывается из собственно поляризации, которая делится на химическую и концентрационную, и перенапряжения.
Химическая поляризация
Химическая поляризация возникает при использовании инертных электродов.
 .
.
 .
.
Какими бы ни были инертные электроды (Pt, С, керамика), все они прекрасно адсорбируют газы.
 .
.
Платина - анод насыщается хлором; платина - катод поглощает водород.
Хлор может только восстанавливаться, водород - окисляться:
 .
.
В электролизере образуется гальванический элемент:
 .
.
Электродвижущая сила возникшего гальванического элемента направлена против внешнего напряжения и ослабляет его.
Данный вид поляризации называется химическим по той причине, что электроды как бы меняют свою химическую природу.
Поляризация играет отрицательную роль, так как она приводит к перерасходу электроэнергии.
С химической поляризацией борются химическим путем. В раствор добавляют вещества, которые очищают электроды от поглощённых газов.
Концентрационная поляризация
Данная поляризация происходит при активном аноде, например, серебряном
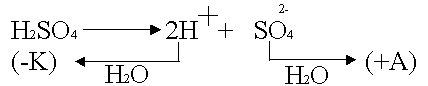
 .
.
В силу диффузии ионы серебра от анода стремятся к катоду, где они начнут восстанавливаться как более сильные окислители.
Поскольку диффузия в жидкостях медленная, концентрация ионов Ag в анодном пространстве намного выше, чем в катодном.
Вследствие этого в электролизере возникает концентрационный гальванический элемент.
ЭДС возникшего концентрационного элемента также направлена против внешнего напряжения и ослабляет его.
С концентрационной поляризацией бороться гораздо проще, чем с химической. Ее устраняют перемешиванием раствора.
Перенапряжение электрода
Перенапряжением электрода называют разность между фактическим и теоретическим электродными потенциалами.
Перенапряжение металлов настолько мало, что им пренебрегают. Велико перенапряжение водорода и кислорода.
Перенапряжение водорода велико при следующих условиях:
· малых плотностях тока,
· низких температурах раствора.
Обратите внимание на лекцию "2 Общеинфекционный синдром".
Перенапряжение также зависит от материала катода.
Перенапряжение водорода наиболее велико на тех металлах, которые в ряду напряжений располагаются вблизи водорода.
Перенапряжение водорода может играть как отрицательную, так и положительную роль.
Отрицательную роль оно играет при необходимости получить водород электролитическим путем.
Положительна роль перенапряжения при необходимости получить с помощью электролиза какой - либо металл, находящийся в ряду напряжений до водорода.
Можно создать условия (плотность тока, температура раствора, материал катода, посторонние ионы в растворе), при которых вследствие высокого перенапряжения водорода из раствора можно восстановить металлы, стоящие в ряду напряжения до водорода, (вплоть до алюминия).



















