Устойчивость и коагуляция коллоидных систем
Лекция 5. Устойчивость и коагуляция коллоидных систем
Понятие об устойчивости дисперсных систем.
Виды устойчивости ДС.
Коагуляция.
Действие электролитов на коагуляцию.
Совместное действие электролитов при коагуляции.
Теория устойчивости ДЛФО.
Скорость коагуляции.
Старение золей. Коллоидная защита.
Рекомендуемые материалы
Вопросы устойчивости дисперсных систем занимают центральное место в коллоидной химии, поскольку эти системы в основном термодинамически неустойчивы.
Под устойчивостью системы понимают постоянство во времени ее состояния и основных свойств: дисперсность равномерного распределения частиц дисперсной фазы в объеме дисперсионной среды и характера взаимодействия между частицами.
Частицы дисперсной системы, с одной стороны, испытывают действие земного притяжения; с другой стороны, они подвержены диффузии, стремящейся выровнять концентрацию во всех точках системы. Когда между этими двумя силами наступает равновесие, частицы дисперсной фазы определенным образом располагаются относительно поверхности Земли.
По предложению Н.П. Пескова (1920г) устойчивость дисперсных систем подразделяют на два вида:
- кинетическая (седиментационная) устойчивость – свойство дисперсных частиц удерживаться во взвешенном состоянии, не оседая (противостояние частиц силам тяжести).
(условия устойчивости – высокая дисперсность частиц, участие частиц дисперсной фазы в броуновском движении);
- агрегативная устойчивость – способность частиц дисперсной фазы оказывать сопротивление слипанию (агрегации) и тем самым сохранять определенную степень дисперсности этой фазы в целом.
Дисперсные системы по устойчивости делят на два класса:
- термодинамически устойчивые (лиофильные коллоиды);
- термодинамически неустойчивые (лиофобные системы).
Первые самопроизвольно диспергируются и существуют без стабилизатора. К ним относятся растворы ПАВ, растворы ВМС.
Свободная энергия Гиббса термодинамически устойчивой системы уменьшается (DG<0).
К термодинамически неустойчивым системам относятся золи, суспензии, эмульсии (DG>0).
В последнее время различают также конденсационную устойчивость: система образует непрочные агрегаты (флокулы) или рыхлые осадки – частицы теряют свою индивидуальную подвижность, но сохраняются как таковые в течение длительного времени.
Коагуляция
Лиофобные коллоиды являются термодинамически неустойчивыми системами, существующими благодаря стабилизации за счет возникновения защитных ионных или молекулярных слоев. Следовательно, изменение состояния этих слоев может привести к потере устойчивости и затем к выделению дисперсной фазы.
Коагуляция - процесс слипания (слияния) коллоидных частиц с образованием более крупных агрегатов с последующей потерей кинетической устойчивости.
В общем смысле под коагуляцией понимают потерю агрегативной устойчивости дисперсной системы.
Скрытая стадия коагуляции – очень быстрая – размер частиц увеличивается, но осадок не выпадает – изменение окраски, помутнение.
Явная стадия – выпадение осадка, выделение двух фаз в растворе. Осадок называется коагулят.
Конечным итогом коагуляции могут быть два результата: разделение фаз и образование объемной структуры, в которой равномерно распределена дисперсионная среда (концентрирование системы). В соответствии с двумя разными результатами коагуляции различают и методы их исследования (для первого результата – оптические, например, для второго – реологические).
Основные процессы, которые могут происходить в дисперсных системах, показаны на рис. 5.1.
Из схемы видно, что понятие коагуляция включает в себя несколько процессов (флокуляция, коалесценция, агрегация, структурообразование), идущих с уменьшением удельной поверхности системы.
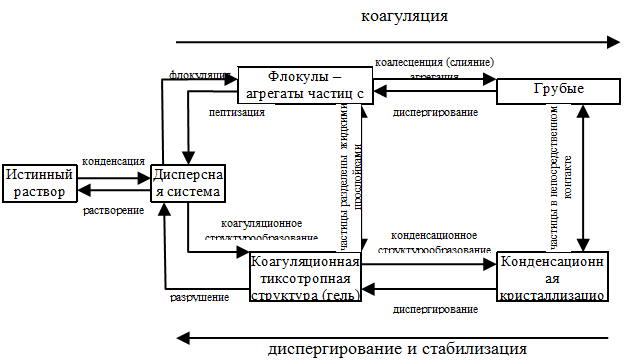
Рис. 5.1. Процессы, происходящие в дисперсных
системах.
Коагуляция может быть вызвана разными факторами:
- введением электролитов;
- нагреванием или замораживанием дисперсной системы;
- механическим воздействием;
- высокочастотными колебаниями;
- ультрацентрифугированием и др. факторами.
Наиболее важным и изученным является действие электролитов.
Действие электролитов на коагуляцию
Установлен ряд эмпирических закономерностей воздействия электролитов, которые известны под названием правил коагуляции:
1. Любые электролиты могут вызвать коагуляцию, однако заметное воздействие они оказывают при достижении определенной концентрации.
Порог коагуляции – минимальная концентрация электролита, вызывающая коагуляцию (g, моль/л; иногда Ск ).
Порог коагуляции определяют по помутнению, изменению окраски или по началу выделения дисперсной фазы в осадок.
2. Правило Шульце-Гарди (правило значности, эмпирическое):
Коагулирующим действием обладает тот ион электролита, который имеет заряд, противоположный заряду потенциалопределяющих ионов мицеллы (гранулы), причем, коагулирующее действие тем сильнее, чем выше заряд.
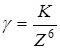
где К – коагулирующая способность (примем ее за единицу).
По правилу Шульца – Гарди значение порогов коагуляции для противоионов с зарядами 1, 2 и 3 соотносятся как 1:1/20:1/500, т.е. чем выше заряд, тем меньше требуется электролита, чтобы вызвать коагуляцию.
Например, коагулируем золь сульфида мышьяка (As2S3): или Fe(OH)2
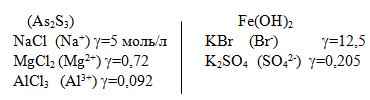
Правило Шульце – Гарди имеет приближенный характер и описывает действие ионов лишь неорганических соединений.
3. В ряду органических ионов коагулирующее действие возрастает с повышением адсорбционной способности.
4. В ряду неорганических ионов одинаковой зарядности их коагулирующая активность возрастает с уменьшением гидратации.
Лиотропные ряды или ряды Гофмейстера – это порядок расположения ионов по их способности гидратироваться (связывать воду).
Слово ''лиотропный'' значит ''стремящийся к жидкости'' (более подходящий термин для случая водных сред – гидротропный).

5. Очень часто началу коагуляции соответствует снижение дзета-потенциала до критического значения (около 0,03 В).
6. В осадках, получаемых при коагуляции электролитами, всегда присутствуют ионы, вызывающие ее.
Совместное действие электролитов
при коагуляции
Смеси электролитов при коагуляции золей редко действует независимо. Наблюдаемые при этом явления можно свести к трем следующим: аддитивность, антагонизм и синергизм электролитов. Указанные явления при использовании смесей электролитов приведены на рис.5.2.
Зависимость 1 – характеризует аддитивное действие электролитов. Коагулирующее действие в смеси определяют по правилу простого сложения:
KCl+KNO3; NaCl+KCl
Кривая 2 – антагонизм электролитов – содержание каждого электролита в смеси превышает его собственную пороговую концентрацию
Al(NO3)3+K2SO4; Ti(NO3)4+Na2SO4
Синергизм действия электролитов демонстрирует кривая 3. Усиливается действие каждого из электролитов – для коагуляции их требуется меньше в смеси, чем каждого по отдельности.
LiCl+CaCl2 действуют на гидрозоль H2S
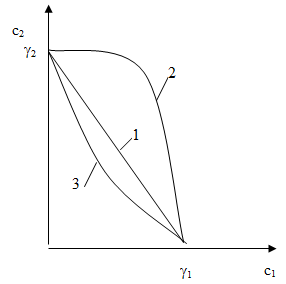
Рис. 5.2. Совместное действие электролитов при
коагуляции.
Теория устойчивости гидрофобных дисперсных систем ДЛФО
Современная физическая теория коагуляции электролитами основана на общих принципах статистической физики, теории молекулярных сил и теории растворов. Ее авторами являются: Б.В. Дерягин, Л.Д. Ландау (1937-1941), Э. Фервей, Я. Овербек (по первым буквам ДЛФО).
Суть теории: между любыми частицами при их сближении возникает расклинивающее давление разделяющей жидкой прослойки в результате действия сил притяжения и отталкивания. Расклинивающее давление является суммарным параметром, учитывающим действие как сил притяжения, так и сил отталкивания.
Состояние системы зависит от баланса энергии притяжения (Uпр) и энергии отталкивания (Uотт). Преобладает Uотт – устойчивая система. Преобладает Uпр - нарушение агрегативной устойчивости – коагуляция.
Изменение энергии взаимодействия между двумя частицами при их сближении изображают графически (рис. 5.3).
Суммарную энергию системы из двух частиц (кривая 3) получают сложением Uотт и Uпр:
U=Uотт+Uпр =
где: В – множитель, зависящий от значений электрических потенциалов ДЭС, свойств среды, температуры;
е – основание натурального логарифма;
c – величина, обратная толщине диффузного слоя;
h – расстояние между частицами;
А – константа молекулярных сил притяжения.
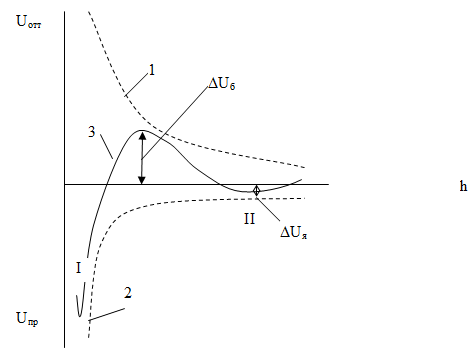
Рис.5.3. Потенциальные кривые взаимодействия
коллоидных частиц:
1 – изменение энергии отталкивания с расстоянием;
2 – изменение энергии притяжения;
3 – результирующая кривая.
Рассмотрим результирующую кривую 3 на рис.5.3. На ней имеются характерные участки:
- В области малых расстояний имеется глубокий первичный минимум (потенциальная яма) – значительно преобладает Uпр. Первичный минимум отвечает непосредственному слипанию частиц (I).
- В области больших расстояний - вторичный неглубокий минимум (вторая потенциальная яма, отвечает притяжению через прослойку среды). На схеме II.
- В области средних расстояний на кривой имеется максимум и, если он расположен над осью абсцисс, то появляется энергетический барьер сил отталкивания (DUб).
Результирующая кривая 3 может иметь различный вид в зависимости от устойчивости дисперсной системы (рис.5.4.).
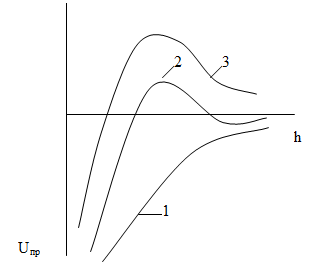
Рис. 5.4. Потенциальные кривые для определенных
состояний устойчивости дисперсной системы:
1 - в системе при любом расстоянии между частицами преобладает энергия притяжения над энергией отталкивания. В такой системе наблюдается быстрая коагуляция с образованием агрегатов.
2 - достаточно высокий потенциальный барьер и наличие вторичного минимума. Частицы взаимодействуют, но не имеют непосредственного контакта и разделены прослойками среды.
3 - система с высокой агрегатной устойчивостью (высокий потенциальный барьер и отсутствие вторичного минимума или при его глубине, меньшей тепловой энергии kТ).
В зависимости от высоты энергетического барьера и глубины потенциальных ям возможны различные варианты поведения частиц при сближении (рис.5.5), частицы обладают кинетической энергией – kТ.
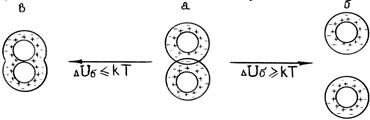
Рис.5.5. Схемы взаимодействия коллоидных частиц
| Состояние в: Малая высота барьера и неглубокий вторичный минимум: DUб@DUя£kT частицы вступают в ближнее взаимодействие, т.е. непосредственно соприкасаются – наступает коагуляция | Состояние а: Характеризуется тем, что перекрываются диффузные слои и сохранены прослойки среды между частицами (гели). Энергетический барьер довольно высок [DUб=(5-10)kT] вторичный минимум неглубок: DUя³kT Взаимодействующие частицы не могут разойтись (удерживают силы притяжения) и не могут приблизиться вплотную (препятствуют силы отталкивания). Добавление электролита чаще всего приводит к коагуляции (уменьшается h). | Состояние б: Высокий энергетический барьер DUб³kT и отсутствие или неглубокий вторичный минимум DUя£kT: Частицы не могут преодолеть барьер и расходятся без взаимодействия. Такая система агрегативно устойчива. |
Дисперсная система агрегативно устойчива при высоком энергетическом барьере сил отталкивания.
Скорость коагуляции
Ход коагуляции в зависимости от концентрации коагулирующего электролита можно подразделить на две стадии: медленную и быструю.
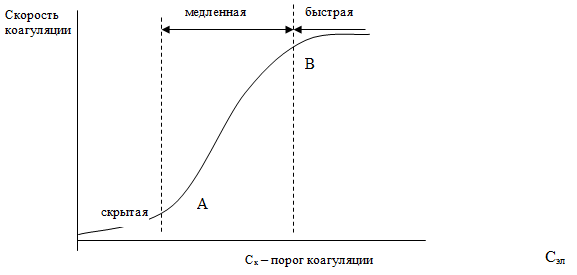
Рис.5.6. Зависимость скорости коагуляции от
концентрации электролита
В области медленной коагуляции скорость сильно зависит от концентрации (отрезок АВ). В точке В скорость становиться постоянной и не зависит от концентрации электролита – здесь значение z - потенциала равно нулю – начало быстрой коагуляции. Концентрацию электролита, начиная с которой скорость коагуляции остается постоянной, называют порогом быстрой коагуляции.
Теории кинетики коагуляции разработаны Смолуховским (1916г).
Рассматривают коагуляцию как реакцию второго порядка, в элементарном акте которой участвуют две частицы:  .
.
Уравнение Смолуховского для расчета числа частиц, слипшихся по m-штук за время t:
 ;
;
 - первоначальное число частиц;
- первоначальное число частиц;
 - время половинной коагуляции (
- время половинной коагуляции ( ).
).
При быстрой коагуляции все столкнувшиеся частицы реагируют (DUб=0).
Уравнение Смолуховского для константы скорости быстрой коагуляции:
 ;
;
где h- вязкость среды.
При медленной коагуляции не все столкновения приводят к слипанию. Уравнение Смолуховского для медленной коагуляции:
 ;
;
где Р – стерический множитель, учитывающий благоприятные пространственные расположения частиц при столкновении, их физические размеры. При быстрой коагуляции все столкновения эффективны и Р=1, при медленной Р<1.
DЕ – потенциальный барьер, при быстрой коагуляции DЕ=0, при медленной DЕ¹0.
h - вязкость.
Порог коагуляции можно вычислить из соотношения, теоретически найденного Дерягиным и Ландау и названным законом 6-й степени:
энергетический барьер между коллоидными частицами исчезает при достижении критической концентрации (g), которая обратно пропорциональна шестой степени заряда иона-коагулятора:
 ;
;
С – константа, зависящая от числа зарядов катиона и аниона;
e - диэлектрическая проницаемость раствора;
А – константа Ван –дер –Ваальсового притяжения;
е- заряд электрона;
k – константа Больцмана;
z– зарядность коагулирующего иона.
В соответствии с этим уравнением значения g для элементов с зарядами противоионов 1, 2 и 3 соотносятся как 1:1/26:1/36=1:1/64:1/729.
Уравнение хорошо обосновывает эмпирическое правило Шульце-Гарди.
В тех случаях, когда велика роль адсорбционно-сольватного фактора устойчивости, проявляется приближенность теории ДЛФО, т.к. она не учитывает роли специфической адсорбции и сродства иона к растворителю.
Связь эффективности соударений с потенциальным барьером при коагуляции была показана Фуксом Н.А.
Если DЕ значительно больше кТ, то скорость коагуляции может приблизиться к нулю и система окажется агрегативно неустойчивой.
В теории, развитой Фуксом, используется представление о коэффициенте замедления коагуляции W, который показывает, во сколько раз константа скорости медленной коагуляции меньше константы скорости быстрой коагуляции. Учитывая выражения для Кб и Км, получим:
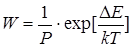
Коэффициент W называют фактором устойчивости или коэффициентом стабильности.
Старение золей
Лиофобные коллоиды обладают слабым взаимодействием дисперсной фазы и дисперсионной среды и характеризуются склонностью к уменьшению дисперсности со временем.
Избыток свободной поверхностной энергии, полученной частицами при их образовании, является (согласно второму началу термодинамики) основной причиной перехода в более устойчивое состояние, которое определяется укрупнением частиц.
Самопроизвольный процесс укрупнения частиц (уменьшения степени дисперсности) в лиофобных золях, называется старением или автокоагуляцией.
Скорость старения гораздо медленнее, чем коагуляция под воздействием электролитов.
Защитное действие молекулярных
адсорбирующих слоев
Некоторые системы обладают очень высокой устойчивостью, они даже приобретают способность к самопроизвольному образованию – коллоидную растворимость.
В большинстве же золей на границе раздела двух фаз существуют адсорбционные слои, образованные молекулами ПАВ. Адсорбционные слои предохраняют частицы от слипания, но они покрывают не всю поверхность, а приблизительно 40…60% ее.
Максимальная устойчивость достигается при образовании полного адсорбционного слоя.
Рекомендуем посмотреть лекцию "Литература и содержание".
Повышение устойчивости дисперсных систем под влиянием ПАВ называют коллоидной защитой или стабилизацией коллоидов.
В качестве стабилизаторов используют: высокомолекулярные ПАВ, желатин, альбумин, казеин, крахмал, пектин, каучуки, гемоглобин и др.
Для количественной оценки стабилизирующего действия того или иного коллоида Р.Зигмонди предложил так называемое золотое число.
Золотое число – это минимальная масса (в мг) стабилизирующего вещества, которая способна защитить 10 мл красного золя золота (воспрепятствовать изменению цвета красный-голубой) от коагулирующего воздействия 1 мл 10%-ного раствора NaCl.
Чем меньше золотое число, тем больше защитное действие коллоида.
Определено также защитное действие в отношении золей серебра – серебряное число, конго рубинового – рубиновое число, серы – серное число и т.д.



















