Лекции: Противогельминтный иммунитет.
Описание
Противогельминтный иммунитет
Иммунная защита от простейших
Антипротозойную защиту можно рассмотреть на примере малярии — наиболее распространенного и одного из самых тяжелых протозойных инфекционных заболеваний. Своеобразие иммунитета при малярии обусловлено особенностями жизненного цикла плазмодиев, сменой экспрессируемых ими антигенов и изменением их локализации. Спорозоиты, проникающие в организм с укусом комара, вызывают раннюю реакцию клеток врожденного иммунитета. Реакция обычно недостаточно эффективна, чтобы элиминировать плазмодии. Взаимодействуя с поверхностными молекулами клеток (CD36, ICAM-1, гиалуронатом, хондроитинсульфатом), в том числе эритроцитов, плазмодии проникают в них и размножаются.
Спорозоиты экспрессируют один из примерно 60 возможных ≪вариантных антигенов≫ — VSA (Variant surface antigen), против которого с участием дендритных клеток и CD4+ Т-лимфоцитов развивается В-клеточный иммунный ответ. Образующиеся при этом антитела обеспечивают частичный лизис плазмодиев, что приводит к ремиссии заболевания. Однако после этого взамен прежнего экспрессируется другой VSA, с которым накопленные антитела не взаимодействуют. Происходит новая волна размножения плазмодия с соответствующей клинической картиной и индукцией новых антител, обеспечивающих очередную ремиссию. На стадии мерозоита плазмодий экспрессирует новые антигены, из которых наиболее известен MSP-1. Они вызывают развитие (преимущественно в селезенке) иммунного ответа, как гуморального, так и клеточного типа. Гуморальный иммунный ответ развертывается преимущественно в лимфоидных фолликулах селезенки. Т-клеточный ответ формируется в двух основных формах — воспалительной и цитотоксической. Воспалительный иммунный ответ реализуется с участием CD4+ Т-лимфоцитов и макрофагов в маргинальной зоне и красной пульпе селезенки. Он сопровождается значительной выработкой цитокинов и вносит наиболее существенный вклад в ограничение инфекции на стадии мерозоитов. Цитотоксический иммунный ответ, опосредованный CD8+ Т-киллерами, развивается в печени и сопровождается значительным повреждением гепатоцитов. Тем не менее элиминировать возбудитель иммунная система не в состоянии. Плазмодий на стадии гаметоцита поступает в кровь, а из нее — в организм промежуточного носителя (комара).
Таким образом, при ответе на плазмодий мобилизуются все основные формы иммунной защиты, однако это не приводит к элиминации патогена.
Это обусловлено главным образом антигенной изменчивостью и сменой стадий развития паразита, характеризующихся различной локализацией и экспрессируемыми антигенами.
Иммунная защита против гельминтов
Существует два типа локализации гельминтов — в кишечнике, куда они поступают с пищей, и в различных других органах (печени, легких, головном мозгу, стенке сосудов и т.д.), куда они проникают гематогенным путем. Паразиты, локализующиеся в органах, часто окружены гликолипидной или гликопротеиновой оболочкой, формируемой клетками хозяина и защищающей гельминт от действия факторов иммунной системы. В кишечнике роль фактора изоляции играет сама слизистая оболочка.
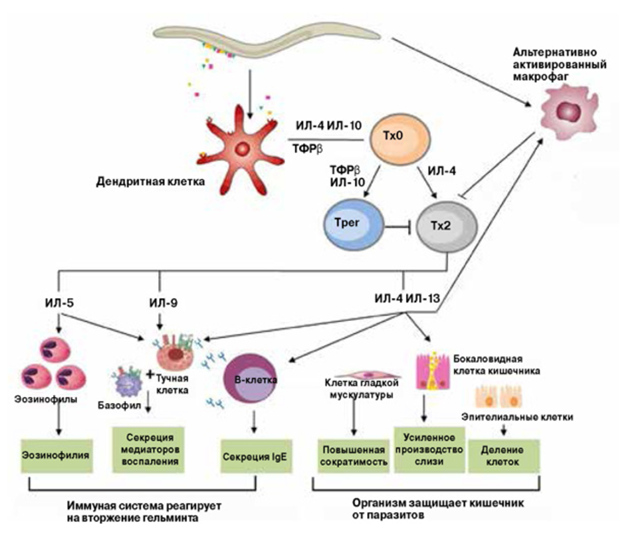
Клетки врожденного иммунитета распознают различные компоненты гельминтов (PAMP) — лизофосфатидилсерин (распознается TLR-2), липопротеины, обогащенные фосфорилхолином (распознаются TLR-4) и др.; гликаны, распознаваемые лектиновыми рецепторами, в частности DC-SIGN; протеазы, секретируемые гельминтами; хитин. В качестве распознающих клеток выступают макрофаги, дендритные клетки, энтероциты слизистой оболочки кишечника. Активация дендритных клеток приводит к развитию незрелых клеток DC2-типа, способствующих дифференцировке Т-хелперов типа Th2. Th2-ответ — преобладающая форма протективного иммунного ответа против гельминтов. Среди цитокинов, секретируемых Th2-клетками при гельмитозах, наиболее важную роль играет IL-4 (обеспечивает переключение изотипов антител на IgE), IL-13 (привлекает эозинофилы и базофилы, обеспечивает морфогенетические перестройки — ремоделирование) и IL-5 (привлекает эозинофилы). Важная защитная роль при гельминтозах принадлежит антителам класса IgE. Взаимодействуя с сенсибилизированными тучными клетками, они стимулируют выброс факторов с антигельминтной активностью и секретируют цитокины, привлекающие базофильные и эозинофильные гранулоциты. Эозинофилы и базофилы формируют вал вокруг гельминтов и выделяют молекулы и вещества, оказывающие антигельминтное действие. Наибольшую роль среди них играют белки эозинофилов — MBP (главный щелочной белок) и ECP (эозинофильный катионный белок), способные вызвать гибель гельминта. Гибель гельминтов в кишечнике сопровождается их эвакуацией из пищеварительного тракта. Гельминты, погибшие в органах, элиминируются клетками мононуклеарной фагоцитирующей системы.
Против гельминтов формируется относительно слабая и кратковременная иммунологическая память, обычно не гарантирующая развития повторных инвазий.
 СГМУ
СГМУ Spes
Spes


















