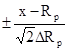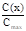Практические занятия
Практическое занятие N1
Определение профилей распределения примесей при термической диффузии
В настоящее время при формировании легированных областей в объеме твердого тела широко используются метод термической диффузии примесей и метод ионной имплантации (внедрения) примесей.
Исторически метод термической диффузии примесей на ранних этапах развития микроэлектроники являлся единственным для модифицирования приповерхностных свойств (типа проводимости, электропроводности, рекомбинационных свойств и др.) твердого тела. В дальнейшем появился более прогрессивный прецизионный метод легирования - ионная имплантация.
Однако термическая диффузия при производстве изделий ЭОТ используется как метод разгонки примесей после ионной имплантации.
При рассмотрении диффузионных процессов следует выделить два класса задач: первый - построение профилей распределения примесей и второй - определение геометрических размеров легированных областей (глубин залегания) при заданных технологических режимах процесса диффузии.
Рассмотрим первый из них.
В полупроводниковой технологии интерес представляют два случая распределения примесных атомов.
Рекомендуемые материалы
1. Диффузия из источника с ограниченным содержанием примеси (ограниченный источник). Примесь в начальный момент находится в бесконечно тонком поверхностном слое. Тогда профиль распределения концентрации имеет вид нормального распределения
 (1.1)
(1.1)
где N - плотность атомов примеси под единицей площади поверхности, неизменная в любой момент диффузии, ат/см2;
х - глубина, соответствующая данной концентрации, см;
D - коэффициент диффузии примеси, см2/с;
t - время диффузии, с.
Глубина залегания р-n -перехода:
 (1.2)
(1.2)
где Со - поверхностная концентрация примеси - ат/см3;
СВ - концентрация примеси в исходной пластине - ат/см3.
В нашем случае, когда х = 0 из (1) следует, что
 (1.3)
(1.3)
Для практических случаев можно пользоваться приближенной формулой

 (1.4)
(1.4)
2.Диффузия из источника с постоянной поверхностной концентрацией примеси (бесконечный источник)

 (1.5)
(1.5)
Где  - табулированная функция ошибок
- табулированная функция ошибок
Со= const и определяется предельной растворимостью примеси при температуре диффузии;
функция erfc - табулирована, но можно использовать ее аппроксимацию
 (1.6)
(1.6)
Для этого случая глубина залегания р-n- перехода
 (1.7)
(1.7)
При последовательной диффузии нескольких примесей выражении для C(x,i) нужно использовать еумму
 (1.8)
(1.8)
Расчет распределения примеси в случае двухстадийной диффузии
Стадия загонки протекает в течение короткого времени t| up постоянной поверхностной концентрации Со,.
Введенное при загонке количество примесных атомов (N, ат/см2 сдужит источником диффузанта при разгонке в течение времени t изменяющейся во времени поверхностной концентрацией С02:
 (1.9)
(1.9)
Для построения профиля распределения примеси при двухстадийной диффузии необходимо знать температуры и время загонки и разгонки. Температура загонки Ti - определяет коэффициент диффузии D| и поверхностную концентрацию Q>i, определяемую предельной растворимостью примеси.
Поверхностная плотность атомов примеси, введенной при загонке, определяется выражением
 (1.10)
(1.10)
Распределение примеси после разгонки определяется выражением
 (1.11)
(1.11)
Пример 1. Построить профиль распределения примеси и определить глубину залегания p-n-перехода в случае двухстадийной диффузии Р в Si р-типа с удельным сопротивлением 10 Ом-см, проводимой в режиме:
T1 = 1050°C; t1 = 10 мин;
Т1=1150°С; t2 = 2 ч.
Решение:
1. Так как на стадии загонки поверхностная концентрация COi постоянна и определяется ггредельной растворимостью примеси при данной температуре, ее можно определить из графика зависимости С =f(Т)(рис.1.3.)Ш,
Находим, что для 1050 °С предельная растворимость Р в Si составляет 1.2 • 102' см"3, т.е.
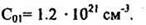
2. Необходимо определить Di при Т = 1050 °С. Из. графика D=f(T) (рис. 1.4.) находим, что
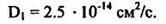
3. Определим количество атомов Р или поверхностную плотность атомов примеси, введенную при загонке, из выражения
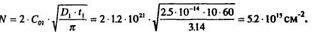
4. Стадия разгонки. Находим D2 из той же зависимости D = f(T); для температуры разгонки 1150 °С получаем
D2 = 4 • 10-13 cm2/c.
5. Можем определить распределение примеси после разгонки из выражения:
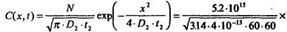
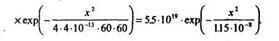
Для сравнения можем построить кривую распределения Р после загонки, пользуясь выражением
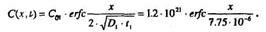
Если построить эти профили, то получим зависимости, изображенные на рис 1.1, и следующие данные
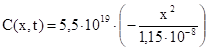
x1=1мкм= 1•10-4см; Сх1 = 2.31•10-19;
х3=2 мкм = 2•10-4см; Сх2 = 1.69•10-19;
хэ=3 мкм = 3•10-4 см; Сх3 = 2,19•10-19;
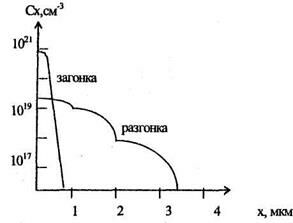
Рис. 1.1. Профили распределения фосфора в Si после двухстадийной диффузии.
6. Определим глубину залегания p-n-перехода после проведения разгонки по формулам


СВ - концентрация примеси в исходной пластине. Ее можно найти из графика р = f(C) (рис. 1.5). Для рр = 1 0 Ом • см получаем
С= 1.2 • 10-15 см3.
Поставляем найденные значения в выражение для xj:

По упрощенной формуле имеем
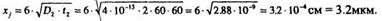
Расчет распределения примеси при диффузии из слоя конечной толщины
В предыдущем случае выполнялось условие v D,t,<D2t2 (1.5- 10"<2.88- 109),
т.е. форма профиля на стадии загонки не влияет на профиль после разгонки, т.к. их глубины залегания несопоставимны. Если условие D1t1 < D2t2 не выполняется, то глубины диффузии при загонке и разгонке сопоставимы и нельзя считать, что диффузия при разгонке идет из бесконечно тонкого слоя с ограниченным содержанием примеси. В этом случае получается комбинированное распределение, определяемое решением уравнения Фика для диффузии из слоя конечной толщины

у - переменная интегрирования; а и z -табличные параметры

Поверхностная концентрация после разгонки С02 = С (x=0,t1,t2). Или

Интеграл в выражении (12) вычислен и табулирован для различных α и z.
Пример 2: Рассчитать распределение примени для двухстадийной диффузии Р в Si в режиме:
Т1 = 1250°С; t1 = 10мин;
Т2=1150°С; t2 = 2ч.
Определить глубину залегания p-n-перехода. Решение:
1. Из графика D = f(T) (см.рис.1.4) определим коэффициент диффузии Р при данных температурах:
D1 = 4 • 10-12 см2/с;
D2 = 4 • 10-13 см2/с.
2. Сравним D1t1 и D2t2:
D1t1, = 4 • 10-12 •10 • 60 = 2.4 • 10-19;
D2t2 = 4 • 10-13 • 2 • 60 • 60 = 2.88 • 10-19, т.к. они близки, необходимо использовать формулу (12).
3. Определим постоянные а и г по формулам (13)
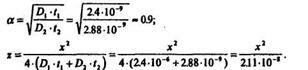
4. Определим поверхностную концентрацию после разгонки по кривой С = f(Т) (см.рис.1.3) (соответствует предельной растворимости Р при данной температуре) при Т1 = 1250 °С
С01 = 1.2 • 1021 см-3.
5. Определим поверхностную концентрацию после разгонки С02:

б. Можем построить распределение концентрации по глубине, используя таблицу расчетных значений а и г.
Задавая значения г = 0.1 - 0.3 - 0.5 и т.д. для α = 0/9, определяем значение интеграла в формуле (12).
Из графика можем найти глубину х:
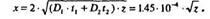
7. На стадии загонки распределение примеси имеет вид (5)
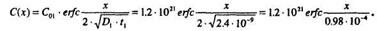
Если построить распределение концентрации Р, после загонки и разгонки получим следующие зависимости (рис. 1.2)
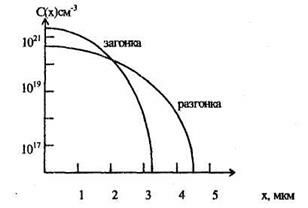
Рис. 1.2. Профили распределения Р в Si в примере 2.
Пример 3. Переход эмиттер-база формируется диффузией фосфора в подложку p-типа в течение t = 1 ч при Т = 1000 °С; концентрация атомов Р на поверхности Si поддерживается на пределе растворимости в твердом состоянии. Предполагая, что концентрация примеси в базе равна концентрации примеси p-типа в исходном материале (или 10|7 см-3), найти глубину перехода эмиттер-база.
Решение.
I вариант
Имеем диффузию из неограниченного источника, т.е. используем формулу (5)
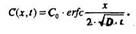
Зная температуру диффузии Т = 1000 °С, находим Со и D из графиков С = f(T) и D=f(T) D = 3 • 10-14 см-3 (рис 1.3-1.4):
C0 = 1021 см-3;
D = 3 • 10-14 см-3;
Тогда
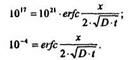
Из графика функции erfc (рис. 1.6) находим для значения 10"*
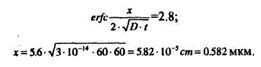
II вариант
Используем формулу (4):
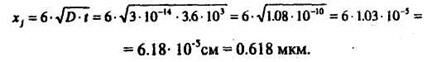
Или по уточненной формуле (7)
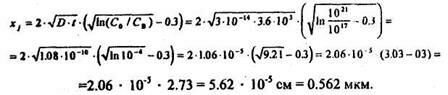
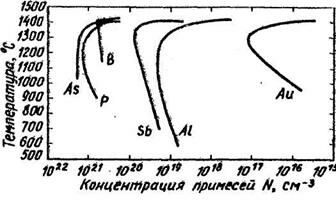
Рис.1.3. Зависимость предельной растворимости примесных элементов в Si oт температуры.
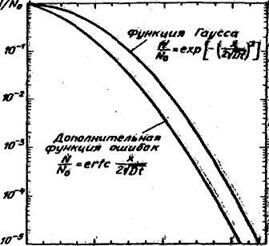
Рис. 1.4. Графики для функции erfc и нормального закона распределения.
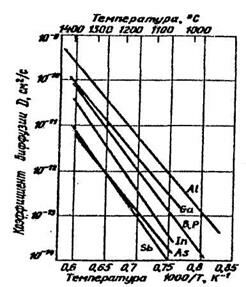
Рис. 1.5. Зависимость коэффициента диффузии примесей в Si от температуры.
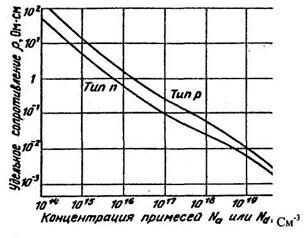
Рис. 1.6. Зависимость удельного сопротивления Si от концентрации примеси.
Практическое занятие N2.
Определение технологических режимов процесса диффузии.
Второй класс задач связан с расчетом технологических режимов первой и второй стадии диффузии или второй стадии диффузии ("разгонка") после ионной имплантации. Последняя наиболее актуальна при изготовлении современных изделий ЭОТ последних поколений.
На первом занятии рассматривались так называемые прямые задачи, т.е. определение параметров диффузионного слоя при заданных режимах диффузии (распределение примеси (профиль диффузии) C(x,t) и глубины залегания p-n-перехода (xj). Рассмотрим так называемые обратные задачи, т.е. определение режимов диффузии при заданных параметрах диффузионного слоя.
Эти задачи имеют большое практическое значение, но эта связь с практикой придает им специфику - они неоднозначны в отношении выбора длительности и температуры процесса. Выбор этих параметров определяют конкретные особенности технологического процесса и возможности технологического оборудования.
Строгое решение обратных задач приводит к определению произведения D•t. Далее чаще всего задаются температурой Т и по найденному значению D определяют длительность процесса t. Иногда при выборе режимов следует учитывать не только температурную зависимость коэффициента диффузии, но и предельную растворимость примеси.
1. Определение режимов диффузии на основании заданных параметров распределения примеси. 1.1. Одностадийная диффузия.
Для расчета стадии разгонки или одностадийной диффузии обратная задача достаточно проста.
Если диффузия ведется из источника с ограниченным содержанием примеси (конечный источник), тогда из формулы для xj
 (2.1)
(2.1)
получим
 (2.2)
(2.2)
Теперь нужно выбрать либо температуру, либо время процесса. Если нас лимитирует производительность, задаем некоторое минимальное время t и на основании вычисления Р определим температуру Процесса
 (2.3)
(2.3)
Пример 1: Определить температуру разгонки As, предварительно внедренного с помощью ионной имплантации в кремний р - типа с удельным сопротивлением 1 Ом-см, если распределение должно обладать глубиной залегания p-n-перехода Xj = 0.5 мкм, поверхностной концентрацией Со = 1 5 • 1020 см'3, а длительность процесса составляет 1 час. Вычислить количество атомов мышьяка N, которое должно быть внедрено в Si.
Решение:
1. С помощью зависимости руд = f(C) (рис. 1.5) найдем С, (т.е.концентрацию примеси в исходной подложке) для Si с руд= 1 Ом•см:
СB = 1.5 •1016 см-3.
2. Определим D по формуле
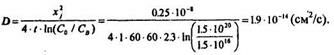
3. Из графика D = f(T) определяем, что такому значению D соответствует температура 1070 °С.
4. Рассчитаем количество атомов As, которое необходимо внедрить перед диффузией с помощью ионной имплантации:
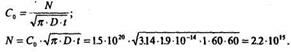
Пример 2: Определить режим диффузии As, проводимой в одну стадию при постоянной поверхностной концентрации С0 = 1.5 • 1020 см-3 (т.е. из бесконечного источника), если подложка Si имеет руд = 1 Ом • см, глубина xj = 0.5 мкм, время диффузии - 1 час.
Решение:
1. С помощью зависимости руд= f(C) найдем CВ:
Св=1.5 • 1016 см-3.
2. Для диффузии из бесконечного источника распределение примеси описывается erfc - функцией, т.е.
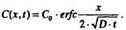
Для этого случая Xj определяется из выражения
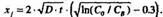
Возведем обе части в квадрат и определим D из выражения
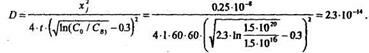
3. По найденному D из зависимости D = f(Т) (рис. 1.4) определим температуру -1080 °С. Учтем предельную растворимость As.
По зависимости С = f(T) (рис.1.3) определим, что для Т=1080 °С предельная растворимость равна 1.7-1021 см . У нас по условию задачи поверхностная концентрация С0 = 1.5 • 1020 см-3 , т.е. необходимо для диффузии использовать обедненный источник диффузанта.
1.2 Двухстадийная диффузия Задача решается в 2 этапа.
1. Определяем режим разгонки.
2. На основании полученных данных - режим загонки.
Режим разгонки найдем, используя формулу (10), т.е.
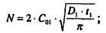
возведем обе части выражения в квадрат и выразим D1•t1:
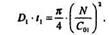
Для стадии разгонки имеем по формуле (9)
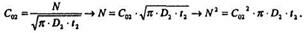
Подставим N в предыдущее выражение
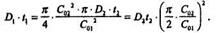
Из этого выражения видно, что для двухстадийной диффузии необходимо регулировать поверхностную концентрацию при загонке С01 либо задавать температуру загонки Т1, определяющую два параметра D1 и С01, а время загонки t, рассчитать по известным данным:
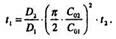
Пример 3: Определить температуры и длительность процессов загонки и разгонки в случае двухстадийной диффузии В в Si n-типа с pуд = 10 Ом • см, если искомое распределение примеси должно иметь следующие параметры:
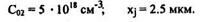
Решение:
1. Зная руд по графику р = f(T) (рис. 1.5), находим СB (концентрацию примеси в исходной подложке):
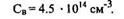
2. Рассчитаемпроизведение D2 • t2
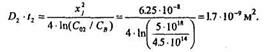
3. Теперь нужно задать либо температуру, либо время разгонки. Зададим температуру, например Т2 = 1150 °С. Для этой температуры можем найти D2 из графика D =f(T) (Рис. 1.4), т.е. D2=7.2 • 10-13 см2/с.
Можем определить время разгонки t2:
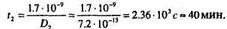
4. Зададим теперь температуру загонки, например Ti=1050°C.
Для этой температуры можем найти Di из графика D = f(Т) (рис. 1.4), т.е.D1 = 6.9 • 10-14 см2/с и С01 из графика С = f(T) (рис. 1.3), т.е. С01 =3 • 1020 см-3.
5. Определим длительность загонки:
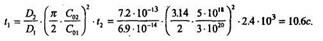
Практически такое время загонки нереально, поэтому нужно использовать либо обедненный источник бора, либо вводить примесь методом ионного легирования.
6. Если использовать ионное легирование, то рассчитаем количество атомов В, которые необходимо ввести при загонке:
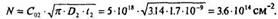
6. Если использовать обедненный источник примеси, то зададим реальное время загонки t| и определим произведение:
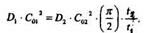
Пусть t1 = 10 мин, тогда:
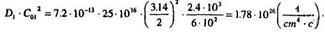
8. Зададим Т1 = 1050 °С, тогда D, = 6.9 • 10-14 см2/с. Тогда из предыдущего выражения
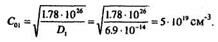
1.3. Определение режимов последовательной диффузии Пусть требуется получить типовую биполярную транзисторную структуру:
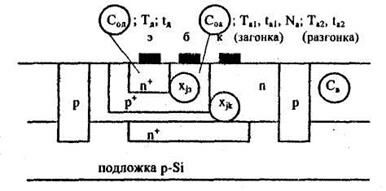
Параметры, обведенные кружком -это заданные параметры
Параметры эмиттерной диффузии: Сод; Тд; tД.
Параметры базовой диффузии: С0а; Ta1; tа1; Nа; Tа2; tа2.
Са - концентрация примеси в эпитаксиальном слое (Известна), т.е. коллектора;
Сод; Соа, - концентрация донорной и акцепторной примесей в эмиттерной и базовой областях соответственно.
Необходимо определить:
1. Режим загонки акцепторной примеси – Та1, ta1, Na.
2. Режим разгонки акцепторной примеси – Та2, tа2.
3. Режим разгонки донорной примеси – Тд, ts.
Расчет режима базовой диффузии аналогичен расчету двухстадийной диффузии в однороднолегированный полупроводник.
Для упрощения принимают, что при эмиттерной диффузии не происходит заметного смещения распределения концентрации акцепторной примеси, т.е.
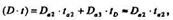
где Dа3 - коэффициент диффузии акцепторной примеси при температуре эмиттерной диффузии.
Для расчета режима эмиттерной диффузии используют уравнение для глубины залегания эмиттерного p-n-перехода:
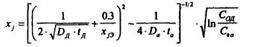
Решив его относительно Dд tД определяем либо температуру, либо длительность процесса диффузии, т.е.:
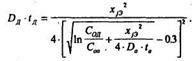
Пример 4. Определить режим загонки (Tа1, tа1, Nа) и разгонки (Та2, tа2) при базовой диффузии В и режим загонки (Тд, tд при эмиттерной диффузии Р в Si, если задано:
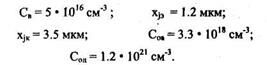
Решение:
Определим режимы базовой диффузии.
1. Найдем произведение Dа2tа2:
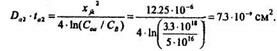
2. Зададим температуру разгонки, например Та1 =1150 "С. Для этой температуры можем найти Dа2 из графика D = f(T), т.e. В2=7.2 • 10-13 см2/c.
Можем определить время разгонки tа2:
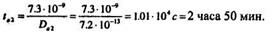
3. Найдем количество атомов В, необходимое для базовой диффузии:
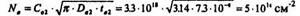
4. Режим загонки бора выберем на основе произведения:
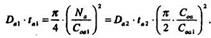
Зададим теперь температуру загонки бора Tа1 = 1050 °С, и из Графика D = f(T) определим коэффициент диффузии при этой температуре:
Dа1 = 6.9 • 10-14 см2/с,
а из графика С = f(T) определим концентрацию
С0а = З • 1020 см-3.
4. Подставим эти значения в предыдущую формулу и определим время загонки бора tа1:
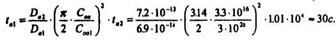
На практике такое время загонки реализовать трудно, так как необходимо время для установления стационарного потока диффузанта.
Поэтому, как и в предыдущем примере, зададим время загонки, пусть tа1 =10 мин.
Вычислим произведение:
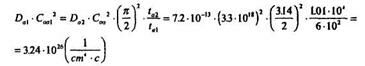
Зададим поверхностную концентрацию бора Соа1 = 5 • 1019 см-3, подставим в предыдущее выражение и рассчитаем коэффициент диффузии Dа1:
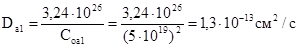
Для этого коэффициента диффузии температура Та1 = 1065°С (рис. 1.4).
7. Определим режим эмиттерной диффузии. Для этого рассчитаем произведение Dдtд:
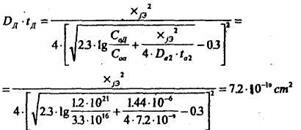
8. Зададим время загонки, пусть ta = 1 час. Подставим это значение и рассчитаем Da:
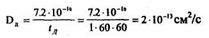
По графику D = f(T) определим температуру эмиттерной диффузии:
Тд=1125°С.
9. Оценим справедливость допущения, что распределение В не изменяется при диффузии Р. Сравним Da2ta2 и Da3tд
Для Т = 1125 ОС => Da3 = 4 • 10-13 см2/с
Тогда:

т.е. выполняется соотношение:
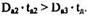
Бор в базе практически не разгоняется при формировании эмиттера диффузией фосфора.
Практическое занятие N3.
Методы расчета ионно-легированных структур.
Ионное легирование (ИЛ) - это процесс бомбардировки твердых тел пучками ускоренных ионов с целью изменения их свойств и структуры.
С помощью Ионного легирования решаются те же технические задачи, что и при термической диффузии, однако данный метод имеет свои особенности.
Типичные параметры ИЛ:
Еуск = 10 – 300 кэВ (1МэВ);
Диаметр ионного пучка ~ 1 см2
Ток ионного пучка = l0  A … mA
A … mA
Глубина внедрения - до 0,5 мкм
Структурная схема установки для ИЛ.
1. Установка с Е > 100 кэВ
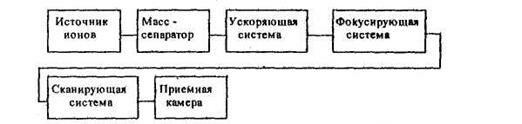
2. Установка с Е < 100 кэВ
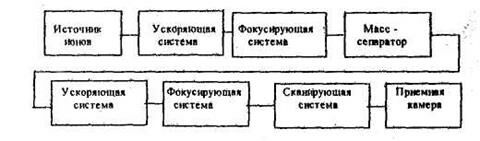
Преимущества ИЛ
1. Высокая управляемость процесса (точное задание дозы и Е).
2. Выбор примеси не ограничивается предельной растворимостью материалов в твердом состоянии.
3. Уменьшение геометрических размеров приборов за счет малого бокового отклонения ионов под защитную маску.
4. Возможность получения сложных ступенчатых профилей.
5. Низкая температура процесса.
6. Чистота процесса (возможность легирования через защитную маску).
Недостатки ионного легирования
1. Возможность получать только неглубокие профили(~0.5 мкм).
2. Повреждение кристаллической решетки требует последующего отжига при Т ~ 450 - 900 °С.
3. Сложность и громоздкость оборудования.
Пробеги ионов
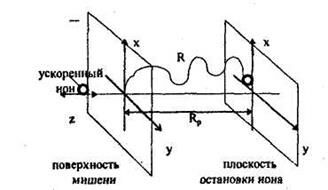
R - полная длина пробега; Rp - проекция полной длины пробега(средний нормальный пробег);  Rp - среднеквадратичное отклонение проекции полной длины пробега (разброс).
Rp - среднеквадратичное отклонение проекции полной длины пробега (разброс).
Для расчета среднего полного пробега R (см) иона с энергией Е (эВ) используют формулы, в которых Е и R выражены в безразмерных единицах е и р соответственно:
 (3.1)
(3.1)
L - нормирующий множитель пробега (см-1)
 (3.2)
(3.2)
где
с = 0.45; d = 0.3 - параметры, учитывающие торможение за счет ядерного взаимодействия;
k и  - коэффициенты, учитывающие торможение за счет электронного взаимодействия:
- коэффициенты, учитывающие торможение за счет электронного взаимодействия:
 (3.3)
(3.3)
z( и z2 - заряды ядра иона и мишени;
M1 и М2 - массы ядра иона и атома мишени
 (3.4)
(3.4)
F - нормирующий множитель энергии (эВ1)
 (3.5)
(3.5)
а - радиус экранирования заряда ядра электронами (см)
 (3.6)
(3.6)
у - коэффициент передачи максимальной энергии ионом атому мишени при лобовом столкновении:
 (3.7)
(3.7)
N2 - собственная концентрация атомов мишени.
Пример 1. Рассчитать средний полный пробег ионов бора с энергией Е = 100 кэВ в Si, если z1 = 5, z2 = 14, М1 = 11, М2 = 28.09, N2= 4.98 • 1022 см-3, с = 0.45, d = 0.3.
1. Необходимо определить: радиус экранирования - а;
коэффициент передачи энергии -  ;
;
коэффициенты электронного торможения - k,  ;
;
нормирующие множители - L, F.
2. Определим радиус экранирования а;
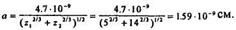
3. Коэффициент передачи максимальной энергии  :
:
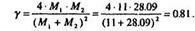
5. Коэффициенты электронного торможения k и  :
:
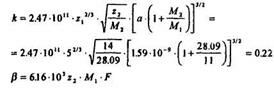
5. Нормирующие множители для пробега L и энергии F:

Теперь можно рассчитать  :
:
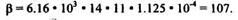
6, Рассчитаем энергию в безразмерных единицах, т.е. (необходимо для расчета безразмерного пробега p):
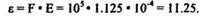
7. Рассчитаем пробег в безразмерных единицах, т.е. р:
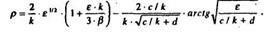
Вычислим отдельные множители:
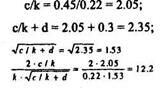
Подставим в предыдущую формулу,
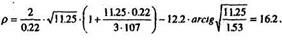
8. Выразим пробег в размерных единицах:
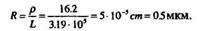
Понятие среднеквадратичного отклонения нормального пробега(или проекции) (ARp)
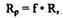
где f - корректирующая поправка, связанная с упругим рассеянием;
R - полная длина пробега;
Rp - проекция полной длины пробега.
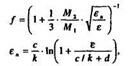
где  П - полная энергия, затраченная на упругое рассеяние;
П - полная энергия, затраченная на упругое рассеяние;
 - энергия в безразмерных единицах.
- энергия в безразмерных единицах.
Так как Rp - это средняя проекция пробега, то часть ионов не достигает Rp, а часть проникает глубже Rp.
Итак,  Rp - это среднеквадратическое отклонение проекции пробега или разброс:
Rp - это среднеквадратическое отклонение проекции пробега или разброс:
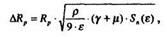
где  - это коэффициент, равный M2/M1.
- это коэффициент, равный M2/M1.
р - пробег в безразмерных единицах;
 - коэффициент передачи максимальной энергии при лобовом столкновении;
- коэффициент передачи максимальной энергии при лобовом столкновении;
 - энергия в безразмерных единицах;
- энергия в безразмерных единицах;
Sn( ) - ядерная тормозная способность:
) - ядерная тормозная способность:
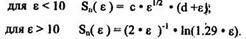
Практическое занятие N4.
Методы расчета ионно-легированных структур (продолжение)
Пример I: Рассчитать Rp и  Rp ионов 11В+ с энергией 100 кэВ в Si.
Rp ионов 11В+ с энергией 100 кэВ в Si.
1. Используя данные примера 1 предыдущего практического занятия, найдем потери на ядерное торможение  п
п
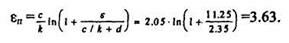
2. Рассчитаем поправку на упругое рассеяние f:
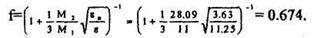
3. Для е > 10 определим тормозную способность Sn( )
)
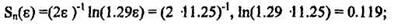
4. Соотношение масс сталкивающихся частиц  :
:
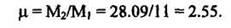
5. Средний нормальный пробег или проекция пробега Rp:
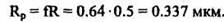
6. Среднеквадратичное отклонение пробега  Rp:
Rp:
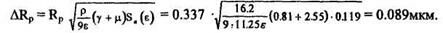
Значения Rp и  RP табулированы для различных ионов и энергий, т.е. [(Rp и
RP табулированы для различных ионов и энергий, т.е. [(Rp и  Rp = f(E)], либо определяются из графиков:
Rp = f(E)], либо определяются из графиков:
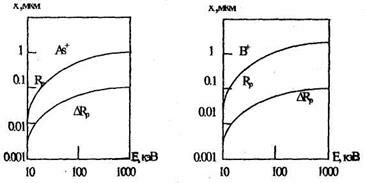
Профиль распределения примеси при ионном легировании , т.е. С(х) описывается в первом приближении кривой Гаусса:
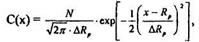
где N - доза [ион/см2];
Rp - средняя проекция длины пробега [мкм];
 Rp - среднеквадратичное отклонение длины пробега [мкм];
Rp - среднеквадратичное отклонение длины пробега [мкм];
х - расстояние от поверхности образца [мкм].
Максимальная концентрация достигается на глубина х = Rp (положение пика концентрации). Для этого случая:
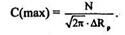
Кроме того, важнейшими параметрами ИЛ являются:
Е - энергия ионов и N - доза внедренных ионов.
Доза - это количество частиц, бомбардирующих единицу поверхности за данное время. На практике N определяется параметрами процесса ИЛ:
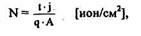
где t - время облучения;
j - ионный ток;
А - площадь сечения ионного пучка;
q - заряд иона (для однозарядного е = 1.6 • 10-19 Кл).
Увеличение дозы легирования - один из путей уменьшения эффекта каналирования за счет увеличения количества дефектов решетки.
Пример 2: Требуется внедрить атомы В в канал МОП-транзистора. Максимальную концентрацию 8 • 1016 см-3 желательно иметь на глубине около 150 нм.
Найти ускоряющее напряжение (Еуск), дозу (N) и разброс ( RP).
RP).
Решение:
1. Т.к. известно Rp = 150 нм = 0.15 мкм, из графика х = f(Еуск) или по таблицам для В находим:
Еуск = 50кэВ и  Rp = 0.05 мкм
Rp = 0.05 мкм
2. Известно, что
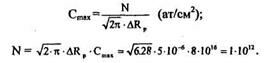
Пример 3: Необходимо внедрить ионы As+ в Si-подложку. Максимальная концентрация 1 • 101 см"3 должна быть получена на глубине около 100 нм. Найти Еуск, дозу (N) и разброс ( Rp ).
Rp ).
Решение:
1. Зная Rp = 0.1 мкм, находим из графика х=f(Еуск) или по таблицам для ионов As+:
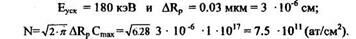
Пример 4: Построить график распределения концентрации ионов Р для легирования Si при дозе 1015 см-2 и ускоряющих напряжениях 40 и 80 кэВ.
Решение:
Из таблиц (или графиков Rp,  Rp= f(Е)) находим:
Rp= f(Е)) находим:
При 40 кэВ Rp = 49 нм  Rp = 16,4 нм
Rp = 16,4 нм
При 80 кэВ Rp = 98 нм  Rp = 29,5 Нм
Rp = 29,5 Нм
При расчете Сmax и С(х) нм необходимо перевести в см и использовать формулу
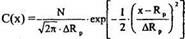
Для построения кривых рассчитываем значения концентрации примеси как минимум в трех точках для каждого ускоряющего напряжения, например,: 1 точка - х = Rp; 2 точка - х = 2 Rp; 3 точка - х=0;
С40(х = Rp ) = 2.4 • 1020; С40(х= 0)= 2.8 • 1016;
С40(х = 2 Rp) = 2.8 • 1016; С80(х= Rp )= 5.4 • 1019;
С80(х = 0) = 2,2 • 1017; С80(х=2 Rp)= 2.2 • 1017.
Расчет профилей распределения примесей в структурах с двойной имплантацией.
Для получения n-p-n-транзистора проводят последовательно ИЛ акцепторной и донорной примесью подложки п-типа.
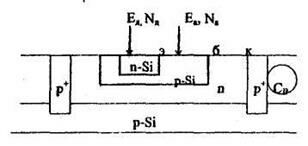
Причем Rра > Ярд, а Смах в < Смах д. Суммарное распределение примеси:
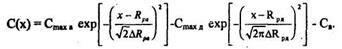
Глубина залегания коллекторного перехода:
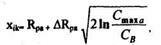
где
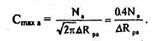
Глубина залегания эмиттерного перехода и Смах:
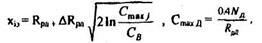
Толщина базы:
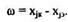
Пример 5: Рассчитать профиль распределения концентрации примеси в транзисторной структуре, созданной внедрением 11В+ и 31Р+ в Si n-типа, если:
СВ=-1016 см-13; Еа = 100кэВ. Ед = 200кэВ; Nа= 5 • 1013см-2; Nд=11015 см-2.
Решение:
1. Зная энергии внедрения, можем из таблиц определить Rp и ARp ионов В+и Р+:
Для В+ при 100 кэВ Rpa = 0.398 мкм  Rpa = 0.094 мкм.
Rpa = 0.094 мкм.
Для Р+ при 200 кэВ Rpa = 0.254 мкм  Rрд = 0.061 мкм.
Rрд = 0.061 мкм.
2. Найдем максимальные концентрации В и Р:

3. Найдем глубины Xjk и Xj3:

Если построить суммарное распределение С(х), получим:
Практическое занятие N5.
Определение технологических режимов ионного легирования
Это так называемые обратные задачи, т.е. определение энергии Е, необходимой для получения заданного среднего нормального пробега Rp или дозы облучения N, необходимой для получения заданной концентрации примеси.
1. Расчет энергии ионов для получения заданного пробега Соотношение пробег-энергия описывается формулой
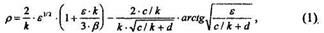
однако простым преобразованием нельзя выразить зависимость энергии от пробега, т.е.  = f(p).
= f(p).
Эту формулу можно упростить, исходя из разложения в ряд функции arctg х и, учитывая, что во многих случаях  • k <= 3 •
• k <= 3 •  , тогда:
, тогда:
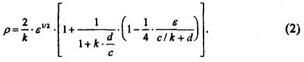
Если соблюдается условие 6 <= с/к + d (это справедливо для большинства практических случаев), то 1п(1+х) »хииз формулы для корректирующей поправки f и энергии на упругое рассеяние иона б„ следует, что
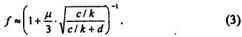
Средний нормальный пробег рР (Rp) связан с полным пробегом p(R) соотношением
рр = f • р - в безразмерных величинах.
Подставив в него формулы (2) и (3) и решив полученное кубическое уравнение, найдем зависимость энергии иона от его среднего нормального пробега.
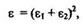
Где
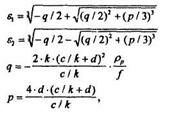
где рр - средний нормальный пробег (или проекция длины пробега) в безразмерных величинах, а р и q - численные параметры.
Пример 1: Определить энергию Е, необходимую для получения среднего нормального пробега ионов Р в Si, равного 0.1 мкм (Rp=0.l мкм).
Для Р: z1 = 15, М1 = 31.
Дм Si: z2 = 14, М2 = 28.09, N2 = 4.96 • 1022(см-3).
Дня определения б необходимо найти ei и е2, р и q, соответственно рр и f, а также нормирующие множители L и F.
1. Определяем соотношение масс ц.:
 = M2/M, = 28.09/31=0.905.
= M2/M, = 28.09/31=0.905.
2. Радиус экранирования а:
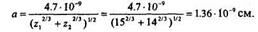
3. Коэффициент передачи максимальной энергии при лобовом столкновении у:
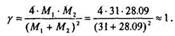
4. Нормирующий множитель энергии F:
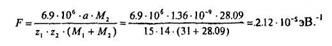
5. Нормирующий множитель пробега L:
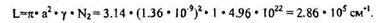
6 Коэффициент электронного торможения к:
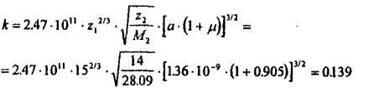
7. Перед тем как рассчитать f (поправку на упругое рассеяние), рассчитаем отдельные множители:
с/k = 0.45/0.139 = 3.24;
c/k + d = 3.24 + 0.3 = 3.54.
(c и d- параметры ядерного торможения = const = 0.45 и 0.3)
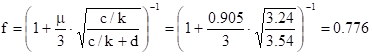
8. Рассчитаем средний нормальный пробег (или проекцию длины пробега) рр в безразмерных единицах:
pp = Rp • L = 0.1 • 10-4 • 2.86 • 105 = 2.86.
9. Найдем значения q и р:
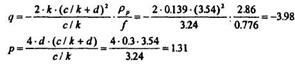
10. Определим значения Е и е2, но сначала вычислим подкоренное выражение:
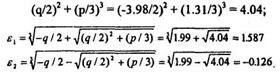
И, Определим значение энергии е в безразмерных величинах, соответствующих данному пробегу:
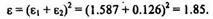
12. Определим энергию в размерных величинах, т.е. в эВ:
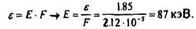
Задачу можно решить графически, имея табличные данные зависимости Rp = f(Е). Для этого строится график Rp(E) и для заданного Rp находится Е.
II. Расчет дозы облучения для получения заданной концентрации примеси
Профиль концентрации примеси при ИЛ описывается кривой Гаусса:
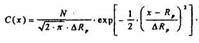
Для ее построения нужно знать Rp,  Rp и N - все эти параметры обычно неизвестны.
Rp и N - все эти параметры обычно неизвестны.
Известны параметры - Xj, Cmax и Св.
Выражение xj получаем из условия С(х) = 0:
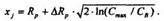
Доза облучения N находится из выражения для Сmах:
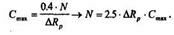
В этом случае для расчета дозы используют графическое решение:
Задают несколько значений Е и для них находят Rp,  Rp.
Rp.
Строится зависимость правой части уравнения для xj от Е. Для заданного значения xj (проведя прямую параллельно оси энергий до пересечения с прямой Rp +  RP) находят искомую энергию.
RP) находят искомую энергию.
Зная энергию, находят для нее  RP и рассчитывают дозу N.
RP и рассчитывают дозу N.
Пример2: Определить энергию и дозу облучения, необходимые для создания p-n-перехода на глубине xj = 0.3 мкм с помощью внедрения Р в Si p-типа с Св=1O16 см-3, если необходимо обеспечить Сmях = 5 • 1019см-3.
1. Из уравнения для xj:
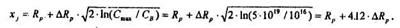
2. Построим кривую Rp + 4.12 •  Rp от энергии в диапазоне Е=80... 160 кэВ, пользуясь табличными данными Rp = f(E) и
Rp от энергии в диапазоне Е=80... 160 кэВ, пользуясь табличными данными Rp = f(E) и  Rp =f(E).
Rp =f(E).
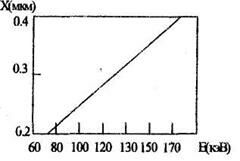
3. Для этой Е = ПО кэВ найдем из таблиц для Rp и  Rp их значения:
Rp их значения:
Rp = 0.136 мкм;  Rp= 0.038 мкм.
Rp= 0.038 мкм.
4. Рассчитаем дозу облучения:
N = 2.5 •  Rp • Cma[= 2.5 • 3.8 • 10-6 • 5 • 1019= 4.75 • 1014 см-2.
Rp • Cma[= 2.5 • 3.8 • 10-6 • 5 • 1019= 4.75 • 1014 см-2.
Расчет режимов имплантации для создания транзисторной структуры
ПримерЗ: Необходимо создать n-p-n-структуру с толщиной базовой области  = 0.1 мкм, xjэ = 0.2 мкм, СВ = 2 • 1016 см-3; Сmax а = 3 • 1018 см-3, Сmax д = 1 • 1020 см-3. Базовая область создается внедрением В, а эмиттеры - Р. Определить режимы ИЛ, т.е. Na, Nд, и Еа„ Ед.
= 0.1 мкм, xjэ = 0.2 мкм, СВ = 2 • 1016 см-3; Сmax а = 3 • 1018 см-3, Сmax д = 1 • 1020 см-3. Базовая область создается внедрением В, а эмиттеры - Р. Определить режимы ИЛ, т.е. Na, Nд, и Еа„ Ед.
В общем виде данная задача не решается. Необходимо использовать упрощающие соотношения:
1. Для хjк:
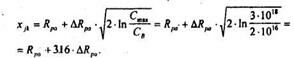
Для ионов с массами М1 < M2 в диапазоне Е = 20... 100 кэВ
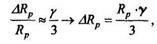
где  - коэффициент передачи максимальной энергии при лобовом столкновении:
- коэффициент передачи максимальной энергии при лобовом столкновении:
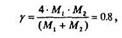
тогда
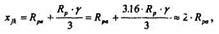
Откуда
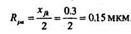
По таблице Rp = f(E) ближайшее значение энергии соответствует 40 кэВ. Для этой Е => Rpa, = 0.161 мкм,  Rp, = 0.0538 мкм.
Rp, = 0.0538 мкм.
Тогда
xjk = 0.161 + 3.16 • 0.058 = 0.33 мкм.
2. Доза облучения ионами В определяется по формуле
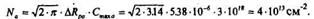
3. Для эмитгерного перехода
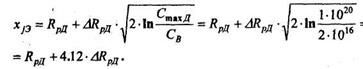
Приближенное выражение для xj3:
Если M1 > М2 в диапазоне Е = 20...100 кэВ
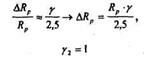
Тогда
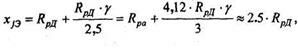
Откуда
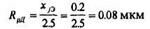
По таблице Rp = f(E) ближайшее значение энергии соответствует 80 кэВ. Для этой Е => Rpд = 0.098 мкм,  Rpд = 0.0295 мкм. Тогда
Rpд = 0.0295 мкм. Тогда
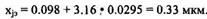
4. Доза облучения ионами Р.
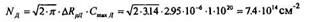
Практическое занятие N6.
Термическое окисление
Одним из базовых технологических процессов производства изделий ЭОТ на основе кремния является процесс термического окисления. Он используется для получения на поверхности кремниевых пластин защитного слоя диоксида кремния, в котором методами литографии формируется в дальнейшем контактная маска, определяющая конфигурацию легированных областей будущих приборов. С использованием такой локальной маски осуществляется последующее легирование пластин методами термической диффузии или имплантации.
В технологии формирования ИС оксиды используются в качестве:
4. Масок при ИЛ или диффузии.
5. Пассивации поверхности полупроводниковых структур.
6. Изоляции приборов друг от друга.
7. Подзатворного диэлектрика в МОП-структурах.
5. Межслойной изоляции в многослойных металлизационных
структурах и т.д.
В настоящее время для формирования окисных слоев используется несколько методов:
1. Термическое окисление.
2. Анодирование в растворах электролитов.
3. Пиролитическое осаждение (осаждение из газовой фазы).
4. Плазменное анодирование.
5. Вакуумные методы.
Термическое окисление является наиболее распространенным методом в технологии ИС.
Химические реакции при термическом окислении Si:
Siтв + O2 => SiO2тв; (1)
Siтв, + 2H2O => SiO2тв, + 2H2 , (2)
, (2)
Термическое окисление - это реакция с расходованием материала подложки.
Модель термического окисления кремния
Кинетика процесса окисления описывается моделью Дила-Гроува. Она применима для температурного диапазона 700-1300 °С, парциальных давлений кислорода (0.2 - 1.0) • 105 Па, толщины окисных пленок 30-2000 нм в атмосфере О2 и Н2O.
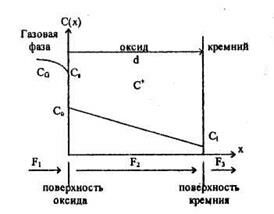
Окисляющие элементы диффундируют из газовой фазы на границу газ-окисел (поток F, представляет число атомов или молекул, пересекающих поверхность единичной площади за единицу времени), переносятся через уже образовавшийся окисел (поток F2) и реагируют на границе SiO2-Si с кремнием (поток F3).
В условиях равновесия F1 = F2 = F3
Для потока F1:
 (3)
(3)
где h0 - коэффициент массопереноса в газовой фазе;
Со - концентрация окислителя в объеме газовой фазы;
Cs - концентрация окислителя у поверхности окисла.
Чтобы связать равновесную концентрацию окислителя в окисле с его концентрацией в газовой фазе, воспользуемся законом Генри:

где Со - концентрация в окисле на внешней поверхности (равновесная);
С* - объемная концентрации в окисле (равновесная);
ps - парциальное давление в газовой фазе у поверхности окисла;
рG - парциальное давление в объеме газовой фазы;
Н - постоянная Генри.
С учетом закона идеальных газов можно заменить Со и Cs парциальными давлениями:

Объединив уравнения 4-6, получим для Fi:

где h - коэффициент массопереноса в газовой фазе, выражаемый в размерности концентрации в твердом теле, т.е.
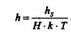
Для потока F2 (поток окисления через окисел): Этот поток описывается законом Фика, т.е.

где D - коэффициент диффузии окислителя;
 - градиент концентрации окислителя в окисле.
- градиент концентрации окислителя в окисле.
Если процесс установившийся, т.е. F2 одинаков в любой точке внутри окисла ( т.е. dF2/dd = 0), получим:

где
Ci - концентрация окислителя на границе окисел-кремний;
d0 - толщина окисла.
Для потока F3. Предполагается, что он пропорционален Q:

где ks - константа скорости реакции окисления. Если совместно решить уравнения для F|, F2 и F3, то получим выражения С; и Со:
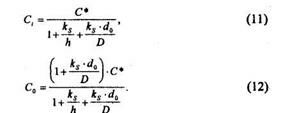
Предельные случаи при рассмотрении уравнений (11) и (12) возникают, когда коэффициент диффузии D либо слишком мал, либо слишком велик.
1. Когда D слишком мал:
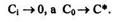
В этом случае говорят, что реакция идет при диффузионном контроле, т.е. лимитирующей стадией является диффузионная стадия протекания реакции. Скорость реакции зависит от скорости доставки окислителя к границе раздела фаз.
2. Когда D очень велик:
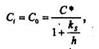
Говорят, что реакция идет при кинетическом контроле, т.е скорость окисления зависит от константы скорости реакции ks и концентрации Qi, равной Со.
Чтобы рассчитать скорость роста окисла, определим N1 как число молекул окислителя, входящих в единичный объем окисного слоя. Так как окисел содержит 2.2 • 1022 см-3 молекул SiO2 и на создание SiO2 требуется одна молекула О2 или две молекулы Н2О, то:
N1 = 2.2 • 1022 см-3 - для окисления в сухом кислороде;
N1 = 2 • 2.2 • 1022 см-3 - для окисления в парах воды.
Если (11) подставить в (10), можно записать выражение для потока окислителя, достигающего границы раздела SiO2-Si в следующем виде:
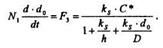
Если решить это дифференциальное уравнение исходя из предположения, что на поверхности Si уже мог быть некоторый слой окисла (т.е. d0 = d1 при t = 0), получим
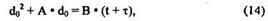
где
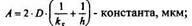
 - параболическая константа скорости, мкм2/ч;
- параболическая константа скорости, мкм2/ч;
 - время
- время
 - соответствует сдвигу по временной оси, который необходим, чтобы учесть наличие первоначального слоя окисла толщиной di.
- соответствует сдвигу по временной оси, который необходим, чтобы учесть наличие первоначального слоя окисла толщиной di.
Решение (14) для d0 = f(t) выглядит так:
 (15)
(15)
При анализе данного уравнения необходимо учесть два предельных случая:
1. Большое время окисления, т.е. t +  >> А2/4 • В;
>> А2/4 • В;
do2 = В • t - параболический закон роста (диффузионный контроль). (16)
2. Очень малое время окисления, т.е. t +  << А2/4 • В;
<< А2/4 • В;
 - линейный закон роста (кинетический контроль); (17)
- линейный закон роста (кинетический контроль); (17)
 - линейная константа скорости окисления
- линейная константа скорости окисления

Константы А, В и В/А рассчитаны и табулированы для окисления в сухом и влажном кислороде.
С* - равновесная концентрация окислителя в окисле (см-3).
Так, например, в SiO2 при 1000 °С она составляет:
| Окислитель | Равновесная концентрация С*, см-3 |
| O2 | 5.2 • 1016 |
| H2O | 3 • 1019 |
Эмпирические формулы для расчета времени окисления
1. Во влажном О2:
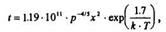
t - время окисления (мин), р - давление кислорода (Па); х -толщина SiO2 (м); k - const Больцмана = 8.6 • 10-5 эВ/К;
Т - температура (К).
2. В парах воды:
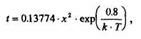
t - время окисления (мин); х - толщина SiO2 (мкм); k - const Больцмана = 8.6 • 10-5 эВ/К; Т - температура (К).
Пример1: Рассчитать толщину слоя Si, который расходуется на образование слоя термического окисла толщиной 1 мкм, если dSi = =2.33 г/см3, dSiO2 = 2.27 г/см3.
1. Реакция, протекающая при термическом окислении:
Si + О2 => SiO2.
Определим молекулярные веса вступающих в реакцию и образующихся веществ:
М.в. Si = 28 г;
M.B. SiO2 = 28+16 • 2 = 60 г.
2. Определим объем Si, вступившего в реакцию, и объем образовавшегося SiO2:
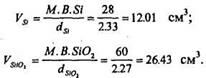
. Соотношение толщин Si и SiO2 будет пропорционально соотношению объемов, т.к. площадь постоянна:
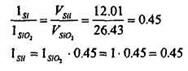
Пример 2: Определить время, необходимое для получения пленки SiO2 толщиной 2 мкм при температуре 920 °С методом термического окисления в парах воды при атмосферном давлении и давлении 20 атм (2 Ml 1а). параболические константы Ватм=0.203 мкм2/ч, В2мпа = 3.00 мкм2/ч.
1. Для этого случая t >> А2/4 • В,  = О, В920 = 0.203 мкм2/ч;
= О, В920 = 0.203 мкм2/ч;
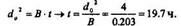
По эмпирической формуле

2. При давлении 20 атм. = 2 МПа: В2мп. = 3.00мкм2/ч;
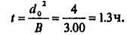
Таким образом, при окислении под давлением приблизительно на порядок можно сократить время окисления, что широко используется на практике, например, в технологии ISOPLANA
Практическое занятие N 7.
Анализ и расчет характеристик тонкопленочных контактов металл-полупроводник
Неотъемлемой частью любого изделия ЭОТ на базе полупроводников являются тонкопленочные контакты типа металл-полупроводник, выполняющие роль связующего звена между полупроводниковой структурой и внешней электрической цепью. С ростом степени интеграции изделий растет и число контактных окон к элементам изделия, т.е. увеличивается число контактов с одновременным уменьшением их топологических размеров.
Тонкопленочные контакты в изделиях ЭОТ бывают невыпрямляющие (омические) и выпрямляющие или диоды Шоттки.
Краткий анализ характеристик контактов
Качество ИЭОТ существенно зависит от электрофизических свойств и надежности металлизации, в частности, невыпрямляющих контактов.
Невыпрямляющие. контакты (НК) класса металл-полупроводник являются неотъемлемым атрибутом любых полупроводниковых ИС. Система тонкопленочных НК, токопроводящих дорожек и контактных площадок образует металлизацию изделия.
Четверть отказов полупроводниковых ИС приходится на металлизацию.
Переходное сопротивление НК логических ИС непосредственно влияет на ВАХ участков схемы и значение напряжения логического 0.
Важнейшими характеристиками НК являются:
1. Переходное сопротивление рк (Ом • см2).
2. Высота потенциального энергетического барьера  В (В).
В (В).
3. Уровень инжекции неосновных носителей.
4. Время наработки на отказ и т.д.
Структура и свойства контактов металл-полупроводник зависит от взаимного расположения уровней Ферми в металле EFm и погупроводнике EfS(pHc.7.1).
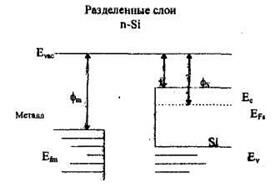
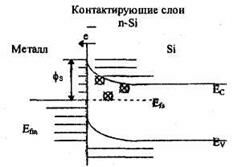
б) Рис.7.1. Зонная диаграмма выпрямляющего контакта.
Если рассматривать случай контактирующих слоев (б), то поскольку Фs<Фm, то электроны переходят из полупроводника в металл и вблизи границы с металлом образуются нескомпенсированные положительные ионы доноров и зоны искривляются вверх (т.к. направление электрического поля в этом слое таково, что энергия основных носителей заряда в нем больше, чем в толще полупроводника).
Для контакта металла с полупроводником p-типа при Фs>Фm, электроны из металла переходят в полупроводник, в приповерхностном слое рекомбинируют с дырками и образуются нескомненсированные отрицательные ионы акцепторов, препятствующие дальнейшему переходу. А зоны при этом искривляются вниз (рис.7.2).
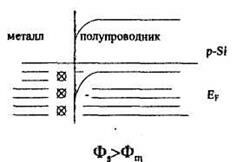
Рис.7.2 Зонная диаграмма выпрямляющего контакта.
Такой контакт характеризуется наличием обедненного слоя в приконтактном слое полупроводника, следовательно, приконтактный слой обладает повышенным сопротивлением и поэтому определяет сопротивление всей системы, т.е. эта особенность характерна для p-n-перехода.
Потенциальный барьер в приконтактном слое называют барьером Шоттки и его величина будет меняться в зависимости от полярности приложенного напряжения (прямое + к металлу, обратное - к n-Si).
Высота Ф, для контакта-Ме n-тип:
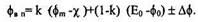
Для контакта Ме-p-тип:
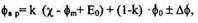
Где
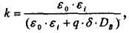
 - электронное сродство к полупроводнику,
- электронное сродство к полупроводнику,
 т - работа выхода электронов из металла,
т - работа выхода электронов из металла,
Е0 - ширина запрещенной зоны,
 о- нейтральный уровень поверхностных состояний,
о- нейтральный уровень поверхностных состояний,
 I - диэлектрическая постоянная вакуума, 8.86 • 10-12 Ф•м-1,
I - диэлектрическая постоянная вакуума, 8.86 • 10-12 Ф•м-1,
 i - диэлектрическая проницаемость диэлектрика на границе раздела металл-полупроводник (Ф см-1),
i - диэлектрическая проницаемость диэлектрика на границе раздела металл-полупроводник (Ф см-1),
 - толщина диэлектрика на границе металл-полупроводник (см),
- толщина диэлектрика на границе металл-полупроводник (см),
DB - плотность поверхностных состояний (см'2, эВ"1),

 - поправка на действие сил изображения (силы изображения - это силы притяжения электронов в слое объемного заряда к металлической поверхности),
- поправка на действие сил изображения (силы изображения - это силы притяжения электронов в слое объемного заряда к металлической поверхности),
q - заряд электрона, 1.6 •10-19 Кл.
При ФМ<ФS происходит накопление основных носителей в полупроводнике, т.е. получается обогащенный слой (рис.7.3).
Сопротивление системы в целом определяется нейтральным слоем полупроводника и, следовательно, не зависит от величины и полярности приложенного напряжения.
На практике для создания БШ используют Mo, Pt, PfSi, Аи, а для создания ИС применяют А1, Ti, силициды тугоплавких металлов и т.д.
Для создания НК обычно проводят подлегирование приповерхностной области контактов, создавая п+ и р+ - области под ними.
Разделенные слои
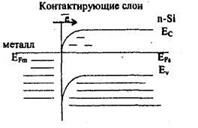
Рис.7.3 Зонная диаграмма невыпрямляющего контакта.
Методы определения величины переходного сопротивления ИК
Все они сводятся к выделению переходного сопротивления НК Rk из измеренного полного сопротивления образца.
Их можно классифицировать:
1. По способу выделения Rk из полного сопротивления образца.
2. По геометрической форме измерительных образцов.
3. По роду используемого тока.
4. По схеме измерения.
1. Определение Яц по приращению полного сопротивления измерительного образца после формирования контактов.
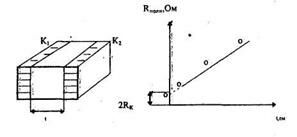
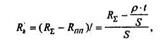
где
р - удельное сопротивление полупроводника, Ом • см;
t –толщина образца, см;
Rпп - сопротивление тела полупроводника, Ом. Удельное переходное сопротивление НК определяется как Rk, приведенное к единице площади:
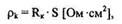
т.е. не зависит от размеров исследуемых контактов и используется для характеристики различных НК.
Rk можно найти по графику зависимости Кполн = f(t) экстраполяцией к точке t = 0.
2. Определение Rk к эпитаксиапьным слоям на низкоомной подложке
Образцы для исследования
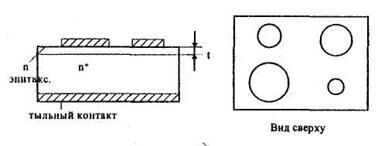
Для одного из контактов на эпитаксиальном слое:
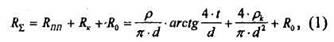
где d - диаметр контакта,
Ro - остаточное сопротивление (связанное с тыльным контактом).
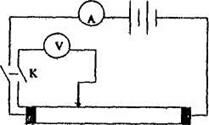
Если все контакты находятся с одной стороны пластины, используется так называемый "четырехзондовый метод".
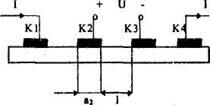
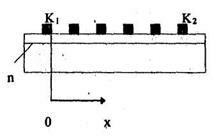
Через контакты К1 и К4 - пропускают постоянный ток и измеряют напряжение между К2 и К3 - U23.
Затем пропускают тот же ток через К2 и К4 и снова фиксируют U23. Оно будет превышать U23 на величину падения напряжения RкI на контакте К2.
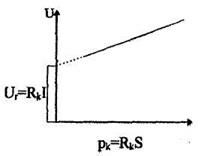
Связь между Rк и рк задается выражением:
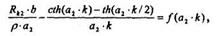
b - длина контактов,
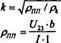
где l- расстояние между контактами К2 и К3.
Имеется график функции С(а • к)
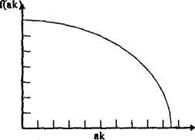
Найдя значение функции f(a • к), находим рК.
3. Определение Rk no распределению потенциалов вдоль образца.
Сущность метода состоит в том, что при прохождении тока по полупроводниковому образцу с металлическими контактами напряжение падает как на сопротивлении объема полупроводника, так и на Rk. Если снять зависимость потенциала на поверхности образца от расстояния до границы НК, то экстраполяцией этого графика к точке на границе контакта можно определить падение напряжения на контакте:
Для расчета характеристик тонкопленочных контактов металл-полупроводник необходимо знание работы выхода металла и полупроводника.
Либо для тонкопленочных контактов;
Либо по формуле:
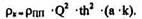
Значения Фm некоторых металлов.
| Металл | Фm | Металл | Фm | Металл | Фm | Металл | Фm |
| Al | 4.25 | V | 4.12 | Zr | 3.90 | Ru | 4.60 |
| Be | 3.92 | Сr | 4.58 | Nb | 3,99 | Pd | 4.80 |
| Ti | 3.95 | Ni | 4.50 | Mo | 4.30 | Ge | 2.70 |
| Та | 4.12 | W | 4.54 | Re | 5.00 |
Типичные значения высоты барьера Шотки для металлов составляют 0,65 - 0,75 эВ.
Степень легирования слоя полупроводника Nd - для n-типа и N, для p-типа влияет на механизм переноса носителей зарядов (электронов и дырок соответственно) в контакте. Различают следующие механизмы переноса носителей через контакт:
а) термоэлектронная эмиссия (перенос над энергетическим барьером);
б) полевая эмиссия (туннелирование) сквозь барьер;
в) термополевая эмиссия (перенос над барьером и туннелирование);
г) туннельно-рекомбинационный механизм.
Указанные механизмы переноса проиллюстрированы на нижеследующем рисунке.
Основные механизмы переноса носителей через контакт при наличии смещения UCM
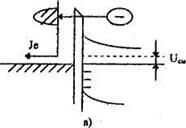
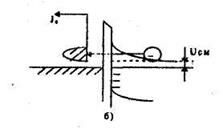
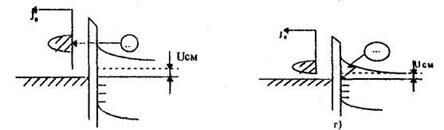
Определить механизм переноса зарядов можно при помощи критерия :
 , где
, где
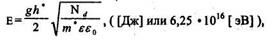
h* - h/2 , h - 6.6 • 10-34;
, h - 6.6 • 10-34;
m* -эффективная масса электрона, 4,55 • 10-31 кг;
m -масса электрона, m*= 0,5 т,
Тогда, если  >> 1, то основной механизм переноса носителей в контакте - термоэлектронная эмиссия ; если
>> 1, то основной механизм переноса носителей в контакте - термоэлектронная эмиссия ; если  << 1 - полевая эмиссия, если
<< 1 - полевая эмиссия, если  ~ 1 - тёрмополевая эмиссия.
~ 1 - тёрмополевая эмиссия.
Туннельно-рекомбинационный механизм встречается в особых типах контактов металл-полупроводник, где имеет место интенсивное взаимодействие материалов в технологическом процессе формирования контактов с образованием новых соединений и границ раздела.
Расчет характеристик контактов
1 .Если  >> 1, то
>> 1, то
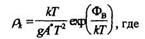
А*- эффективная постоянная Ричардсона (А•см-2•К-2), свободных электронов постоянная Ричардсона А*=120 А•см-2•К-2.
Для кремния p-типа А*/А=0,66.
Для кремния n-типа:
А*/А=2,2 в направлении движения электронов <111>;
А*/А=2,1 в направлении движения электронов <100>.
2. Если  << 1, то
<< 1, то
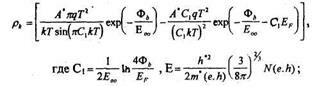
EF - энергия уровня Ферми;
е, h -индексы электронов и дырок (Nd ~Ne, Na ~NP).
3. Если  ~ 1,то
~ 1,то
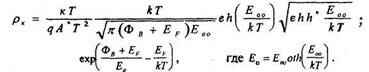
Нужно учесть, что последнее выражение для рк справедливо, если
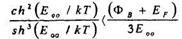
Расчет RK ведется применительно к омическим контактам к областям базы n-p-n -планарных транзисторов с Na =1018 -1019 см-3 и к областям эмиттеров (коллекторов) с Nd >1020 см-3.
Средняя площадь контактов Sk может быть выбрана из диапазона 1-8 мкм2.
Выбор металла контактов производится самостоятельно, исходя из технических условий или индивидуального задания.
Приложение
Таблица 1
Значения средних нормальных пробегов и стандартных отклонений
пробегов, выраженные в нанометрах, для ряда ионов с энергиями 20-
200 эВ в кремнии.
Таблица 2 Некоторые характерные точки кривой Гаусса
| Е,эВ | 11B+ | 27AI+ | 3lp+ | 75Sb+ | 12lSb+ |
| 20 Rp | 78 | 29 | 26 | 16 | 14 |
| | 32 | 11 | 9.4 | 3.7 | 2.4 |
| 40 Rp | 161 | 56 | 49 | 27 | 23 |
| | 54 | 19 | 16.4 | 6.2 | 3.8 |
| 60 Rp | 244 | 85 | 73 | 38 | 31 |
| | 71 | 27 | 23 | 8.4 | 5.1 |
| 80 Rp | 324 | 114 | 98 | 48 | 38 |
| | 84 | 35 | 30 | 10.5 | 6.3 |
| 100 Rp | 398 | 144 | 123 | 58 | 46 |
| | 94 | 42 | 35 | 12.5 | 7.4 |
| 120 Rp | 469 | 175 | 149 | 68 | 53 |
| | 102 | 48 | 41 | 14.5 | 8.4 |
| 140 Rp | 537 | 205 | 175 | 79 | 60 |
| | 110 | 54 | 47 | 16 | 9.5 |
| 160 Rp | 603 | 236 | 201 | 89 | 67 |
| | 116 | 60 | 52 | 18 | 10.5 |
| 180 Rp | 665 | 266 | 228 | 99 | 74 |
| | 121 | 60 | 57 | 20 | 11.5 |
| 200 Rp | 725 | 297 | 254 | 110 | 81 |
| | 126 | 70 | 61 | 22 | 12.5 |
Таблица 2
| Некоторые характерные точки | кривой Гаусса | ||||||||
|
| 0 | 0,833 | 1,52 | 2,14 | 2,63 | 3,04 | 3,39 | 3,71 | 4 |
|
| 1 | 0,5 | 0,1 | 0,01 | 10-3 | 10-4 | 10-5 | 10-6 | 10-7 |

Зависимость толщины пленки SiO2, выращенной
в атмосфере сухого кислорода, от времени для температур С°
1-700; 2-800; 3-900; 4-1000; 5-1100; 6-1200; 7-1300; 8-1400.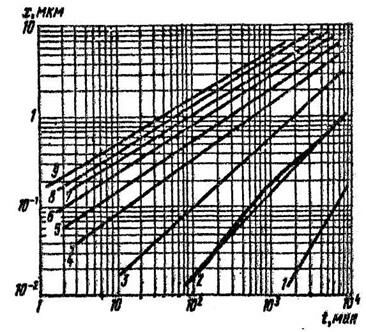
Зависимость толщины пленки SiO2, выращенной
В атмосфере водяного пара, от времени для температур С°:
1-600; 2-700; 3-800; 4-900; 5-1000; 6-1100; 7-1200; 8-1300;
9-1400.
Таблица З Значения erfc функции для различных а и г.
| ж / а | 0.1 | 0.3 | 0.5 | 1.0 | 2.0 | 3.0 | 5.0 |
| 0.1 | 0.09015 | 0.07376 | 0.06035 | 0.03655 | 0.01340 | 0.00491 | 0.00066 |
| 0.3 | 0.26295 | 0.21403 | 0.17422 | 0.10416 | 0.03725 | 0.01333 | 0.00174 |
| 0.5 | 0.41626 | 0.33557 | 0.27058 | 0.15812 | 0.05419 | 0.01866 | 0.00224 |
| 0.7 | 0.54464 | 0.43340 | 0.34515 | 0.19596 | 0.06398 | 0.02120 | 0.00242 |
| 0.9 | 0.64829 | 0.50812 | 0.39903 | 0.21979 | 0.06867 | 0.02213 | 0.00245 |
| 1.5 | 0.84509 | 0.63065 | 0.47586 | 0.24431 | 0.07141 | 0.02247 | 0.00246 |
| 3 | 0.99920 | Обратите внимание на лекцию "53 Цена и источники Победы". 0.68698 | 0.49825 | 0.24708 | 0.07147 | 0.02247 | 0.00246 |

 RP
RP