Влияние щелочи и примесных компонентов на процесс цианирования
Лекция 8. Влияние щелочи и примесных компонентов на процесс цианирования
Влияние щёлочи
Введение щелочи в состав цианистых растворов предотвращает гидролиз цианистых соединений с образованием и выделением летучей синильной кислоты, способствует снижению расхода цианида, осаждению вредных примесей (железо II), коагулирует мелкодисперсные частицы пульпы, что улучшает процесс сгущения. Однако концентрация щелочи выше оптимальной при цианировании приводит к снижению извлечения благородных металлов.
Цианиды в водных растворах диссоциируют с образованием синильной кислоты и гидроксильных ионов:
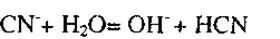
Гидролиз цианистых растворов приводит, во-первых, к значительной потере цианида, а во-вторых, к насыщению окружающего воздуха парами ядовитой синильной кислоты. При концентрациях цианида, применяемых на практике, степень гидролиза составляет 5... 10 %. В табл…. приведены данные по степени гидролиза растворов NaCN.
Как видно из табл…, даже при небольших концентрациях щелочи степень гидролиза резко уменьшается. При введении в процесс цианирования щелочи в виде извести разложение цианида значительно снижается. В последующих операциях сгущения и фильтрации остаточная щелочность повышает скорость осаждения твердой фазы пульпы.
Таблица 2.1
Рекомендуемые материалы
Степень гидролиза растворов NаСN
| Концентрация NаСN | Степень гидролиза, % (без СаО) | Степень гидролиза, %, при концентрации СаО в растворе, % (моль/л) | ||
| % | моль/л | 0,01 (1,78 • 10-3) | 0,05 (8,92 • 10-3) | |
| 0,5 | 10,20 ×10-2 | 1,1 | 0,32 | 0,07 |
| 0.2 | 4,08×10-2 | 1,7 | 0,34 | 0,07 |
| од | 2,04×10-2 | 2,5 | 0,35 | 0,07 |
| 0,05 | 1,02×10-2 | 3,5 | 0,35 | 0,07 |
| 0,02 | 0,408×10-2 | 5,4 | 0,35 | 0,07 |
| 0,01 | 0,204×10-2 | 7,6 | 0,35 | 0,07 |
| 0,005 | 0,102×10-2 | 10,5 | 0,35 | 0,07 |
| 0,002 | 0,041×10-2 | 16,1 | 0,35 | 0,07 |
Для защиты от гидролиза цианида содержание СаО должно быть не менее 0,025 %. Если в качестве щелочи используют гидроксид натрия, то присутствие в растворе 0,01 % NаОН защищает цианистые растворы от разложения вследствие гидролиза.
При значениях рН среды < 9,36 цианистый водород (синильная кислота) выделяется в атмосферу (улетучивается из жидкой фазы пульпы). На рис. 2.4 приведена зависимость содержания синильной кислоты (НCN) от рН среды.
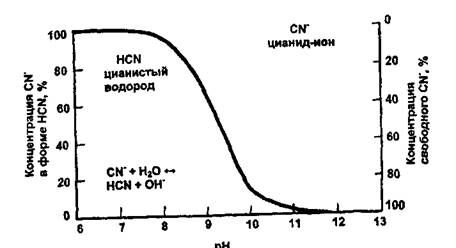
Рис. 2.4. Зависимость концентрации НСN и СN- от рН раствора
Снижение рН возможно при промывке пульп и аппаратов цианирования, при попадании углекислого газа, вызывающего нейтрализацию извести:
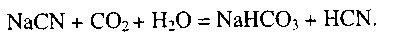
Синильная кислота может образовываться и в результате разложения п ри окислении цианатоводорода по реакциям:
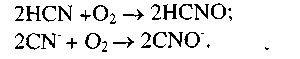
Цианат-ион образуется при наличии минералогических, бактериологических, фотохимических катализаторов:
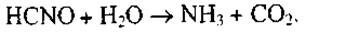
Однако повышение концентрации щелочи выше установленного минимума нецелесообразно по следующим обстоятельствам:
- снижается скорость растворения благородных металлов вследствие образования на его поверхности пленок;
- увеличивается взаимодействие с сопутствующими минеральными компонентами;
- возрастает расход восстановителя (цинка) при цементационном методе осаждения золота из раствора.
Влияние примесей
Минералы железа
Минералы железа, сопутствующие рудопроявлениям золота, ока зывают существенное влияние на процесс цианирования. Главная роль во взаимодействии с цианистыми растворами принадлежит продуктам окисления сульфидов железа. Как известно, окисление пирита и марказита начинается с первичной диссоциации с образованием сернистого железа и элементной серы с последующим гидролизом сульфида железа до сульфата железа. Элементная сера окисляется с образованием сернистой и серной кислот:
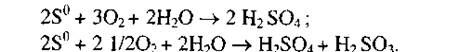
Сульфат железа (II) в дальнейшем окисляется до сульфата железа (Ш):
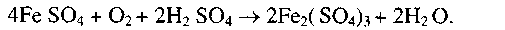
В дальнейшем образуется нерастворимый основной сульфат
2Fе2О3 • SО3, который затем переходит в гидроксид железа Fе(ОН)3.
Все отмеченные продукты окисления сульфидов железа присутствуют при длительном хранении минерального сырья в отвалах, лежалых хвостах и даже в самом месторождении.
При цианировании естественно возрастает расход кислорода на окисление пирита и пирротина. Образующиеся при окислении продукты взаимодействуют с цианидом:
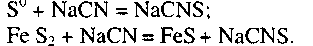
Роданистые соединения (тиоцианаты) образуются также при взаимодействии с сульфидной серой, тиосульфатом и другими продуктами окисления сульфидных минералов, присутствующих на поверхности и в жидкой фазе:
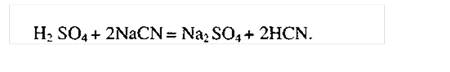
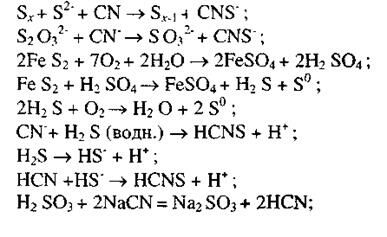
Присутствие в цианистых растворах отмеченных соединений определяется рН среды и окислительно-восстановительным состоянием жидкой фазы пульпы.
Сульфат и гидроксид железа в присутствии щелочи реагируют по уравнениям:
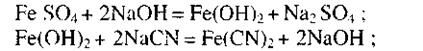
при избытке цианида:
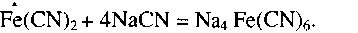
При недостатке щелочи возможно образование «берлинской лазури»:
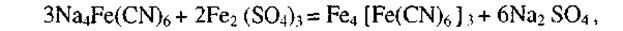
а это ведет к еще большему расходу цианида.
При избытке щелочи образуется сульфат кальция, который может отлагаться на поверхности металла:
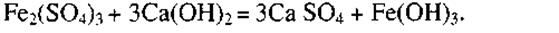
Поэтому перед цианированием соли железа необходимо перевести в нерастворимые соединения:
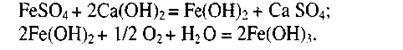
Минералы меди
Минералы меди, окисленные и сульфидные, также часто сопутствуют золоту; они обычно представлены халькозином, ковеллином, боратом, халькопиритом, блеклыми рудами, оксидами, гидроксидами, карбонатами, сульфатами, реже - хризоколлой и металлической медью.
Сульфиды меди взаимодействуют с цианистыми растворами, образуя растворимые соединения, увеличивают расход цианида и снижают извлечение золота. При этом образуются комплексные соединения:
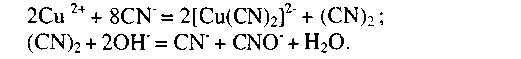
При избытке цианида возможны реакции:
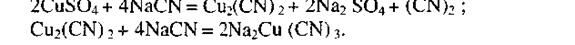
Карбонаты и гидроксиды меди в щелочных растворах цианида образуют следующие соединения:
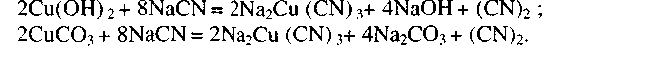
При взаимодействии с сульфидом меди возможно образование роданид-ионов и цианистой соли меди:
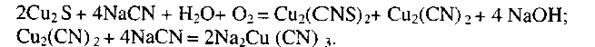
Образующиеся цианистые соединения, взаимодействуя, переходят
в роданистую медь по реакциям:
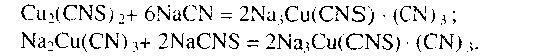
По реакционной способности по отношению к цианистым раствором медные минералы можно расположить в ряд: азурит > малахит > медь > халькозин > куприт > борнит> энаргит > тетраэдрит > хризоколла > халькопирит.
Медь всех этих минералов взаимодействует с цианидом с образованием одновалентного комплекса меди и дициана:
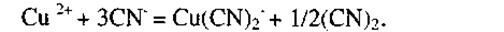
Окисленные минералы меди могут потреблять 1,5...2 кг СN- на 1 кг меди в руде с образованием в основном цианистого комплекса Сu(СN)32- . Сульфидные минералы потребляют значительно меньше цианида.
Минералы цинка
Сопутствующий золоту окисленный минерал цинка смитсонит ZnСО3 легко растворяется в цианистом растворе:

Окисленный с поверхности сфалерит взаимодействует с цианидом с образованием комплексного соединения цинка и роданистой соли, повышая при этом расход цианида. Простые сульфиды мышьяка и сурьмы растворяются в цианистых растворах с образованием сернистого натрия и поглощением из раствора значительной части кислорода. Цианирование такого минерального сырья ведут при пониженной щелочности пульпы.
Теллуриды золота
Теллуриды золота в цианистый раствор переходят труднее, чем металлическое золото, что связано с образованием пассивирующей пленки теллуровой кислоты. Цианирование проходит по реакции:
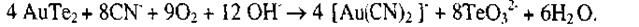
При недостатке кислорода:
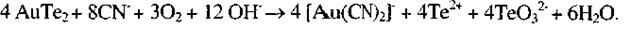
Соединения сурьмы и мышьяка
Сурьма и мышьяк не взаимодействуют с цианидом, однако при сутствующие в растворе соединения сурьмы и мышьяка образуют на поверхности золота тонкие, но очень прочные пленки, которые препятствуют взаимодействию цианида и кислорода с поверхностью металла.
К преимуществам технологии цианидного выщелачивания следует
"12 Отходы кожи и их переработка" - тут тоже много полезного для Вас.
отнести:
- высокую селективность процесса при небольших концентрациях цианида;
- неагрессивность среды, благодаря применению щелочных сред;
- простоту схем переработки;
- использование недефицитного и сравнительно дешевого реагента.
Однако высокая токсичность цианидов, необходимость применения специальных защитных мер предосторожности, невозможность эффективного использования применительно к упорному минеральному сырью вызывает необходимость разработки более экономичных и экологически чистых технологий переработки золотосодержащего сырья.





















