Цианирование химизм процесса
Лекция 7. Цианирование химизм процесса
Основным методом извлечения золота из упорных руд и концентратов, кеков выщелачивания является цианирование. Сущность этого метода заключается в выщелачивании (растворении) золота с помощью разбавленных растворов цианистых солей щелочных и щелочноземельных металлов в присутствии окислителя (кислород, перекисные соли, озон и т.д).
Физико-химические основы цианирования
Химия и кинетика процесса цианирования
Наибольший практический интерес представляет прочный цианидный комплекс [Au(CN)2]-, который образуется растворением металлического золота в водном растворе цианида, насыщенного кислородом воздуха.
Процесс цианирования золота идет по реакции:
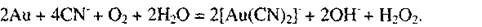
Константа нестойкости комплекса [Au(CN)2]- незначительна (1,1×10-41).
Рекомендуемые материалы
Окислительный потенциал золота весьма высок, а большинство окислителей имеют более отрицательные потенциалы, уступающие потенциалу золота. Так, кислород имеет потенциал:
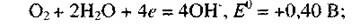
окислительные потенциалы кислорода при его восстановлении до пероксида водорода
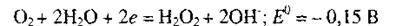
и пероксида водорода при его восстановлении до гидроксильных ионов
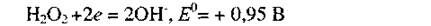
также недостаточны, чтобы окислить металлическое золото и перевести его в раствор.
Потенциал золота уменьшается, если снизить активность ионов золота в растворе, что достигается в процессе растворения золота в щелочных цианистых растворах.
Процесс растворения золота является электрохимическим:
- анодный процесс - переход металла в виде ионов в раствор с освобождением эквивалентного количества электронов
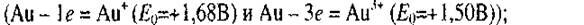
- катодный процесс - ассимиляция появившихся избыточных электронов каким-либо деполяризатором (восстановление окислителя).
Восстановление кислорода на катодных участках с образованием гидроксила идет в несколько стадий:
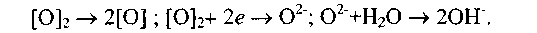
Возможны и другие стадии восстановления кислорода с образованием пероксида водорода:
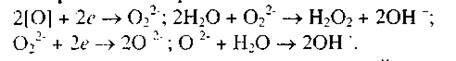
Восстановление кислорода - медленный процесс, но в присутствии серебра скорость реакции возрастает. Адсорбция кислорода на серебре с образованием оксидной пленки приводит к диссоциации молекулы кислорода: [O2] ® 2[O], что в дальнейшем ускоряет образование гидроксила. Скорость диффузии молекул кислорода или скорость восстановления кислорода на поверхности металла определяет кинетику процесса растворения золота.
Основная причина растворения золота (серебра) - образование комплексных ионов цианида с соответствующими высокими значениями свободной энергии, но для этого необходима диффузия ионов цианида к поверхности металла. Образующиеся на поверхности комплексные анионы золота затем переходят в раствор.
Кислород в процессе растворения золота может быть заменен другими окислителями, например пероксидом натрия и бария, озоном, бромистым цианидом. Кислород или другой окислитель необходим для ассимиляции избыточных электронов, накапливающихся в результате перехода в раствор ионов металла. Уменьшение концентрации кислорода или его отсутствие в растворе может прекратить процесс растворения металла, несмотря на достаточную концентрацию цианида.
Процесс цианирования - типично гетерогенный процесс, который проходит во всем объеме раствора. При этом должны соблюдаться условия подвода реагирующих веществ к частицам минералов и отвода от них продуктов реакции. Процесс растворения золота в цианистом растворе включает несколько стадий:
- адсорбция кислорода цианистым раствором;
- доставка ионов цианида и молекул кислорода из объема раствора к поверхности минерала (металла);
- химическая реакция на поверхности частицы минерала (металла);
- отвод продуктов растворения от поверхности в раствор.
Каждая из этих стадий определяет общую скорость процесса растворения золота в целом. Самая медленная стадия этого процесса -перенос реагента из объема раствора к поверхности твердых частиц
пульпы. Перенос частиц твердого вещества осуществляется, во-первых, в результате молекулярной диффузии за счет разности концентраций из области большей концентрации в область меньшей, во-, вторых, вследствие конвекции (движения) частицы растворенного вещества вместе с потоком жидкости. Эти два фактора обеспечивают конвективную диффузию.
Скорость молекулярной диффузии значительно ниже скорости переноса вещества за счет движения жидкости, и только при малой скорости движения жидкости основную роль играет молекулярная диффузия. В непосредственной близости от твердой частицы находится тонкий слой, в котором преобладающая доля вещества переносится молекулярной диффузией. Переносу вещества оказывает сопротивление не весь пограничный слой, а только небольшая его часть, называемая диффузионным слоем. Толщина его тем меньше, чем больше скорость движения жидкости относительно твердого тела и чем меньше коэффициент диффузии и вязкости раствора. Наиболее важна величина зависимости толщины диффузионного слоя от интенсивности перемешивания, т.е. от скорости движения жидкости относительно твердого тела.
Если скорость химической реакции во много раз больше скорости диффузии реагента, то ион или молекула реагента, оказавшийся у поверхности, быстро вступает в химическую реакцию. Концентрация ионов или молекул у поверхности частицы будет намного меньше, чем в объеме раствора. Характер распределения концентрации реагента вблизи поверхности частицы имеет вид, показанный на рис……
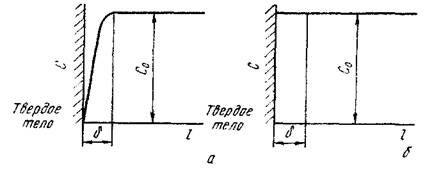
Рис… Распределение концентрации С реагента
на расстоянии l от поверхности твердого тела в диффузионном (а) и кинетическом (б) режимах
Скорость диффузии подчиняется уравнению:
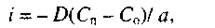
где i - скорость диффузии;
D - коэффициент диффузии;
Сп - концентрация реагента на поверхности тела;
С0- концентрация реагента в объеме раствора;
а - толщина диффузионного слоя.
Это уравнение показывает, что в диффузионной области скорость диффузии реагента к поверхности выщелачиваемого вещества и, следовательно, всего процесса выщелачивания возрастает с ростом интенсивности перемешивания (толщина диффузионного слоя уменьшается) и концентрации реагента.
Диффузия растворяемого вещества от поверхности твердого тела частицы в объем раствора также возрастает с увеличением интенсивности перемешивания. С повышением концентрации продукта реакции на границе твердое тело - жидкость скорость выщелачивания растет, достигая максимума при концентрации, соответствующей пределу растворимости. Диффузия продукта реакции в объем раствора обычно протекает достаточно быстро и не лимитирует скорость процесса выщелачивания.
Когда в процессе цианирования участвует кислород, необходимо учитывать особенности кинетики адсорбции его раствором. Адсорбцию кислорода раствором можно рассматривать как диффузионный процесс в тонкой пограничной пленке жидкости, соприкасающейся с газом. При насыщении газом жидкости на поверхности раздела жидкость - газ скорость адсорбции газа, отнесенная к единице поверхности твердой фазы, равна
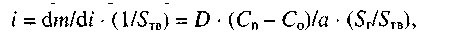
где i - скорость адсорбции газа, моль/(см2 ×с);
dm/di - количество газа, адсорбируемого в единицу времени, моль/с;
D - коэффициент диффузии газа в растворе см2/с;
Сп - концентрация газа в насыщенном растворе, моль/см3;
С0 - концентрация растворенного газа в объеме раствора, моль/см3;
а - толщина диффузионного слоя раствора у границы раствор - газ, см;
SГ- поверхность раздела раствор - газ, см2;
SТВ- поверхность твердой фазы, см2.
Адсорбция кислорода цианистым раствором обычно не лимитирует скорость выщелачивания, что достигается применением аэрирующих устройств, насыщающих раствор кислородом. Но процесс выщелачивания может лимитироваться скоростью химической реакции на поверхности твердого тела. Для химических реакций, протекающих на границе раздела фаз, количество прореагировавшего в единицу времени реагента и образовавшегося продукта реакции пропорционально поверхности раздела фаз. Скорость химической реакции может быть описана кинетическим уравнением и не зависит от условий перемешивания. Для практического выщелачивания важно знать, в каком режиме идет процесс: в кинетическом или диффузионном. Наиболее надежным критерием контроля скорости является установление оптимальных условий перемешивания. Увеличение скорости процесса с повышением интенсивности перемешивания свидетельствует о том, что растворение протекает в диффузионной области.
Наоборот, независимость скорости процесса от условий перемешивания указывает на кинетический режим. Другим критерием протекания в диффузионной или кинетической области может служить характер изменения скорости процесса от температуры. Скорость химической реакции растет с повышением температуры быстрее, чем скорость диффузии. Скорость диффузионного процесса также возрастает с температурой. Кинетический режим при низких температурах может превратиться в смешанный при более высоких температурах и затем перейти в диффузионный. При одной и той же температуре усиление перемешивания может привести к переходу процесса из диффузионной области в кинетическую.
Кинетику цианирования И.А. Каковский и Ю.Б. Холманский изучали с применением разработанной ими методики вращающегося диска. При этом исследовали влияние концентрации цианида, парциального давления кислорода над раствором, скорости вращения диска, температуры процесса и других факторов.
На рис… и … приведена зависимость скорости растворения золота от скорости вращения диска и парциального давления кислорода.
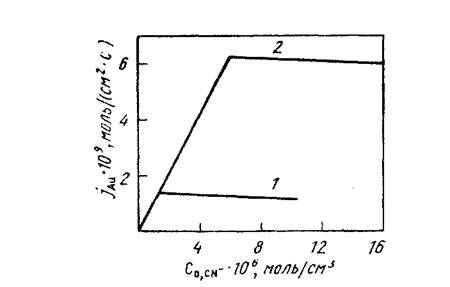
Рис. 2.2. Зависимость скорости растворения золота
от концентрации КСN (Т =25 °С, п = 100 об/мин)
при парциальном давлении кислорода, МПа:
1-0,021; 2-0,101
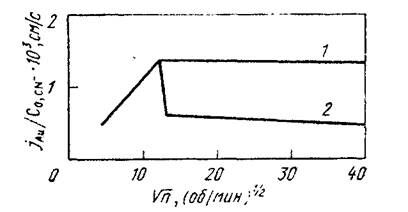
Рис. 2.3. Зависимость скорости растворения золота
от скорости вращения диска при Т = 25 °С
и парциальном давлении кислорода, МПа:
1 -0,021; 2 -0,101
При небольшой частоте вращения диска (до 150 об/мин) скорость растворения пропорциональна числу оборотов диска в степени 0,5. Золото растворяется в диффузионном режиме; при низких концентрациях цианида скорость процесса контролируется доставкой ионов СN-, а при высоких - молекул растворенного кислорода. Оптимальное соотношение концентраций цианида и кислорода, обеспечивающее максимальную скорость растворения при данной концентрации одною из реагентов, равно около 5. Как видно из рис. 2.3, прямолинейная зависимость между соотношением скорости растворения золота и концентрации цианида и скоростью вращения диска свойственна диффузионному режиму процесса лишь при скорости вращения < 150 об/мин. При более высокой частоте вращения диска скорость растворения золота не зависит от числа оборотов диска. Процесс растворения золота при высоких оборотах переходит в кинетический режим. Возрастание количества оборотов диска ведет даже к снижению скорости растворения (кривая 2, рис. 2.3), т.е. к пассивированию поверхности. Предполагается, что при интенсивном перемешивании молекулы кислорода, адсорбируясь на золоте, вытесняют с его поверхности ионы СN-, что тормозит растворение. При повышении концентрации цианида или введении в раствор поверхностно-активных веществ (спиртов, эфиров) снижается пассивация поверхности частиц золота за счет вытеснения молекул кислорода.
В реальных промышленных условиях процесс цианирования золота проходит со значительно большими осложнениями, чем при лабораторных исследованиях. Практика работы заводов и фабрик показывает, что в большинстве случаев растворение золота идет в диффузионном режиме. Используя интенсивное перемешивание, можно достичь значительного увеличения скорости растворения независимо от того, лимитируется ли процесс диффузией ионов СN- или диффузией молекул растворенного кислорода. Оптимальная концентрация свободного цианида составляет ~ 0,01 % NаCN; на практике применяют более крепкие растворы (0,02...0,05 % NаCN), что объясняется присутствием в минеральном сырье значительного количества примесей.
Сопутствующие минералы способны окисляться, потребляя часть растворенного кислорода. Снижение концентрации кислорода ниже равновесных значений неизбежно уменьшает скорость растворения золота. Концентрацию кислорода в пульпе поддерживают интенсивной аэрацией. Растворимость кислорода прямо пропорциональна его парциальному давлению над раствором; при повышенном давлении
кислорода должна быть и оптимальная концентрация цианида. Повышенное парциальное давление кислорода достигается использованием технического кислорода при атмосферном или повышенном давлении или сжатого воздуха. Оптимальный диапазон температур составляет 15...45 °С. Повышение температуры сравнительно слабо влияет на скорость растворения золота, но значительно ускоряет побочные реакции взаимодействия цианида с сопутствующими минералами. Кроме того, при повышенных температурах, усиливается гидролиз цианистых растворов. Крупность исходного материала и зерен золота влияют на скорость растворения.
Основное влияние на скорость цианирования оказывает диаметр частиц выщелачиваемой руды и их пористость. При пористой и рыхлой структуре цианированию можно подвергать материал достаточно грубого помола Доставка цианида и кислорода во внутреннюю диффузионную область к поверхности золотин проходит по трещинам и капиллярам. Скорость процесса в этом случае не зависит от интенсивности перемешивания, но определяется концентрацией цианида. Крупность и форма золотины также влияет на скорость цианирования.
Бесплатная лекция: "8 Статистический анализ и прогнозирование сезонных явлений" также доступна.
Вязкость пульп, определяемая соотношением кристаллических и коллоидных частиц и степенью разжижения пульпы, влияет на скорость растворения золота. Глинистые и охристые руды перед цианированием требуют повышенного разжижения и интенсивного длительного перемешивания. Однако необходимость разжижения пульпы связана с увеличением объема аппаратуры и повышением расхода реагентов, а наличие илов снижает эффективность операций сгущения, фильтрации и промывки. Поэтому для руд типа упорных необходимо применять наиболее интенсивные процессы.
Теллуриды золота также снижают скорость перевода золота в раствор. Для улучшения растворимости теллуридов необходимо применять более тонкое измельчение, при котором увеличивается поверхность растворяющихся частиц золота, а также повышать концентрацию щелочи.
кислорода должна быть и оптимальная концентрация цианида. Повышенное парциальное давление кислорода достигается использованием технического кислорода при атмосферном или повышенном давлении или сжатого воздуха. Оптимальный диапазон температур составляет 15...45 °С. Повышение температуры сравнительно слабо влияет на скорость растворения золота, но значительно ускоряет побочные реакции взаимодействия цианида с сопутствующими минералами. Кроме того, при повышенных температурах, усиливается гидролиз цианистых растворов. Крупность исходного материала и зерен золота влияют на скорость растворения.
Основное влияние на скорость цианирования оказывает диаметр частиц выщелачиваемой руды и их пористость. При пористой и рыхлой структуре цианированию можно подвергать материал достаточно грубого помола Доставка цианида и кислорода во внутреннюю диффузионную область к поверхности золотин проходит по трещинам и капиллярам. Скорость процесса в этом случае не зависит от интенсивности перемешивания, но определяется концентрацией цианида. Крупность и форма золотины также влияет на скорость цианирования.
Вязкость пульп, определяемая соотношением кристаллических и коллоидных частиц и степенью разжижения пульпы, влияет на скорость растворения золота. Глинистые и охристые руды перед цианированием требуют повышенного разжижения и интенсивного длительного перемешивания. Однако необходимость разжижения пульпы связана с увеличением объема аппаратуры и повышением расхода реагентов, а наличие илов снижает эффективность операций сгущения, фильтрации и промывки. Поэтому для руд типа упорных необходимо применять наиболее интенсивные процессы.
Теллуриды золота также снижают скорость перевода золота в раствор. Для улучшения растворимости теллуридов необходимо применять более тонкое измельчение, при котором увеличивается поверхность растворяющихся частиц золота, а также повышать концентрацию щелочи.





















