Полная и полезная разность температур
Лекция №14
Полная и полезная разность температур.
N - число корпусов
 =
= -
- – полная разность температур
– полная разность температур
 =
= -
- -
- -полезная разность температур
-полезная разность температур  =
= , где
, где  -движущая сила процесса переноса тепла в I корпусе, т.е.
-движущая сила процесса переноса тепла в I корпусе, т.е.  -
- -разность температур греющего пара .
-разность температур греющего пара .
Определение поверхности теплообмена корпусов:
 +
+ +
+ =
= -
-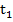
 =
= ;
; - коэффициент теплоотдачи от конденсирующегося пара к стене
- коэффициент теплоотдачи от конденсирующегося пара к стене
 =
=
 ;
;  =
= ;
;  =
= ;
; =
= ;
; =
= ,
, - коэффициент теплоотдачи от стенки к кипящей жидкости .Выражаем соответствующие разности температур и складываем их.
- коэффициент теплоотдачи от стенки к кипящей жидкости .Выражаем соответствующие разности температур и складываем их.
Рекомендуемые материалы
 =
= ;
;  =(
=(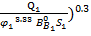
 =(
=( +
+ +(
+(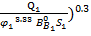 ;
; ;
;
 =
= +
+ +
+ =>f(S)=0 (1) Ищем S методами однопараметрической оптимизации. В частности, S можно определить графически:
=>f(S)=0 (1) Ищем S методами однопараметрической оптимизации. В частности, S можно определить графически:
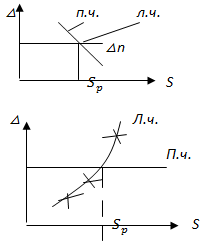
Где л.ч.- левая часть уравнения (1),п.ч. -правая часть уравнения (1)
Перенос массы
Вывод уравнения неразрывности для многокомпонентной среды.
Уравнение выводится из закона сохранения массы i компонента .Если процесс идет с химическим превращением, то появляется удельный источник (сток) массы i компонента 
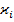 :
:
 [
[ dV]=
dV]= dV
dV
 +div(
+div( )=
)=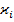
Пусть имеем n-компонентов:
 +div(Σ
+div(Σ )] =
)] = =>
=> – т.е. переходит в уравнение неразрывности для однокомпонентной среды.
– т.е. переходит в уравнение неразрывности для однокомпонентной среды.
 =0- по закону сохранения массы при химических превращениях.
=0- по закону сохранения массы при химических превращениях.
Введем скорость центра масс:
 ==
== =
= =>
=> =
= =
= ρ
ρ
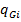 =
= - поток массы i компонента
- поток массы i компонента
 +div(
+div( )-div(
)-div( )+ div(
)+ div( )=
)= +div[
+div[ (
( + div(
+ div( )=
)= + div(
+ div( )+div
)+div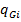 =
=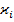 - уравнение неразрывности для i компонента.
- уравнение неразрывности для i компонента.
Суммируем уравнения неразрывности для всех компонентов:
 + div(
+ div( )+divΣ
)+divΣ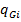 =Σ
=Σ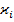
𝛴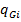 =
= -
- =0; Σ
=0; Σ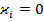
Получим:
 + div
+ div =0 –уравнение неразрывности для однокомпонентной среды
=0 –уравнение неразрывности для однокомпонентной среды
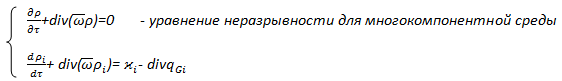
Вывод уравнения концентрации
 =
= =>
=> =
= – концентрация ( массовая или мольная). Тогда из уравнения неразрывности для многокомпонентной среды получаем:
– концентрация ( массовая или мольная). Тогда из уравнения неразрывности для многокомпонентной среды получаем:
ρ[ +
+ grad
grad ]+
]+ [
[ +div
+div ]=- div
]=- div =
= -div
-div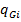
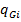 =[
=[ ]=
]=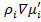
µ=f(T,P,U, )-химический потенциал. Это работа образования одного моля i-компонента.
)-химический потенциал. Это работа образования одного моля i-компонента.
 - поток химического потенциала i-компонента.
- поток химического потенциала i-компонента.
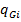 =ρ[
=ρ[ (
( )∇
)∇ +
+ (
( ) ∇
) ∇ +
+ (
( ) ∇
) ∇ +
+ ∇U+…]
∇U+…]
=ρ[ ∇
∇ +
+ ∇T+
∇T+ ∇P+
∇P+ ∇U]=ρ[∇
∇U]=ρ[∇ +
+ ∇T+
∇T+ ∇P+
∇P+ ∇U], где
∇U], где  - коэффициенты диффузии, термодиффузии, бародиффузии, электродиффузии ;
- коэффициенты диффузии, термодиффузии, бародиффузии, электродиффузии ; - термо, баро, электродифузиозные коэффициенты- результат нормирования соответствующих коэффициентов различных видов диффузии i компонента
- термо, баро, электродифузиозные коэффициенты- результат нормирования соответствующих коэффициентов различных видов диффузии i компонента 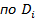
 =
= ;
;  =
= ;
; =
=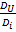
Выражение учитывает сумму потоков массы i компонента, вызванных изменением концентраций температур, давлений, электрических потенциалов и т.д.
ρ[ +
+ grad
grad ]= -ρdiv[
]= -ρdiv[ ∇
∇ +
+ ∇T+
∇T+ ∇P+
∇P+ ∇U]
∇U] -уравнение концентрации для i компонента
-уравнение концентрации для i компонента
 +
+ +
+ +
+ = -
= - [
[ +
+ +
+ ]
] - частный случай уравнения концентрации i компонента для изотропных условий и в пренебрежении другими видами диффузии в декартовой системе координат (уравнение Фика).
- частный случай уравнения концентрации i компонента для изотропных условий и в пренебрежении другими видами диффузии в декартовой системе координат (уравнение Фика).
В частном случае для стационарного диффузиозного (молекулярного) переноса массы имеем:
div(- grad
grad )=0
)=0
- grad
grad =const-закон Фика
=const-закон Фика
 =-
=- grad
grad -удельный объемный поток i компонента
-удельный объемный поток i компонента
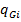 =-
=- grad
grad - удельный массовый поток i компонента
- удельный массовый поток i компонента
 =𝛽△
=𝛽△ = -
= - grad
grad =-
=- => 𝛽 =
=> 𝛽 = - коэффициент массоотдачи. Получен по аналогии с коэффициентом теплоотдачи. Удельный объемный поток i-го компонента.
- коэффициент массоотдачи. Получен по аналогии с коэффициентом теплоотдачи. Удельный объемный поток i-го компонента.
Теория подобия в процессах переноса массы.
 +
+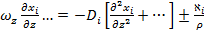
Введем безразмерные параметры:  , где xi0, ω0, z0-характерные параметры.
, где xi0, ω0, z0-характерные параметры.
 +
+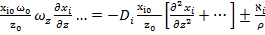
Нормируем комплексы характерных параметров при всех членах уравнения по комплексу параметров при диффузионном члене:
 +
+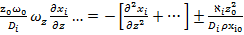
В лекции "Принципы выбора способа первичного вскрытия и свойств промывочной жидкости" также много полезной информации.
Foд= - диффузионный критерий Фурье (мера нестационарности процесса);
- диффузионный критерий Фурье (мера нестационарности процесса);
Peд= - диффузионный критерий Пекле (соотношение конвективного и диффузионного переноса массы) Peд=
- диффузионный критерий Пекле (соотношение конвективного и диффузионного переноса массы) Peд= =Re Prд, где Prд=
=Re Prд, где Prд= - диффузионный критерий Прандтля.
- диффузионный критерий Прандтля.
Po= - соотношение источника (стока) массы к диффузионному переносу. Дефузионный критерий Померанцева.
- соотношение источника (стока) массы к диффузионному переносу. Дефузионный критерий Померанцева.
 +…=-
+…=-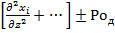
Из граничного условия аналогичного условию III рода в теплообмене получаем диффузионный критерий Био: Biд= .
.
β[xi(τ,0)-xi]= ; β
; β [xi(τ,0)-xi]=
[xi(τ,0)-xi]= ; Biд[xi(τ,0)-xi]=
; Biд[xi(τ,0)-xi]=