Классификация коррозии
Классификация коррозии
I. По механизму:
1. Электрохимическая коррозия- это коррозия металла в присутствии электропроводящей среды и протекающая через посредство электро-химических элементов самопроизвольно образующихся на поверхности металла.
2. Химическая коррозия – это коррозия вызванная непосредственным взаимодействием метала и агрессивной среды, причем среда в этом случае может и не являтся электролитом.
К химической относятся :
- газовая коррозия (в газовых средах, которые не содержат электролит )
- коррозия в р-рах неэлектролитах.
3. Комбинированная коррозия (одновременно протекающая химическая и электрохимическая)
Рекомендуемые материалы
4. Биологическая коррозия – это коррозия, которая возникает в результате жизнедеятельности какого либо рода бактерий.
Виды электрохимической коррозии:
- По условиям протекания делится:
А) коррозия в жидких средах (кислотная, щелочная, солевая, морская);
Б) коррозия в расплавах;
В) коррозия при полном, частичном, переменном погружении в среду;
Г) коррозия в перемешиваемом и не перемешиваемом электролите.
- Атмосферная коррозия:
А) коррозия в атмосфере воздуха (при наличии водяных паров);
Б) коррозия в присутствии паров электролитов.
- Грунтовая коррозия (почвенная).
- Контактная коррозия – коррозия вызванная тесным контактом между металлами, которые имеют разный потенциал.
- Структурная коррозия – коррозия вызванная неоднородностью структуры металла.
- Щелевая коррозия – возникает в резьбовых соединениях.
- Электрокоррозия – коррозия вызванная действием на металл токов рассеивания, либо под воздействием наведенного электрического поля.
- Коррозия внешним током.
Виды комбинированной коррозии:
1) коррозия под напряжением (механическим);
2) коррозия при трении (эрозийная коррозия):
3) кавитационная коррозия (появляется в результате взаимодействия среды).
II. Виды коррозий по характеру:
1. Сплошная коррозия:
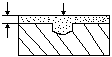
А. равномерная;
Б. неравномерная (характерна для сплавов и металлов с неупорядоченной структурой).
2. Селективная коррозия (характерна для сплавов и металлов с неупорядоченной структурой).

3. Язвенная коррозия – образуются очень широкие щели. Характерна для черных металлов (глубина разрушений превышает их протяженность).
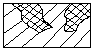
4. Питтинговая коррозия. Характерна для трубопровода который находится в земле.
5. Пятнистая коррозия – большая площадь очагов и их малая глубина.
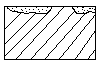
6. Подповерхностная коррозия – очаг разрушения находится под поверхностью металла, что приводит к вспучиванию и расслоению металла.
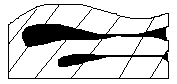
7. Межкристаллитная (наиболее опасный вид коррозии). Характерна для сплавов с высокой степенью неоднородности;коррозия происходит по границам зерен кристаллов.
Механизм электрохимической коррозии.
При погружении металла в электролит в результате взаимодействия между ними возникает разность потенциалов (электрических), что связано с образованием двойного эл. слоя.
Двойной эл. слой представляет собой не симметричное распределение заряженных частиц у границы раздела фаз.
Причинами этого распределения являются:
1) Переход катионов из металлов в электролит.
2) Переход катионов из растворов в металл.

3) Селективная адсорбция ионов на поверхности металлов

4) За счет адсорбции на поверхности металла полярных молекул.

5) Одновременный переход катионов из раствора в металл и наоборот. В этом случае возникает наибольшая скорость коррозии.

Переход катионов металла в р-р может быть описан следующим уравнением:
 Me+mH2O I Men+ * mH2O + ne
Me+mH2O I Men+ * mH2O + ne
(анодный процесс). Он сопровождается током I.
Обратный ему катодный процесс:
Men+ * mH2O + ne I Me+mH2O ,
Также сопровождается током I, но в обратную сторону
Направление тока зависит от потенциальной энергии катионов в узлах кристаллической решетки метала и в растворе.
Если потенциальная энергия катионов в узлах кристаллической решетки метала больше чем в растворе, тогда ток носит прямой характер и называется анодный.
Пме >Пр I> I
Если потенциальная энергия катионов в узлах кристаллической решетки метала меньше чем в растворе, тогда ток носит обратный характер и называется катодный.
Пме < Пр I < I Iк=I –I
Когда потенциальная энергия катионов в узлах кристаллической решетки метала и в р-ре равны, тогда существует так называемый ток обмена.
Iобм=I –I=10-8 - 10-5 А/см2
Абсолютное значение величины этого тока определить невозможно.
Стандартный водородный электрод – платиновая пластина определенного сечения опущена в раствор соляной кислоты.
Коррозионный элемент – это тот же самый гальванический, но только замкнутый.
| Li -3.01V Fe -0.44V |
| Cu +0.34V Pt +4V |
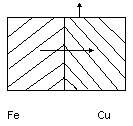
-0,44-0,34=-0,78 , все зависит от концентрации ионов водорода в растворе.
На скорость коррозии влияет:
1. концентрация ионов водорода или рН-среды;
Zn – стоек в нейтральных и щелочных средах,
Pb – стоек в слабокислых, нейтральных и щелочных редах,
Pt – стойкая в кислых, нейтральных и слабощелочных, но не стойкая в сильнощелочных средах.
2. концентрация электролита;
3. состав электролита;
В лекции "4.1 Экономическое развитие" также много полезной информации.
4. наличие растворенного кислорода. Чем больше содержание кислорода, тем больше скорость коррозии электроотрицательных элементов;
5. качество обработки поверхности;
6. наличие механических напряжений в материале;
7. скорость перемешивания электролита или скорость течения электролита;
8. наличие примеси в металле;
9. температура.




















