Препараты сложных эфиров азотной кислоты
Препараты сложных эфиров азотной кислоты
Препараты:
Nitroglycerinum. Нитриглицерин
Описание: бесцветное, бледно-желтое масло, тяжелая вязкая жидкость. Растворим в спирте, органических растворителях, мало растворим в воде.
Получение: пропусканием глицерина через нитрующую (HNO3к + H2SO4к) смесь при 12оС.
Лекарственные формы:
1. Concentratum Nitroglycerini 1% pro infusionibus
2. Tabulettae Nitroglycerini 0,0005
3. Solutio Nitroglycerini 1% oleosa in capsullis 0,0005 et 0,001
4. Инъекционные формы: Perlinganit, Nitro-pol, Nitro-mak.
5. Мази, пленки
6. Аэрозоли – Nitrolingual spray
Рекомендуемые материалы
8. Полимерные таблетки из микрокапсул – Sustac, Nitrolong
Подлинность:
1. Гидролиз с последующей идентификацией глицерина
С3H5(NO2)3 + 3KOH à C3H5(OH)3 + 3KNO3
C3H5(OH)3 + H2SO4 à CH2=CH-CHO (запах акролеина) + 2H2O
2. Синее окрашивание с дифениламином
RONO2 + 


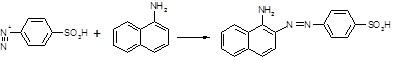
Примеси: частные специфические – этиленгликоля динитрат (ТСХ)
Количественное определение:
1.Обратная алкалиметрия:
НГ + 5KOH  CH3COOK + HCOOH + KNO3 + 2KNO2 + 3H2O
CH3COOK + HCOOH + KNO3 + 2KNO2 + 3H2O
Избыток КОН оттитровывают HCl с индикатором крезоловым красным или бромкрезоловым пурпурным.
f=1/5; 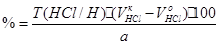
2. Фотоколориметрия:
Нитроглицерин  Глицерин + 3HNO3
Глицерин + 3HNO3
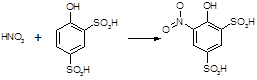
 желтая окраска
желтая окраска
Измеряют D при 408-410 нм, результаты сравнивают с KNO3 по графику.
3. Спектрофотометрия
4. Со сплавом Деварда (Cu-50%, Al-45%,Zn-5%):
Нитроглицерин + NaOH à Глицерин + 3NaNO3
NaNO3 + 4Zn + NaOH à NH3 + Na2ZnO2 + H2O
2NH3 + H2SO4 изб à (NH4)2SO4
избыток H2SO4 оттитровываем щелочью с метиленовым красным. f=1/3. Контроль.
Препараты карбоновых кислот и их солей
RCOOH(Me, R’) – увеличение растворимости, уменьшение токсичности, Н обеспечивает раздражающее действие и антимикробную активность.
Получение: 1. Окислением спиртов 2. Из галогенпроизводных УВ.
Физические свойства: от подвижной жидкости через вязкие до твердых веществ
Растворимость: падает с увеличением Mr, в спирте хор. растворимы, для солей – наоборот.
Химические свойства:
1. Кислотность: Ка = 10-4-10-5. Способны образовывать соли с Ме, оксидами Ме, растворами едких щелочей, гидроксидами Ме, карбонатами Ме. Соли подвергаются гидролизу – рН>7.
2. Образуют комплексные соединения с солями тяжелых Ме – Fe(III), Cu(II).
3. Вступают в реакции этерификации
Препараты:
Kalii acetas. Калия ацетат. CH3COOK
Описание: Белый, кристаллический порошок со слабым запахом уксусной кислоты, гигроскопичен, на воздухе расплываются.
Растворимость: ОЛР в воде, ЛР в спирте.
Подлинность:
CH3COO- + C2H5OH  CH3COOC2H5 Запах
CH3COOC2H5 Запах
7CH3COO- + 3FeCl3  2(CH3COO)3Fe•Fe(OH)2(CH3COO) + 7Cl- + 2HCl красный цвет.
2(CH3COO)3Fe•Fe(OH)2(CH3COO) + 7Cl- + 2HCl красный цвет.
Чистота: допускаются общие примеси, OH-, недопустима примесь восст-щих веществ.
Количественное определение:
1. Неводное титрование в ледяной уксусной кислоте. Титрант – раствор HClO4 в ледяной уксусной, индикатор – кристаллический фиолетовый.
HClO4 + CH3COOH « ClO4- + CH3COOH2+
CH3COOK « CH3COO- + K+
CH3COO- + CH3COOH2+ à 2CH3COOH
K+ + ClO4-« KClO4
f=1; 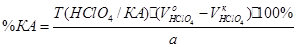
2. Нефармакопейный метод: прямая ацидиметрия с индикатором треополином 00:
CH3COOK + 0,1M HCl à CH3COOH + KCl
До перехода окраски из желтой в красноватую, рТ инд. = 1,3 – 3,2
f=1; 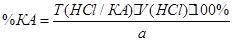
3. Ионообменная хроматография.
Хранение: хорошо укупоренная тара, предохраняет от попадания воды.
Применение: как диуретическое средство; при гипокалемии.
Calcii lactas. Кальция пропионат-2-ол пентагидрат. (CH3-CHOH-COO)2Ca•5H2O
Описание: белый аморфный порошок почти без запаха, на воздухе выветривается
Растворимость: медленно растворим в воде, легко растворим в горячей воде, практически нерастворим в 95% спирте.
Получение: окисление глюкозы в присутствии солей кальция.
Подлинность: ИК-спектроскопия – характерные пики на группы COO- и OH. Реакция А на ион кальция.
На лактат-ион: к раствору препарата прибавляют H2SO4 и KMnO4 до малиново-фиолетовой окраски, окраска исчезает, запах уксусного ангидрида:
(CH3-CHOH-COO)2Ca + 4KMnO4 + 11H2SO4  10CH3CHO + 2K2SO4 + 4MnSO4+10CO2+5CaSO4+ 16H2O
10CH3CHO + 2K2SO4 + 4MnSO4+10CO2+5CaSO4+ 16H2O
Нефармакопейные:
Ацетальдегид в прис. нитропруссида Na дает синюю окраску.
С реактивом Несслера – темно-бурый осадок.
Йодоформная проба
Чистота: прозрачность и цветность в сравнении с эталонами, щелочность и кислотность (ФФ + NaOH).
Наличие летучих и жирных кислот (при нагревании с H2SO4 не д. б. запаха жирных кислот).
общие – Cl-, SO42-; частные – Ba, Mg, щелочные Me; микробиологическая чистота; потеря в массе при выслушивании 20-30%
Количественное определение: прямая комплексонометрия с аммиачным буфером, индикатор– кислотный хром темно-синий, f=M, расчет производится на безводный препарат.
Хранение: хорошо укупоренная тара
Применение: источник кальция, антиаллергическое средство.
Calcii gluconas. Кальция глюконат
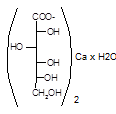
Описание: белый зернистый или кристаллический порошок без запаха и вкуса
Растворимость: умеренно медленно растворим в холодной воде, легко растворим в горячей с образованием мутного раствора, практически нерастворим в спирте и эфире.
Получение: окисление глюкозы в присутствии CaBr2, CaCl2
Подлинность: ИКС, характерные реакции на кальций; при добавлении к раствору препарата хлорида окисного железа появляется светло-зеленое окрашивание.
Чистота: Прозрачность в сравнении с эталоном, рН 6-7, галогены – Cl-, Br-, SO42-, тяж. Ме – допустимы, потеря в массе при высушивании – 1%.
Специфические – декстрин, сахароза. Препарат растворяют при нагревании в смеси из 2 мл разведенной соляной кислоты и 10 мл воды и кипятят 2 минуты. К охлажденному раствору приливают постепенно 8 мл раствора карбоната натрия и через 5 минут фильтруют (CaCO3). 5 мл фильтрата кипятят в течение 1 минуты с 2 мл реактива Фелинга; не должно наблюдаться образование красного осадка
Количественное определение: прямая комплексонометрия. Расчет на кристаллогидрат.
Хранение: сухое место
Применение: источник кальция, антиаллергическое средство.
Natrii citras pro injectionibus. Натрия цитрат для инъекций
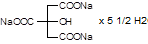
Описание: белые кристаллы или кристаллический порошок без запаха, выветривающиеся на воздухе
Растворимость: легко – в воде, практически нерастворим в спирте
Получение: взаимодействие лимонной кислоты с карбонатом Nа. Полученную соль перекристаллизовывают из спирта.
Подлинность: ИКС, реакция А на цитраты (с хлоридом кальция):
2 + 3CaCl2
+ 3CaCl2  (
( )2Ca3 + 6NaCl
)2Ca3 + 6NaCl
Осадок растворим в HCl.
Реакции на Na.
Нефармакопейные:
1. Реакция Б на цитраты: при нагревании цитрата с уксусным ангидридом через 20-40 секунд развивается карминово-красное окрашивание
2. Реакция Штаре:

 CO2 + HOOC-CH2-CO-CH2-COOH
CO2 + HOOC-CH2-CO-CH2-COOH  2CO2 + 5HBr + Br2CH-CO-CHBr2
2CO2 + 5HBr + Br2CH-CO-CHBr2
Выпадает белый кристаллический осадок.
3. С реактивом Денеже: свежеприготовленный раствор основного сульфата ртути.
 + KMnO4
+ KMnO4 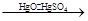
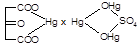
Чистота: раствор должен быть прозрачным и бесцветным; рН 7,8-8,3; недопустимы As (III), допустимы общие.
Специфические: тартраты – насыщенный раствор + ацетатный буфер – раствор должен быть прозрачен.
Оксалаты: навеску растворяют в воде, прибавляют HCl, спирт и CaCl2, оставляют на час, раствор должен остаться прозрачным.
Потеря в массе при выслушивании – 25-28%, микробиологическая чистота
Количественное определение: неводное титрование
1. HClO4 + CH3COOH « ClO4- + CH3COOH2+
2. натрия цитрат + 3CH3COOH « 3Na+ + 3CH3COO- + лимонная кислота
3. CH3COO- + CH3COOH2+ à 2CH3COOH
4. Na+ + ClO4-« NaClO4
f=1/3
ГФX: ионобменная хроматография
Цитарт натрия + [катионит]Н+ à [катионит]3Na+ + лимонная кислота.
Титруют NaOH с фенолфталеином. f=1/3.
Нефармакопейные:
1. Прямая ацидиметрия:
натрия цитрат + 3HCl  3 NaCl + лимоннам кислота.
3 NaCl + лимоннам кислота.
f=1/3
2. Обратная аргентометрия:
натрия цитрат + 3AgNO3  цитрат серебра¯ + 3NaOH
цитрат серебра¯ + 3NaOH
Избыток нитрата серебра оттитровывают роданометрически (NH4SCN) .f=1/3
3. Образование комплекса с медью – прямая куприметрия (CuSO4) с мурексидом.
Хранение: сухое прохладное место
Применение: консервант препаратов крови.
Natrii oxybutyras. Натрия оксибутират. HO-CH2-CH2-CH2-COONa
Описание: белый с желтоватым оттенком гигроскопичный порошок. ЛР в воде, Р в спирте, ПНР в эфире, хлороформе.
Получение: из g-бутиролактона (специфическая примесь)
Подлинность: ИКС, Б – на Na; лактона – гидроксамовая проба
Количественное определение: неводное титрование f=1; прямая ацидиметрия f=1.
Люди также интересуются этой лекцией: 5 Суждение и норма.
Хранение: список Б, в сухом, защищенном от света месте.
Применение: снотворное, неингаляционный наркоз, порошки, ампулы, сиропы, концентрат (66,7%).
Lithii oxybutyras. HO-CH2-CH2-CH2-COOLi
Подлинность: окрашивает пламя в фиолетовый цвет, рефрактометрия.
Количественное определение: неводное титрование.
Хранение: список Б
Применение: в психиатрии.




















