Производство титана
2.5. Производство титана
Титан как элемент открыт в 1791 г. Его промышленное производство началось в 50-х годах XX века и получило быстрое развитие. Титановые сплавы имеют наиболее высокую удельную прочность среди всех металлических материалов, а также высокую жаропрочность и коррозионную стойкость и находят все более широкое применение в авиационной технике, химическом машиностроении и других областях техники. Титан используют для легирования сталей. Двуокись титана TiO2 используют для производства титановых белил и эмалей; карбид титана TiC — для особо твердых инструментальных сплавов.
Титан по распространению в природе занимает четвертое место среди металлов и входит в состав более чем 70 минералов. К основным промышленным титаносодержащим минералам относятся рутил (более 90% ТiO2) и ильменит TiO2-FeO (60%TiO2). Ильменит входит в состав титаномагнетитов — его смеси с магнитным железняком; они содержат до 20% ТiO2. К перспективным рудам относятся сфен CaO-SiO2-TiO2 (32—42% TiO 2) и перовскит СаО- TiO (60% ТiO 2).
Сырьем для получения титана являются титаномагнетитовые руды, из которых выделяют ильменитовый концентрат, содержащий 40 ... 45 % ТiO2, -30 % FеО, 20 % Fе2О3 и 5 ... 7 % пустой породы. Название этот концентрат получил по наличию в нем минерала ильменита FеО-ТiO2.
Ильменитовый концентрат плавят в смеси с древесным углем, антрацитом, где оксиды железа и титана восстанавливаются. Образующееся железо науглероживается, и получается чугун, а низшие оксиды титана переходят в шлак. Чугун и шлак — разливают отдельно в изложницы. Основной продукт этого процесса - титановый шлак - содержит 80 ... 90 % ТiO 2, 2 ... 5 % FеО и примеси SiO2, А12О3, СаО и др. Побочный продукт этого процесса - чугун — используют в металлургическом производстве.
Полученный титановый шлак подвергают хлорированию в специальных печах. В нижней части печи располагают угольную насадку, нагревающуюся при пропус-кании через нее электрического тока. В печь подают брикеты титанового шлака, а через фурмы внутрь печи - хлор. При температуре 800 ... 1250 °С в присутствии углерода образуется четыреххлористый титан, а также хлориды СаС12> МgС12 и др.:
ТiO2 + 2С + 2С12 = ТiСl + 2СО.
Четыреххлористый титан отделяется и очищается от остальных хлоридов благодаря различию температуры кипения этих хлоридов методом ректификации в специальиых установках.
Рекомендуемые материалы
Титан из четыреххлористого титана восстанавливают в реакторах при температуре 950 ... 1000 °С. В реактор загружают чушковый магний; после откачки воздуха и заполнения полости реактора аргоном внутрь его подают парообразный четыреххлористый титан. Между жидким магнием и четыреххлористым титаном происходит реакция
ТiС12 = Тi + 2МgС12.
Производство титана является технически сложным процессом. Двуокись титана TiO2 — химически прочное соединение. Металлический титан (tПЛ = 1725 °С), обладает большой активностью. Он бурно реагирует с азотом при температуре 500—600 °С и кислородом воздуха при 1200—1300 °С, поглощает водород, взаимодействует с углеродом и т. д. Наиболее широкое распространение получил магниетермический способ, осуществляемый по следующей технологической схеме: титановая руда ® обогащение ® плавка на титановый шлак ® получение четыреххлористого титана TiCl4 ® восстановление титана магнием.
Обогащение титановых руд. Титаномагнетиты и другие бедные руды обогащают электромагнитным и другими способами, получая концентрат, содержащий до 50 % TiO2 и около 35 % Fe2O3 и FeO.
Плавку на титановый шлак проводят в электродуговой печи. Шихтой служат прессованные брикеты, состоящие из мелкоизмельченного концентрата, антрацита или угля и связующего (сульфитный щелок). В результате плавки получают богатый титановый шлак, содержащий до 80 % TiO2. Побочным продуктом является чугун, содержащий до 0,5 % Ti. Измельченный шлак подвергают магнитной сепарации (для удаления железосодержащих частиц), смешивают с мелким нефтяным коксом и связующим и спрессовывают в брикеты. После обжига при 700—800 °С брикеты направляют на хлорирование.
Получение четыреххлористого титана TiCl4 в герметизированных электрических печах представлено на рис. 2.9.

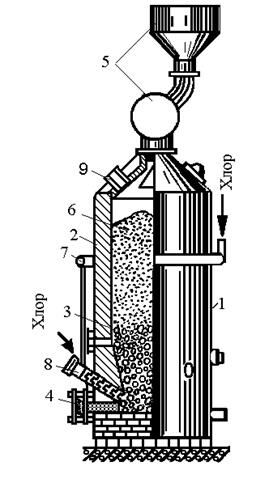
Нижнюю часть печи заполняют угольной (графитовой) насадкой, которая служит электрическим сопротивлением и нагревается при пропускании электрического тока. В реакционной зоне печи выше уровня угольной насадки развивается температура 800…850 °С. При хлорировании образуется четыреххлористый титан по реакции TiO2+2C-T2Cl2=TiCl4+2CO. Пары четыреххлористого титана находятся в паро-газовой смеси, содержащей SiCl4 и другие хлориды; СО, С12 и другие газы.
Ее очищают от твердых частиц и охлаждают в конденсаторах, в результате чего получают жидкий четыреххлористый титан. Для более полной очистки от твердых частиц конденсат отстаивают и фильтруют.
Четыреххлористый титан отделяют от других хлоридов путем ректификации конденсата, основанной на различии температур кипения различных хлоридов. Жидкий четыреххлористый титан направляют на восстановление.
В настоящее время для получения четыреххлористого титана начинают применять другие способы хлорирования: в хлоратоpax непрерывного действия, в солевом расплаве; перспективным является хлорирование в кипящем слое.
Восстановление титана магнием из TiCl4 проводят в герметичных реакторах (ретортах) из нержавеющей стали, установленных в электрических печах сопротивления. После установки в печь из реторты откачивают воздух и заполняют ее очищенным аргоном; после нагрева до температуры 700° С заливают расплавленный магний и начинают подачу жидкого TiCl4. Титан восстанавливается магнием по реакции TiCl4+2Mg=Ti+2MgCl2. Эта реакция сопровождается выделением большого количества тепла и в реакторе поддерживается необходимая температура 800…900 °С без дополнительного нагрева за счет регулирования скорости подачи TiCl4. Частицы восстановленного титана спекаются в пористую массу (титановая губка), пропитанную магнием и хлористым магнием. Расплав хлористого магния периодически удаляют через патрубок в дне реактора. В промышленных реакторах (емкостью до 2 т) получают титановую губку, содержащую до 60% Ti, 30 °/o Mg и 10 % MgCl2.
Рафинирование титановой губки производят методом вакуумной дистилляции. Крышку охладившейся реторты снимают и вместо нее устанавливают водоохлаждаемый конденсатор; затем реторту снова устанавливают в печь. Дистилляция проводится при 950…1000 °С и вакууме около 10-3 мм рт. ст. Примеси титановой губки Mg и MgCl2 расплавляются, частично испаряются и затем выделяются в конденсаторах. Получаемый оборотный магний возвращается в производство, MgCl2 используют для производства магния.
Получение титановых слитков. Титановые слитки получают переплавкой титановой губки в вакуумных электрических дуговых печах. Расходуемый электрод изготавливают прессованием из измельченной титановой губки. Электрическая дуга горит между расходуемым электродом и ванной расплавленного металла, постепенно заполняющего изложницу, затвердевающего и образующего слиток.
Наличие вакуума предохраняет металл от окисления и способствует его очистке от поглощенных газов и примесей.
Для получения слитков может быть использована дробленая титановая губка, загружаемая в печь дозатором. В этом случае дуга горит между расплавленным металлом и графитовым электродом, поднимаемым по мере заполнения изложницы металлом.
4 Предмет и метод корпоративного права - лекция, которая пользуется популярностью у тех, кто читал эту лекцию.
Для обеспечения высокого качества слитков плавку повторяют два раза. При второй плавке расходуемым электродом служит слиток, полученный при первой плавке.
Титановые сплавы выплавляют в электрических дуговых вакуумных печах, аналогичных применяемым для переплавки титановой губки. В качестве шихтовых материалов используют титановую губку и легирующие элементы в соответствии с заданным химическим составом сплава. Из шихты прессованием при 280….330 °С изготавливают переплавляемый (расходуемый) электрод. Плавку ведут в вакууме или в атмосфере аргона. Перед началом плавки на поддон в качестве затравки насыпают слой стружки из сплава такого же состава. Для более равномерного распределения легирующих элементов в сплаве полученный слиток переплавляют вторично.
Натриетермический способ получения титана отличается от магниетермического тем, что титан из TiCl4 восстанавливают металлическим натрием. Этот процесс проводят при относительно невысокой температуре, и титан в меньшей степени загрязняется примесями. Вместе с тем натриетермический способ технически более сложен.
Кальциееидридный способ основан на том, что при взаимодействии двуокиси титана TiO2 с гидридом кальция СаН2 образуется гидрид титана ТiH2, из которого затем выделяется металлический титан. Недостаток этого способа состоит в том, что получаемый титан сильно загрязнен примесями.
Иодидный способ применяют для получения небольших количеств титана очень высокой чистоты, до 99,99%. Он основан на реакции Ti+2I2 « TiI4, которая при 100 …200 °С идет слева направо (образование Til4), при 1300…1400 °С —в обратном направлении (разложение ТiI4).
Рафинируемую титановую губку помещают в реторту и нагревают до 100…200 °С; внутрь реторты вводят и разбивают ампулу с йодом, взаимодействующим с титаном по реакции Ti+2I2 ® TiI4. Разложение TiI4 ® Ti+2I2 и выделение титана происходит на титановых проволоках, натянутых в реторте, нагретых до 1300… 1400 °С пропусканием тока.



















