Физико-химические основы азотнокислотного разложения фосфоритов
Лекция №7
Физико-химические основы азотнокислотного разложения фосфоритов
Разложение фосфоритов азотной кислотой протекают по основным и побочным реакциям:
Са5F(PO4 )3 +10HNO3 = 3H3PO4+ 5Ca(NO3)2+ HF
(Са,Мg)CO3+ HNO3= Ca,Mg(NO3)2+ CO2+H2O
M2O3+ 6HNO3= 2M(NO3)3+ 3H2O (AI, Fe – М)
CaF2+ 2HNO3= Ca(NO3)2+ 2HF
FeO+ 3HNO3= Fe(NO3)3+ NO2+2H2O
Рекомендуемые материалы
6HF+ SiO2→H2SiF6+ 2H2O
4HF+ SiO2→SiF4+2H2O
SiF4+2HF→H2SiF6
Al2O3+H3PO4=2AlPO4+3H2O
Fe2O3+2H2PO4=2FePО4+3H2O
Содержащийся в исходном апатитовом концентрате нефелин и эгирин также разлагаются азотной кислотой.
1) нефелин
KAlSiO4 ∙ 4NaAlSiO4∙ nSiO2+ 20HNO3= KNO3+4NaNO3+5Al(NO3)3+nSiO2+10H2O
2) эгирин
Na2OFe2O3∙ 4SiO2+8HNO3=2NaNO3+2Fe(NO3)3+4SiO2+4H2O.
Факторы, влияющие на процесс.
1. С повышением температуры скорость процесса увеличивается оптимальная температура 500С, выше этой температуры резко усиливается коррозия аппаратуры. Температура поддерживается за счет теплового эффекта реакции.
К (раз) =96-99%
2) норма HNO3 рассчитанная на СаО и MgO принимается от стехиометрии
N =110-150%
3) концентрация азотной кислоты не влияет на процесс C(HNO3) = 47-60%
4) скорость перемешивания влияет положительно.
5) Тонина помола сырья влияет положительно.
6) τ(пр)=1,5- 2ч.
Выделение фтора при обработки природных фосфорной азотной кислотой большая часть фтора содержащегося в фосфатах переходит в раствор АКВ в виде Н2SiF6, который отрицательно влияет на переработку. Фтор из раствора выделяется с помощью добавляемой к нему натриевой соли (NaNO3, Na2CO3, Na2SO4).
N=200-300% (соли) от стехиометрического т.к. нужно высаливать, при этом 80-85% F осаждается в виде Na2SiF6.
При азотнокислотной переработки 1т. апатита получено 63кг Na2SiF6 c влажностью 30% с содержанием Na2SiF6 в сухом веществе составляет 87%.
Выделение редкоземельных элементов.
В апатитовом концентрате содержится 0,9- 0,96% редкоземельных элементов (Ce,- La) выделение редкоземельных элементов из раствора полученного в результате разложения апатитового концентрата азотной кислотой основано на малой растворимости фосфатов редкоземельных элементов в слабо кислых растворах рН= 2- 2,5.
Оптимальные условия для осаждения 80- 90% редкоземельных элементов: концентрация раствора 35% (Ca(NO3)2) концентрация Р2О5-95% t = 60o C.
Нейтрализация всей свободной HNO3 и 50% первого иона водородного фосфорной кислоты, время осаждения 2 часа, при этом из 1т апатита получено 10,7кг фосфатов редкоземельных элементов.
Процесс осуществляется следующим образом, АКВ (после выделения из неё шлама фтористых соединений) нейтрализуют газообразным аммиаком или известняком.
(в виде суспензии СаСО3 при рН= 2- 2,5 проводят нейтрализацию, выпадают белые кристаллы.
2Ce(NO3)3+2H3PO4+3CaCO3=2CePO4↓+3Ca(NO3)2+3CO2+3H2O.
Процесс проводят непрерывно в несколько последовательно соединенных реакторах с паровыми змеевиками при перемешивании.
Отделение осадка от раствора производят декантацией, затем на барабанных вакуум-фильтрах (в осадке 15-25% влаги).
Кислотная переработка фосфорного сырья.
При такой переработки преследуют 2 цели:
1.перевести нерастворимые формы фосфора в усвояемые растениями и животными формы.
2.получить из фосфатного сырья, которое содержит много примесей более чистые соли или соединения, которые могут быть использованы в качестве технических продуктов.
Схема переработки фосфатов
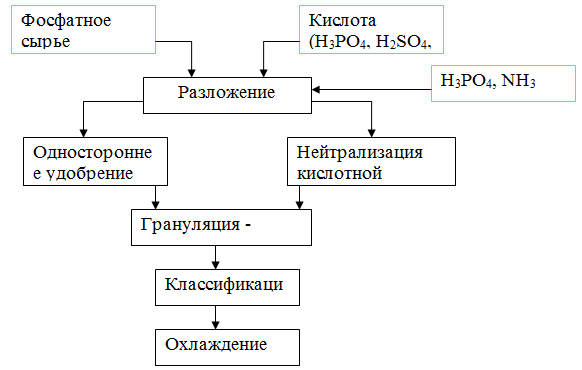
2Ca5F(PO4)3+14HNO3+3H2O=3Ca(H2PO4)2∙ H2O+7Ca(NO3)2+2HF(2)
Ca5F(PO4)3+4HNO3→ 3Ca3HPO4
Информация в лекции "7 ВКЛ" поможет Вам.
2Ca5F(PO4)3+2HNO3→3Ca3(PO4)2+Ca(NO3)2+2HF(4)
Применяют следующие способы, соотношение СаО к Р2O5 в перерабатываемой системе.
1.вымораживание Са(NO3)2 ∙ 4H2O из вытяжки при t =-20 – 0oC
2. Разложение фосфатов азотной и серной кислотой.
3.Осаждение избытка кальция в виде СаSO4 серной кислотой или сульфатами аммония, натрия, калия.
4. Осаждение избытка кальция в виде СаSО4 двуокисью углерода и аммиака.






















