Предельные углеводороды
Тема № 6
1. Гомологический ряд предельных углеводородов
2. Изомерия
3. Способы получения
4. Газообразные алканы
5. Жидкие алканы
6. Физические свойства алканов (циклоалканов)
А) Циклоалканы низкокипящих фракций и газоконденсатов
Рекомендуемые материалы
Б) Циклоалканы средних фракций
В) Циклоалканы тяжёлых фракций
7. Химические свойства алканов (циклоалканов)
А) Хлорирование и фторирование
Б) Термическая деструкция и гидрогенолиз
В) Окисление
8. Окислительная конверсия метана в синтез-газ
9. Основные химические продукты, получаемые из предельных
углеводородов
10. Литература Гомологический ряд. Для алканов гомологический ряд начинается с метана как простейшего представителя предельный гомологический ряд:
СН4 – метан С5Н12 – пентан
С2Н6 – этан С6Н14 - гексан
С3Н8 – пропан С7Н16 – гептан
С4Н10 – бутан С8Н18 – октан и т. д.
Как видно, каждый последующий член ряда отличается от предыдущего по составу на группу СН2 называют гомологической разностью, члены ряда называют гомологами. Отсюда можно вывести в общую формулу ряда предельных углеводородов: СпН2п+2.
Гомология – явление, общее для органической химии. Она наглядно иллюстрирует проявление одного из основных законов диалектики – перехода количество в качество.
Изомерия. Четвёртый член гомологического ряда предельных углеводородов бутан С4Н10 отличается от трёх предыдущих гомологов тем, что имеет два изомера: нормальный бутан с неразветвлённой углеродной цепью и изобутан с разветвлённой углеродной цепью
СН3 – СН2 – СН2 – СН3 СН3 – СН – СН3

СН3
нормальный бутан изобутан
Оба эти углеводорода – газы, но с различной температурой кипения: - 0,50С для бутана и - 11,70С для изобутана.
Первые члены гомологического ряда алканов – метан, этан, пропан – существуют только в одной форме. Они не имеют изомеров. У бутана существуют два изомера. У углеводорода состава С5Н12 – пентана известны три изомера:
СН3


 СН3 – СН2 – СН2 – СН2 – СН3 СН3 – СН – СН2 – СН3 СН3 – С – СН3
СН3 – СН2 – СН2 – СН2 – СН3 СН3 – СН – СН2 – СН3 СН3 – С – СН3
СН3 СН3
пентан изопентан неопентан
С увеличением числа углеродных атомов в молекуле углеводорода возрастает и число возможных изомеров. Так, для гексана оно составляет 5, для гептана – 9, для октана – 18, для нонана – 35, для декана – 75, для пентадекана С15Н32 – 4347, для эйкозана С20Н42 – 366319. Это не значит, что все теоретически возможные изомеры получены. Для углеводо-
родов С1 – С9 они получены, для высших членов ряда получены лишь некоторые.
Способы получения. Главными источниками получения алканов является нефть, природные и попутные газы и каменные угли.
1. Предельные углеводороды с небольшим числом углеродных атомов от С1 до С11 можно выделить фракционной перегонкой нефти, газа или смесей углеводородов, получаемых гидрированием угля. Реакция гидрирования угля под давлением, а также оксида или диоксида углерода в присутствии катализаторов – железа, кобальта, никеля при 200 – 4500С имеет важное самостоятельное значение для получения синтетического бензина:
 4000С; 100*105Па
4000С; 100*105Па
пС +(п + 1)Н2 СпН2п+2
2000С
 пСО + (2п +1)Н2 СпН2п+2 + пН2О
пСО + (2п +1)Н2 СпН2п+2 + пН2О
Ni
2. Одним из способов получения алканов является гидрирование непредельных углеводородов в присутствии катализаторов – платины, палладия, никеля или хромита меди:
Катализ
 R – CH = CH – R* + H2 R – CH2 – CH2 – R*
R – CH = CH – R* + H2 R – CH2 – CH2 – R*
3. Алканы получают реакцией восстановления галогенопроизводных водородом в момент его выделения или водородом, возбуждённым катализатором, а также иодоводородом:
CH3 – CH2 – Cl + 2H à CH3 – CH3 + HCl
 Катализ
Катализ
CH3 – CH2 – Cl + H2 CH3 – CH3 + HCl
CH3 – CH2 – Cl + HI à CH3 – CH3 + I2
4. Синтез алканов можно осуществить по реакции Вюрца действием металлического натрия на моногалогенопроизводные. При этом могут быть получены углеводороды сим- метричного и несимметричного строения
2CH3I + 2Na à CH3 – CH3 + 2NaI
CH3 + CH3 – CH2I + 6Na à CH3 – CH3 + CH3 – C2H5 + C2H5 – C2H5 + 6NaI
При использовании реакции Вюрца удовлетворительный выход алканов дают пер - вичные галогенопроизводные. В случае вторичных или третичных галогенопроизводных выход предельных углеводородов составляет всего несколько процентов.
Вместо натрия могут быть использованы другие металлы, например литий, магний, цинк.
5. Предельные углеводороды могут быть получены из галогенопроизводных действием металлического лития и солей меди:
R – X + 2Li à R – Li + LiX
2R – Li + CuI à R2CuLi + LiI
R2CuLi + 2R*I à 2R – R* + LiI + CuI
6. В лабораторной практике предельные углеводороды получают декарбоксилирова- нием карбоновых кислот сплавлением их со щёлочами:
O
R – C + NaOH à R – H + NaHCO2
O – H
Газообразные алканы. В зависимости от месторождений углеводородные газы под- разделяют природные, попутные и газы газоконденсатных месторождений.
Природные газы добывают с чисто газовых месторождений. Они состоят в основном из метана с небольшой примесью этана, пропана, бутанов, пентанов, а также азота. Эти газы относятся к группе сухих. Содержание метана в них в основном 93 – 98%, этана и пропана – незначительно. Более высокомолекулярные углеводороды, как правило, присутствуют в виде слоёв, хотя некоторые газы характеризуются их повышенным содержанием. В газах имеется небольшая примесь диоксидов углерода и азота.
Попутные газы добывают совместно с нефтью. При выходе нефти на поверхность газ вследствии снижения давления выделяется из нефти. Попутные газы относятся к жирным
и служат источником для извлечения из них лёгкого бензина – так называемого газового бензина.
При переработке нефти из нефтезаводских газов на газофракционирущих установках (ГФУ) получают следующие углеводородные фракции (чистотой 90 – 96%):
этановая – сырьё для пиролиза, хладоагента на установках депарафинизации масел и выделение ксилола и др.;
пропановая – сырьё для пиролиза, получения ожиженного газа, хладоагента;
изобутановая – сырьё для алкилирования и производства синтетического каучука;
н-бутановая – сырьё для пиролиза, производства синтетического каучука, компонента бытового ожиженного газа и др.;
изопентановая – сырьё для производства изопренового каучука и компонента высокооктановых бензинов;
пентановая – сырьё для процессов изомеризации и пиролиза, получения амиловых спиртов.
В последние годы в связи с увеличением глубины разведочных скважин и освоением новых перспективных территорий открывается всё больше газоконденсатных и нефтегазоконденсатных залежей, конденсат становится самостоятельным полезным ископаемым.
Газоконденсатные залежи – это скопление в недрах газообразных углеводородов, из которых при снижении давления выделяется жидкая углеводородная фаза – конденсат (смесь углеводородов – пентана и более высоких гомологов метана).
Конденсат бывает сырой и стабильный. Сырой конденсат представляет собой жидкость, получаемую непосредственно в промысловых сепараторах при нормальных условиях углеводороды, в которых растворено то или иное количество газообразных углеводородов. Стабильный конденсат получают из сырого путём его дегазации.
Газы газоконденсатных месторождений содержат большое количество метана, а также высокомолекулярных углеводородов, входящих в состав бензиновых, керосиновых, а иногда и дизельных фракций нефти. Большая часть разведанных и введённых в эксплуатацию за последние годы газовых месторождений относится к газоконденсатному типу. В газах этих месторождений содержатся 2 – 5% и более жидких углеводородов.
Конденсаты, как и нефти, состоят из алканов, нафтенов и аренов. Однако распределение этих групп углеводородов в конденсатах имеет ряд особенностей:
абсолютное содержание (в среднем) аренов в бензиновых фракциях конденсатов выше, чем в нефтях;
встречаются бензиновые фракции, в которых содержится одновременно большое количество нафтенов и аренов;
между содержанием алканов и аренов в бензиновых фракциях существует обратная связь (чем больше алканов, тем больше аренов); содержание разветвленных алканов ниже, чем н-алканов. Конденсаты с высоким содержанием аренов широко распространены на территории Амударьинской и Днепровско-Донецкой впадины (соответственно до 60 и 28-31%).
Газоконденсаты Заподного Предкавказья в направлении регионального погружения от Староминско - Леннинградского до Усть-Лабинского характерезуются изменением типа конденсанта – от алканового через алкано-нафтеновый и алкано-ареновый до арено-алканового. Отношение алканов к аренам в этих конденсатах составляет соответственно 17 – 22; 5,4 – 7,2; 0,8 – 1,2 и 0,7 –0,8, а содержание ароматических углеводородов возрастает от 3 – 4 до 44 – 48%.
Основную часть конденсатов всех исследованных газоконденсатных месторождений Средней Азии (было изучено 50 различных конденсатов) составляют бензиновые (лигроиновые) фракции (100 – 200%) или углеводороды состава С7 – С13; содержание в конденсатах легкой части (до 100оС) редко превышает 10%. Некоторые конденсаты отличаются высоким содержанием гомологов бензола (20 – 30% и выше) и гомологов циклогексана (до 25 – 25%); другие – низким содержанием этих углеводородов и повышенным - гомологов циклопентана.
Углеводородный состав конденсатов характеризуется следующими закономерностями. Среди алканов разветвленного строения преобладают монометилзамещенные: 2-, 3- и 4-метилзамещенные. В наибольшем количестве содержатся 2-метилпентан, 2-метил - гексан и 2-метилгептан. Среди диметилпроизводных присутствуют главным образом 2,3- и 2,4-диметилозамеры. Циклопентановые углеводороды помимо циклопентана представлены в основном его метили этилзамещенными, а также 1,2- и 1,3-диметилцикло- пентанами. В конденсатах обычно содержатся все три изомера диметилциклогексана, причем на долю 1,3-диметилциклогексана приходится от 50 до70%количества изомеров.
Представляет значительный интерес состав газа Оренбургского газового и газоконденсатного месторождений. Залежь газа массивная, высота залежи 514 м, она имеет нефтяную оторочку. Раздел газ – нефть находится на отметке 1750 м, а раздел вода – нефть – на отметке 1770 м. Из всех скважин кроме газа выносятся конденсат и сероводород.
ЖИДКИЕ АЛКАНЫ.
Углеводороды лёгких фракций нефти. Алканы от С5 до С9, входящие в состав бензиновых фракций, в обычных условиях представляют собой жидкости. На основании анализа индивидуальных углеводородов, выделенных из 10 нефтей СНГ, установлено, что бензиновые фракции нефти в основном представлены соединениями с простейшими заместителями. Исключение составляют нефти месторождений Анастасиевского и Нефтяные Камни, в которых имеются изомеры с длинными боковыми цепями.
Анализ данных о содержании индивидуальных алканов в бензиновых фракциях
одинаковых пределов перегонки показал, что в наибольшем количестве находится простейший углеводород, а следующим за ним изомером обычно является метилзамещенный в положении 2 или 3.
Из 35 теоритически возможных нонанов уже выделено 24. Найдены все 5 изомеров гексана, из 9 гептанов – 7, из 18 изомеров октана – 16. Количественное содержание сильно разветвлённых изомеров незначительно.
Таким образом, на долю н-октана и трех простейших его изомеров приходится более 85% от суммы октанов. Аналогично на н-гексан и простейшие изомеры приходится 97% от суммы гексанов.
При исследовании бензинов различных нефтей комбинированным методом было определено до 90% углеводородов – алканов, циклоалканов С5 и С6 и аренов. Установлены некоторые закономерности в распределении углеводородов в бензине в зависимости от типа нефти. Бензины различных нефтей содержат примерно один и тот же набор углеводородов, однако в неодинаковом количестве, причем 10 углеводородов, присутствующих в бензине, содержатся в наибольшем количестве.
В настоящее время надежно установлены основные закономерности в распределении алканов и изоалканов в бензинах нескольких десятков отечественных нефтей всех типов. Выделяют три основных типов бензина. Оказалось, что составы бензинов всех парафинистых нефтей (А1) достаточно близки. При этом соотношение между нормальными и разветвлёнными изомерами варьирует незначительно. В бензинах нефтей типа А2 значительно ниже содержание н-алканов, а распределение изоалканов примерно такое же, что и в бензинах нефтей типа А1. В бензинах нефтей типа Б часто наблюдается аномальное распределение изомеров. Так, среди углеводородов С5 – С8 нефтей этого типа наблюдаются высокие концентрации гемм и виц - замещённых структур. В нефтях типа А1 (сургутской, ромашкинской, грозненской парафинистой) содержание н-гексана составляет 52 – 71%, н-гептана 55,9 –61%, н-октана 41 – 54,8%, н-нонана 30,7 – 38,4%, н-декана 39,4 – 39,9% (на сумму изомеров соответственно). В типа А2 (Старо-Грозненский) содержание н-алканов С6 – С10 значительно ниже и равно соответственно 12,0; 9,5; 4,3; 5,2 и 2,0% (от суммы изомеров).
Среди разветвлённых изомеров С6 – С3 в нефтях А1 и А2 резко преобладают метил- замещенные структуры по отношению к дизамещённым. Для четырёх указанных выше нефтей это соотношение варьирует в пределах 3,2 – 15,0. Концентрация гемм - замещённых углеводородов незначительны. Напротив в нефтях группы Б высоко содержание диметилзамещённых структур, как геминальных, так и вицинальных. Например, в анастасиевско-троицкой нефти (группа Б) соотношение моно- и дизамещённых соответствующих гомологов С6 – С9 варьирует в интервале 0,05 – 0,96. В нефтях группы Б среди метилзамещённых углеводородов более высоко содержание 3-метилалканов, а в нефтях А1 и А2 – 2-метилалканов.
Ал. А. Петров систематизировал количественные данные об относительном распределении гексанов, гептанов, октанов, нонанов, н-деканов в нефтях типа А1, А2, Б и газовых конденсатах. Среди изомерных гексанов в нефтях количественно определены н-гексан, 2- и 3-метилпентаны, а также 2,3- и 2,2-диметилбутаны. Состав изомеров гептана следующий: н-гептан, 2- и 3-метилгептаны, 2,3-, 2,4-, 2,2- и 3,3-диметилпентаны, а также
2,2,3-триметилбутан. Среди изомеров октана в нефтях определены н-октан, 2-, 3- и 4-ме – тилгептаны, 2,3-, 2,4-, 2,5-, 3,4-, 2,2-, 3,3-диметилгексаны, а также 2,3,4-, 2,2,3, 2,3,3-три – метилпентаны.
В алканах С9 обнаружено весьма высокое содержание двух углеводородов – 2,3- и 2,6-диметилгептанов. Предполагается, что эти углеводороды принадлежат к соединениям реликтового типа. Среди изомеров С10 отмечено заметное преобладание изопреноидного углеводорода 2,6-диметилоктана и 2-метил-3-этилгептана и 2,3-диметилоктанов С7 и С9 в нефтях обусловлены их образованием из реликтовых предшественников путем отрыва алифатических цепей от стеранов.
Углеводороды средних фракций нефти. Значительно труднее исследовать углеводородный состав средних фракций нефти, что видно на примере изучения ромашинской и арланской парафинистых нефтей. Обе нефти отличаются высоким содержанием серосодержащих соединений (1,8 и 2,84% серы), смолистых веществ (9,0 и 20,3%); они могут быть отнесены к парафинистым нефтям (содержание парафина 4,9 и 4,7%). Исследование нефтей проводили по одной программе. Нефть после деасфильтизации при низкой температуре перегоняли с выделением фракции 180 – 350оС, которая и подвергалась дальнейщему исследованию. Фракция содержала около 19% н-алканов и 20% аренов.
С помощью адсорбционной хроматографии на силикагере дробные фракции 180 – 200, 200 – 300 и 300 – 350оС были разделены на две части: 1) смесь алканов и циклоалка – нов и 2) смесь аренов и серосодержащих соединений. н-Алканы выделяли из смеси методом комплексообразования с карбамидом и затем обычным путем идентифицировали с помощью ГЖХ. Углеводороды, выделенные тиокарбамидом, помимо н-алканов содержат некоторое количество алканов разветвлённого строения и циклоалканов. Так, было установлено, что кристаллизующиеся углеводороды фракции 300 – 3500С ромашинской нефти, образующие комплекс с тиокарбамидом, содержали 60% н-алканов и ≈ 40% изоалканов и циклоалканов. В ходе исследования был разработан другой метод выделения н-алканов из смеси насыщенных углеводородов с помощью адсорбционной хроматографии на угле. В дальнейшем этот метод был усовершенствован и применён для разделения алканов и циклоалканов разветвлённого строения – наиболее трудно разделяемой смеси углеводородов нефти. В дистилляте 180 – 3500С ромашкинской и арланкой нефтей найдены н-алканы от С11 (ундеканы) до С20 (эйкозана). Содержание каждого из этих углеводородов составляет 0,4 – 0,5%. На основании анализа керосиновых фрак- ций 77 отечественных и зарубежных нефтей показано, что в них присутствует десять изомеров декана. Некоторые изомеры частично выделены, а большая часть обнаружена спектрофотометрически. Из углеводородов С11 – С16 в этих фракциях найдены ундекан, додекан, три- и тетрадекан, пентадекан и гексанов (цетан).
Ал. А. Петров исследовал сочетанием методов ГЖХ и масс-спектрометрии алканы средних и высококипящих фракций отечественных нефтей различных типов. В надёжно количественно оределены моно- и диметилзамещённые алканы С11 – С15. Метил- замещённые алканы симметричного строения (5-метилнонан, 6-метилундекан) содержат- ся в значительно меньших количествах, чем остальные изомеры. Эта тенденция наблюдалась также для 4-метилгептана и 3-метилпентана.
Содержание метилзамещённого изомера снижается по мере перемещения СН3-группы к центру молекулы. Отношение суммарного содержания монометилзамещённых алканов к содержанию изомерного н-алкана в углеводородах различной молекулярной массы в общем сохраняется при некоторой тенденции к снижению с ростом алифатической цепи молекулы.
Если суммировать результаты исследований индивидуального состава углеводо- родов нефти, то к настоящему времени число выделенных или надёжно определённых составляет более 600. Лучше всего изучены нормальные алканы.
В нефти установлено присутствие всех н-алканов, от бутана (tкип=0,50С) до тритриаконтана С33Н68 (tкип=4750С); некоторые из этих углеводородов выделены в чистом виде с чистотой выше 99%. Содержание н-алканов в нефтях снижается с повышением молекулярной массы; количество высших гомологов – 0,1% и ниже.
Физические свойства алканов определятся их составом и строением. Первые четыре члена гомологического ряда при обычных условиях – газы, С5 – С15 – жидкости, начиная С16 – твёрдые тела (табл. 1).
Таблица 1. Физические свойства некоторых алканов.
| Название | Формулы | Т.пл., 0С | Т. кип., 0С | d204 |
| Метан Этан Пропан Бутан Изобутан Пентан Изопентан Неопентан Гексан Неогексан Гептан Октан Изооктан Нонан Декан Эйкозан | СН4
С2Н6
С3Н8 С4Н10
СН3 – СН(СН3) – СН3 С5Н12 (СН3)2СН – СН2 – СН3 СН3 – С(СН3)3 С6Н14 (СН3)3С – СН2 – СН3 С7Н16 С8Н18 (СН3)3С – СН2 – СН(СН3)2 С9Н20 С10Н22 С20Н42 | -182,5 -182,8 -187,6 -138,3 -159,4 -129,7 -159,9 -16,6 -95,3 -99,7 -90,6 -56,8 -107,4 -53,6 -29,7 … 36,4 | -161,5 -88,6 -42,1 -0,5 -11,7 36,07 27,9 9,5 68,7 49,7 98,5 125,7 99,2 150,8 174,0 … 342,0 | 0,415 (при –1640С) 0,561 (при –1000С) 0,583 (при- 44,50С) 0,500 (при 00С) 0,563 0,626 0,620 0,613 0,660 0,649 0,684 0,703 0,692 0,718 0,730 0,777 |
С увеличением молекулярной массы повышается температура плавления и кипе- ния алканов, возрастает плотность. Алканы с нормальной цепью углеродных атомов кипят при более высокой температуре, чем алканы с разветвлённой цепью. Это объясняется меньшим взаимодействием между молекулами с разветвлённой цепью в жидком состоянии: боковые цепи создают пространственные препятствия для сближения молекул. Кроме этого, углеводороды с разветвлённой цепью мало склонны к комплексообразованию например с мочевиной, в то время как нормальные алканы образуют комплексные соединения. Различие в способности к комплексообразованию даёт возможность отделять алканы изостроения от углеводородов нормального строения.
Все углеводороды парафинового ряда легче воды и нерастворимы в ней, но хорошо растворимы друг в друге и сами являются хорошими растворителями жиров, масел и других органических соединений.
Газообразные и твёрдые углеводороды не обладают запахом, жидкие углеводороды имеют характерный запах бензина и керосина.
Циклоалканы составляют большую часть нефти, при переработке значительная их часть переходит в дистиллятные продукты. В нефтях встречаются моно- и полициклические циклоалканы. Первые представлены в основном циклопентанами и циклогексана- ми, вторые включают конденсированные соединения типа декалина С10Н18:
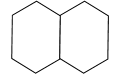 |


 сочленнёные соединения типа бициклогексана:
сочленнёные соединения типа бициклогексана:


 соединения с мостиковыми связями типа норборнана:
соединения с мостиковыми связями типа норборнана:


 спирановые соединения типа диспиро [5,1,5,1] тетрадекана:
спирановые соединения типа диспиро [5,1,5,1] тетрадекана:






 трициклические углеводороды типа адамантана (трицикло [3,3,1,10,7] –декана):
трициклические углеводороды типа адамантана (трицикло [3,3,1,10,7] –декана):
пергидроароматические углеводороды типа трицикло [7,3,1,05.13] –тридекана:
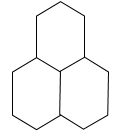
Циклоалканы более сложного строения не обнаружены в нефтях. Циклоалканам присущи следующие особенности: геометрическая изомерия молекул; способность к структурным превращениям в процессах нефтепереработки; положительное влияние на качество топливных и масляных дистиллятов; связь строения с генезисом и метаморфизмом нефти.
Строение циклоалканов изучено недостаточно, особенно в средне- и высококипящих фракциях нефти, так как отсутствуют эффективные методы из выделения и разделения. Исследования строения и идентификация индивидуальных циклоалканов нефтей и их фракций сопряжены с большими трудностями из-за крайне незначительных различий свойств циклоалканов и гомологов циклоалканов, не разделяющихся при ректификации и хроматографии. Требуется осуществлять многократные превращения циклоалканов с помощью реакций изомеризации, дегидрирования, деструкции в углеводородов других классов, поддающихся анализу известными методами.
Циклоалканы нефтяных фракций являются основным источником для получения ароматических углеводородов (риформинг), капролактама, адипиновой кислоты и других продуктов.
ФИЗИЧЕСКИЕ СВОЙСТВА.
Циклоалканы низкокипящих фракций и газоконденсатов.
Установлены основные закономерности их распределения в нефтях и фракциях. В табл.2
приведен групповой состав углеводородов легких фракций нефтей и газо конденсата ряда крупных месторождений.
ТАБЛИЦА 2. Групповой состав фракции н.к.- 125оС (в %)
| Месторождение | Массовый выход, в % | Циклоалканы | ||
| пятичленные | шестичленные | |||
| Грозненское Заподно-Сибирское Сургутское Сахалинское Первомайское Эхабинское Бакинское Нефтяные Камни Кара-Даг (газоконденсат) | 6,8
5,7
13,9 7,0 2,4 40,0 | 22,0 14,5 31,0 53,0 25,5 16,0 | 20,0 14,0 31,0 27,0 26,5 27,0 | |
Из табл.1 видно, что больше всего циклоалканов содержит фракция газоконденсата (172 кг/т сырья с учетом выхода фракции). С повышением температур конца кипения фракций в них появляются би- и трициклоалканы (табл.3)
ТАБЛИЦА 3. Соотношение структурных групп циклоалканов фракции 125-230оС бакинской нефти.
| Структуры | Алкилцикланы | |||
| С9 | С10 | С11 | С12 | |
| Бициклоалканы: трициклоалканы | 100:0 | 95:5 | 84:16 | 85:15 |
| Декалины: другие бициклоалканы | - | 57:43 | 43:57 | 49:51 |
Ниже представлен массовый состав углеводородов стандартного прямогонного бензина ромашкинской нефти, %
Циклоалканы 27,97
Метилциклопентан 1,87
Диметилциклопентаны 1,85
Триметилциклопентаны 1,50
Циклогексан 0,63
Метилциклогексан 4,34
Диметилциклогексаны 2,34
Циклоалканы С9 5,60
С10 5,14
С12 2,30
Алканы С5-С12 58,64
Арены 13,39
Бензины циклоалканового типа содержат 50-70%, алканнового типа – 20-30% циклоалканов. Внастоящее время проводятся интенсивные исследования состава циклоалканов 10 нефтей различных месторождений и их фракций.
Интересен углеводородный состав газоконденсатов и бензинов, содержащих значительные количества циклоалканов. Между конденсатами и бензинами существует гинетическая связь-они имеют похожий углеводородный состав. Однако в газа конденсатах преобладают моно-, ди- и тризамещенные шестичленные циклоалканы, а в бензинах пяти- и шестичленные циклоалканы присутствуют в примерно равных конентрациях. Среди пятичленных циклоалканов преобладают метилциклопентаны.
С повышением температур начала и конца кипения нефтяных фракций резко усложняются состав и строение циклоаланов. Для выделения би- и трициклоалканов проводят ректификацию, деароматизацию и депарафинизацию узких фракций нефти. Смесь изоалканов и циклоалканов разделяют термической диффузией. Гидрокрекингом на платиновом катализаторе при 380-450оС удалялись неадамантановые соединения, составляющие 80-90% суммы трициклоалканов. С помощью газожидкостной хроматографии идентифицированы следующие производные адамантана: 1-метил-, 2-метил-, 1,3-диметил-(цис), 1,4-диметил(транс), 1,2-диметил-, 1-этил-, 2-этил, 1,3,5-триметил-, 1,3,6-триметил-, 1,3,4-триметил-, 1,3,4-триметил-(цис), 1,3,4—триметил-(транс) и 1-метил-3-этиладаманта –на.
ЦИКЛОАЛКАНЫ СРЕДНИХ ФРАКЦИЙ.
Средняя молекулярная масса циклоалканов увеличивается при переходе к более высококипящим фракциям нефти примерно в равной степени как за счет возрастания числа циклов, так и удлинения алифатических радикалов, 50-70% углерода в высококипящих фракциях циклоалканов приходятся на долю алифатических цепей. Для циклоалканов высококипящих фракцийхарактерны длинные алифатические цепи, число
атомов углерода которых уменьшается с увеличением цикличности молекул при приблизительно эквивалентной молекулярной массе.
При исследовании рядов циклогексана и декалина широкой фракции 180-350оС арланской нефти циклоалкано-изоалкановая часть хроматографических фракций подвергалась аналитическому дегидрированиюна железоплатином катализаторе. Продукты дегидрирования разделяли хроматографически на оксиде алюминия. Дегидрогенизаты содержали: фракция 180-200оС – 25% образовавшихся вторичных ароматических углеводородов, из них 2,2% моно- и 0,3% бициклосоединений; фракция 200-300оС-11,9% вторичных углеводородов, из них 10,2% моно- и 1,7% бициклосоединений; фракция 300 – 350оС-45,3% вторичных углеиодородов, из них 40,5% моно- и 4,8% бициклических аренов. Таким образом, в исследованных фракциях и в исходной широкой фракции 180-350оС соотношение моно- и бициклоалканов составляло (6 ÷ 8):1. С помощью газожидкостной хроматографии количественно идентифицированы декалин, 1- и 2-метилдекалины, 2-этилдекалин, 1,2-, 1,3-, 1,4-, 1,5-, 1,6-, 2,3-, 2,6- и 2,7-диметилдекалины. Качественно установлено присутствие гексаметиленовых углеводородов: моно-, ди- и тризамещенных производных циклогексана, однозамещенных и дизамещенных производных бициклогексила с радикалами в 2,2*-, 2,3*-, 2,4*-, 2,3-, 2,4-, 2,5-положениях, 2,6,2*,6*-тет – раметилдициклогексила, производных гидринданов. Общая характеристика арланской нефтиприведена в табл.4 и 5.
ТАБЛИЦА 4. Состав и физические свойства фракций арланской нефти.
| Пределы перегонки оС | Плотность при 20оС, кг/м3 | Молекулярная масса | Углеводородный состав, % | |||
| Нормальные алканы | Изо алканы | Цикло пентаны | Цикло гексаны | |||
| 180-200 | 792 | 148 | 18,5 | 46,4 | 11,5 | 1,5 |
| 200-300 | 834 | 186 | 19,9 | 30,0 | 14,3 | 6,0 |
| 300-350 | 880 | 259 | 18,3 | 14,7 | 14,7 | 15,2 |
ТАБЛИЦА 5. Содержание декалина и его производных в арланской нефти и фракции 200-300оС (в %)
| Соединение | Нефть | Фракция 200-300оС | Соединение | Нефть | Фракция 200-300оС |
| Декалин | 0,002 | 0,016 | 2,6- и 2,7-диметил- | 0,007 | 0,052 |
| 2-Метил | 0,004 | 0,032 | 1,3- и 1,6-диметил- | 0,002 | 0,018 |
| 1-Метил | 0,005 | 0,038 | 1,4-, 1,5-, и диметил- | 0,005 | 0,040 |
| 2-Этил | 0,006 | 0,045 | 1,2-ди-метил- | 0,0009 | 0,067 |
Таким образом, и в легких, и в средних, и в тяжелых фракциях нефти моноциклоалканы содержатся в значительных количествах наряду с закономерным возрастанием в высококипящих фракциях многокольчатых структур
ЦИКЛОАЛКАНЫ ТЯЖЕЛЫХ ФРАКЦИЙ.
Большой интерес для нефтехимических производств представляет изучение строения углеводородов тяжелых фракций нефтей, например вакуумных газойлей.
Фракции450-520оС вакуумных газойлей ряда нефтей содержали высокомолекулярные полициклоалканы. Для их выделения и анализа из фракций удаляли арены и нормальные алканы. Полученные циклоалканоизоалкановые фракции подвергали вакуумной перегонке при остаточном давлении 1,33 Па, затем обрабатывали тиокорбамидом, 15-23% углеводородов образовывали комплексы. Хроматографией получали концентраты стеранов и тритерпанов, которые анализировали на хроматографе. Эталоном служила смесь синтетических индивидуальных стеранов- холестана, кампестана и стигмастана, а также концентрат тритерпанов, гопаны С29-С32. Стераны и трепаны концентратов идентифицировали с помощью хромато-масс-спектрометрии. В концентрате углеводородов мангыщлакской нефти, образующих аддукт с тиокарбамидом, идентифицировано 6 стеранов С27 и С28, два 4-метилстерана С29-С30, холестан С27, эргостан (кампестан) С28, изоэргостан С28,изостигмастан С29, 4-метиоэргостан С29 и 4-метилстиг- трате углеводородов мангышлакской нефти, образующих аддукт с тиокарбомидом, обнаружен стеран стигмастан С29,9 тритерпанов С27-С32, Аналогичным методом в арланской нефти идентифицированы 6 стеранов С27-С28 и 10 тритерпанов. В самотлорской нефти стераны отсутствовали, но было идентифицировано 12 тритерпанов. Ниже приведено массовое содержание циклоалканов фракций 450-520оС разных месторождений (в %):
Меторождение Стераны Триетрпаны Мангышлакское 0,007 0,03 Арланское 0,001 0,001 Самотлорское 0 0,01 Всего идентифицировано 14 стеранов и 34 тритерпанов.
















 В мангышлакской нефти методом хроматомассспектрометрии идентифицированы моноциклоалканы С10-С22, принадлежащие к гомологическому ряду транс- 1,1,3-метил -2-алкилциклогексана. Алкильные заместители в углеводородах, начиная с С14, имели изопреноидный тип строения:
В мангышлакской нефти методом хроматомассспектрометрии идентифицированы моноциклоалканы С10-С22, принадлежащие к гомологическому ряду транс- 1,1,3-метил -2-алкилциклогексана. Алкильные заместители в углеводородах, начиная с С14, имели изопреноидный тип строения:
Углеводороды подобного строения содержались во фракции 180-400оС, выход которой на нефть составил 40%. По данным масс-спектрометрических исследований во фракции циклоалкано-изоалканов содержались (в%): 31,4 изоалканов, 26,4 моноциклоал-канов, 23,7 би-, 11,9 три-, 6,6тетрациклоалканов.
Таким образом, в низкокипящих фракциях нефтей содержатся преимущественно алкилпроизводные циклопентана и циклогексана, в высококипящих фракциях – полициклоалканы и моноциклоалканы изопреноидного строения.
ХЛОРИРОВАНИЕ И ФТОРИРОВАНИЕ АЛКАНОВ.
Хлорирование алканов. При парофазном хлорировании парафинов скорости замещения водорода при первичных, вторичных и третичных атомов углерода относятся как 1,00 : 3,25 : 4,43. При более высокой температуре эти скорости приближаются к одной и той же величине независимо от того, происходит хлорирование в жидкости или газовой фазе. Слишком высокая температура или чрезмерная продолжительность реакции вызывает пиролиз монохлоридов, которые по своей устойчивости располагаются в следующем порядке: первичные > вторичные > третичные.
Промышленное значение имеют продукты хлорирования алканов С1-С5 и высших парафинов (С12-С13).
Из всех насыщенных углеводородов метан хлорируется с наибольшим трудом, однако, при достаточно высокой температуре реакция протекает нормально.
Хлорирование метана протекает ступенчато:
CH4 + Cl2 à CH3Cl + HCl Δ H = -23,9 ккал/моль
СH3Cl + Cl2 à CH2Cl2+HCl Δ H = -23,7 ккал/моль
CH2Cl2 + Cl2 à CHCl3 + HCl Δ H = -24 ккал/моль
CHCl3 + Cl2 à CCl4 + HCl Δ H = -24ккал/моль Кроме этих реакций может протекать разложение:
CH4 + 2Cl2 à C + 4HCl (эту реакцию можно использовть для получения безводного хлористого водорода).
В настоящее время не удалось установить такие условия, которые позволили бы получить только один из продуктов хлорирования метана. Состав продуктов хлорирования в большей степени зависит от соотношения реагентов и температуры, чем от катализаторов. На рис. 17 представлена зависимость состава продуктов хлорирования от исходного соотношения хлора и метана.
На промышленной установке, где подучают четыре хлорпроизводных метана, используют чистые метан и хлор. Хлорирование осуществляют при 450-500оС, после чего хлорпроизводные, содержащие смесь CCl4 и CHCl3, абсорбируют, отделяют образовавшуюся хлористоводородную кислоту от хлора и непрореагировавшего метана. После этого разделяют фракционной перегонкой CH3Cl (т.кип. = 24оС) и CH2Cl2 (т.кип. = =40оС). Остаток из абсорбционной колонны, содержащей немного CCl4 (т.кип.=46,8оС) и CHCl3 (т.кип.=61,2оС), вновь хлорируют в жидкой фазе. В результате получают двойную смесь, содержащую только CCl4 и CHCl3, которые можно разделить ректификацией.
Хлорирование высших парафинов. Хлорирование С12-С13-парафинов, входящих в фракцию керосина, кипящей при 220-245оС, проводят для получения “керилхлорида”; последний используется для производства синтетических моющих средств. Хлорирование проводят при 60оС до получения 50%-ной степени превращения в монохлорпроизводное (керил – хлорид). Керилхлоридом затем алкилируют бензол и получают продукт алкилирования (керилбензол). Дальнейшим сульфированием керилбензола получают сульфонаты (моющие средства).
Cl2 C6H6 SO3


 RH RH R – C6H5 R – C6H5 – SO3Cl,
RH RH R – C6H5 R – C6H5 – SO3Cl,
где R = C12 – C13 - парафины
Фторирование алканов. Развитие промышленности фторпроизводных (полифторпроизводных низших алканов и высокомолекулярных фторированных продуктов) объясняется ценными свойствами этих соединений.
Низшие фторпроизводные (ССl2F2 , CClF3 и др.) широко используют в холодильных машинах (фреон), а полимеры [( - CF2 – CF2 -)п] – в качестве защитных материалов против коррозии; последние способны выдерживать температуры до 400 – 450оС (тефлон).
Фторпроизводные можно получать аналогично хлорпроизводным: прямым и косвенным фторированием.
При прямом фторировании тепловой эффект реакций замещения водорода на фтор намного выше ( - 103 ккал/моль), чем в случае хлорирования ( - 23 ккал/моль). Это приводит к местным перегревам, в результате чего реакции между углеводородами и фтором имеют взрывной характер. Поэтому для прямого фторирования совершенно необходимо обеспечить температурный контроль реакции, например, разбавляя реакционную смесь инертным газом (N2) или применяя реакторы с металлической насадкой (ситами), способной быстро поглощать тепло. Фторирование в жидкой фазе позволяет легче контролировать температуру в реакторе. Осуществление процесса этого типа приводит в случае метана и этана к получению смеси моно- и полифторпроизводных.
Очень часто фторирование осуществляют в условиях гетерогенного катализа в присутствии металлического серебра или используя агенты фторирования – фториды поливалентных металлов (AgF2, CoF3 и т. д.).
RH + 2CoF3 à RF + 2CoF2 + HF
2CoF2 + F2 à 2CoF3
При помощи этих реакций можно замещать на фтор все атомы водорода в молекуле и получать перфторуглероды.
В других промышленных методах фторпроизводные получают обработкой хлорпроизводных фторидами металлов (или HF в их присутствии):
RCl + AgF à RF + AgCl
SbCl5 + Cl2
 CCl4 + 2HF CCl2F2 + 2HCl + другие фторпроизводные
CCl4 + 2HF CCl2F2 + 2HCl + другие фторпроизводные
Термическим разложением некоторых фторпроизводных получают перфторированные непредельные соединения, например, тетрафторэтилен [мономер для получения чрезвычайно стабильного полимера – тефлона ( - СF2 - )п] из дифторхлорметан.
600 – 1000OC
 2CHF2Cl F2C = CF3 + 2HCl
2CHF2Cl F2C = CF3 + 2HCl
Ненасыщенные фторпроизводные для получения полимеров можно синтезировать также присоединением HF к ацетилену:
HC = CH + HF à CH2 = CHF
фторвинил
Дегидрирование. В зависимости от степени строения циклоалканов при дегидрировании могут быть получены моно-, би- и полициклические арены. Например, образование алкилбензола из циклогексанов происходит при нагревании в присутствии катализатора – платинированого угля, содержащего 18% платины или 2% железа и 20% платина.
Реакция дегидрирования широко используется для изучения индивидуального и группового состава циклоалканов различных фракций нефти, а также лежит в основе промышленного процесса облагораживания прямгонных бензинов каталитического реформинга. При реформинге одновременно протекают процессы дегидрогенизации гексанов, дегидроциклизации нормальных алканов и изомеризации пятичленных циклоалкано в шестичленные. Риформинг проводится при 480-500оС, давлении 3,6-4,0 Мпа. Применяется бифункциональныйкатализатор АП-64,содержащий 0,60-0,65% платины (дегидрирующий катализатор) на оксидеалюминия (изомеризующий катализатор). Более эффективен полиметаллический платинорениевый катализатор типа КР-102, КР-104А, позволяющий осуществлять риформинг при меньшем давлении 1,4-2,0 МПа. В процессе риформинга сырье претерпевает следующие изменения:
|
Сырьё (бензин) |
АП-64 | КР104А | |||
| Пределы перегонки, оС | 30-173 | 102-176 | |||
| Массовое содержание углеводородов, % | |||||
| Циклоалканов | 29,0 | 30,6 | |||
| Аренов | 8,7 | 8,5 | |||
| Алканов | 62,2 | 60,8 | |||
| Алкенов | 0,1 | 0,1 | |||
| Катализатор | |||||
| Массовое содержание углеводородов, % | |||||
| Аренов | 61,6 | 65,6 | |||
| Алканов | 34,4 | 30,6 | |||
Термическая деструкция и гидрогенолиз
Пиролиз проводят при 500-550оС, как это имеет место при изучении структуры углеводородов нефтяных фракций в лабораторных условиях. При этом циклоалканы деструктируют. Газохроматографическим методом идентифицируют продукты разложения циклоалканов.
 |




 R**
R**


 R* R* + R R**
R* R* + R R**





 R
R
 |  | ||||||
 |  | ||||||

 R
R


 R + R* + R**
R + R* + R**
 |
Термическая деструкция циклоалканов происходит при промышленном пиролизе нефтяных фракций в трубчатых печах. При 840-860оС, времени превращения 0,4-0,5с получают в числе других многочисленных продуктов (этилена, пропилена, бутадиена) бензол и из него последующей переработкой – циклогексан для призводства капролактама. Сырьё с высоким содержанием алканов, например бензин – рафинад 60 – 140оС, позволяющее получать арены, алкены и затем циклоалканы, имеет следующий состав (в %) :
Нормальны алканы 39,4
Изоалканы 49,7
Циклоалканы 4,0
В том числе
Метилциклопентан 2,7
Циклогексан 1,3
Весьма высокой термической устойчивостью обладает адамантан или трицикло [3. 3. 1. 13,7] декан - трициклический циклоалкан, впервые обнаруженный в нефтях в 1933г. и имеющий следующую упрощенную структуру:





 CH2 – CH – CH2
CH2 – CH – CH2



 CH2
CH2
или
CH – CH2 – CH



CH2 – CH – CH2
Адамантан обладает устойчивой структурой с минимально напряжёнными связями. Его термическая деструкция начинается при 660оС и завершается на 94% при 675оС образованием алкенов и аренов. В присутствии алюмосиликатного или алюмохромового катализатора адамантан превращается в продукты разложения при 550 – 570оС. В среде водорода в контакте с катализаторами на кизельгуре происходит гидрогенолиз адамантана: на никелевом катализаторе при 300 – 500оС, на иридиевом или платиновом при 500 – 550оС образуются газообразные вещества, бензол, нафталин и др.
ОКИСЛЕНИЕ
Большое практическое значение имеет реакция окисление циклогексана, в результате которой образуются циклогексанон, циклогексанол, гидропероксид циклогексила, адипиновая кислота и побочные вещества (вода, кислоты, эфиры):
С6Н12 + О2 à C6H10O + H2O
С6Н12 + 1/2 О2 à C6H11OH
С6Н12 + О2 à C6H11OOH
С6Н12 + 2,5О2 à HCOO(CH2)4COOH + H2O
В газовой фазе некаталитическое окисление циклогексана кислородом воздуха происходит при 130 – 160оС, давление 1 – 10 МПа при взаимодействии с кислородосодержащими соединениями или молекулярным кислородом по схемам:

 HNO3 H2
HNO3 H2


 NXOY – NO2 = N – OH
NXOY – NO2 = N – OH
 | |||
 | |||
 – OH = N – OH
– OH = N – OH

 H2 O2
H2 O2
 |  |  |

= O
 NOCl
NOCl
 = N – OH
= N – OH
Схема получения капролактама включает гидрирование бензола в циклогексан при 320-360оС, давлении 30 Мпа, катализатор - сульфиды никеля и вольфрама. Циклогексан окисляют в циклогексаноксим и последний изомеризуют в е - капролактам - сырье для производства капрона. Исходным продуктом вместо бензола может служить циклогексан.
 По непрерывной схеме проводится обработка циклогексана 35% азотной кислотой при 120-125оС, давлении 0,4-0,5 МПа, мольном отношении кислоты к циклогексану не более 1,33 : 1. Побочный продукт нитрования - адиптновая кислота:
По непрерывной схеме проводится обработка циклогексана 35% азотной кислотой при 120-125оС, давлении 0,4-0,5 МПа, мольном отношении кислоты к циклогексану не более 1,33 : 1. Побочный продукт нитрования - адиптновая кислота:
HNO3

 OH COOH – (CH2)4 – COOH
OH COOH – (CH2)4 – COOH
Нитроциклогексан восстанавливают в циклогексаноксим водородом в среде жидкого аммиака в присутствии медного катализатора при 80-130оС, давлении
17-20 МПа с выходом оксида 85-90%.
Перспективно окисление циклогексана диоксидом азота, протекающее при относительно низкой температуре ( 70о) в течение 6ч с образованием смеси 80% адипиновой кислоты, 10% нитроциклогексана и примесей других продуктов:
 C6H12 + NO2 C6H12 + HNO2
C6H12 + NO2 C6H12 + HNO2
 C6H11NO2
C6H11NO2

 C6H11 + NO2
C6H11 + NO2
C6H11ONO
 C6H11 + NO C6H11NO
C6H11 + NO C6H11NO

 O
O

 C6H11 + O =N N = O C6H11ONO = NO2
C6H11 + O =N N = O C6H11ONO = NO2
 O
O
Возможно использования для окисления циклогексана оксида хрома (VI).
Жидкофазное окисление циклогексана кислородом воздуха происходит при 120-130оС, давлении 1,5-2 МПа в присутствии катализаторов нафтената кобальта или стеарата марганца. Суммарный выход циклогексанола и циклогексанона достигает 65-75%, одновременно образуется 0,5 т адипиновой кислоты на 1 т капролактама.
Весьма эффективен способ получения капролактама, основанной на фотохими-ческом нитрозировании циклогексана раствором хлороксида азота (III) при облучении видимым светом с длиной волны 450-550 ммк и насыщении раствора газообразным хлороводородом :




 NOCl, HCl
NOCl, HCl
NOH HCl
Хлоргидрат циклогексароксима изомеризуют с получением капролактама. Большой практический интерес представляет процесс жидкофазного окисления моноциклоалканов в присутствии борной кислоты, связывающей образующиеся спирты в борнокислые эфиры, устойчивые к дальнейшему окислению. Этерифицирующие добавки – борную кислоту или борный ангидрид добавляют в реактор для окисления (5% от массы окисляемого углеводорода). Окисление проводилось в реакторе барботажного типа азотоводородной смесью, содержащей 3,5 – 7,0 % кислорода при удельном расходе газовой смеси 500-1500 л/(кг•ч), 145-185оС в течение 3-4 ч.
Окисление гомологов циклогексана происходит при 165оС газовой смесью, содержавшей 3,5% кислорода при удельном расходе смеси 1000 л/ (кг•ч). Алкилциклопентаны более химически инертны по сравнению с алкилциклогексанами, поэтому их окисление происходит в более жестких условиях газовой смесью, содержащей 7% кислорода в течение 3-4ч. С удлинением боковой цепи степень окисления алкилциклопентанов возрастает: гексилциклопентан окисляется на 36,2 %, нонилциклопентан – на 42,0 %. Окисление пропилциклопентана в присутствии борного ангидрида происходило при 180оС окисляющей смесью с 2,4% кислорода при удельном расходе смеси 2500 л/(кг•ч), давлении 1,15 МПа в течение 0,5-2,0ч. Функция борного ангидрида в процессе окисления аналогична борной кислоте.
Характеристика спиртов, полученных окислением углеводородов, представлена ниже:
| Углеводород | T кип (при давлении в КПа), оС | 20 n D | Гидроксильное число, мг КОН/г |
| пропилциклопентан | 74-76 (1,06) | 1,4552 | 431 |
| гексилциклопентан | 121-124 (0,53) | 1,4618 | 254 |
| нонилциклопентан | 99-102 (0,53) | 1,4586 | 328 |
При окислении алкилциклопентанов образовывались в основном вторичные спирты, в небольшом количестве - первичные и до 1,6% третичные. Из пропилциклопентана получено 16% 1-циклопентил- 1-пропанола- и 1-пропил- 2-циклопентанола (цисизомер), 20,4% 1-пропил- 2-циклопентанола (транс – изомер), 15,1% 1-циклопентил- 2-пропанола, 47,2% 1-пропил- 3-циклопентанола. С удлинением боковой цепи возрастала доля циклоалкеновых спиртов с
гидроксильной группой в боковой цепи. Без использования борной кислоты в продуктах окисления возрастала доля третичных спиртов. Образующиеся спирты имели то же число атомов углерода в молекуле, что и исходный углеводород.
Окислением циклоалканов средней фракциибалаханской нефти получены нефтяные кислоты, по качеству не уступавшие товарным продуктам – мылонафту, асидолу-мылонафту, получаемым выщелачиванием кислот из нефтей и нефтепродуктов. Исходным сырьем являлась фракция концентрата циклоалканов 250-350оС с содержанием 23% циклогексанов и 77% циклопентанов с боковыми цепями С6-С15. Окисление проводилось на плотной установке при 140оС с постепенным снижением нагрева до 110оС со скоростью 5оС/ч в присутствии 2% нафтенатов марганца и калия в расчете на массу сырья, с удельным расходом воздуха 0,9 м3/(кг•ч) в течение 4,5 ч. нафтенат калия ингибировал окисление циклоалканов в гидроксикислоты. Выход нафтеновых кислот 16%, гидроксикислот – 2%.
АЛКИЛИРОВАНИЕ
Молекула циклогексана симметрична, в ней отсутствуют третичные углеродные атомы, поэтому она не взаимодействует с алкенами. Метилциклогексан в присутствии комплекса хлоридов алюминия и железа (III) (20 : 1) взаимодействует с алкенами (пропеном, метилпропеном, 1 - ноненом, 1 - додеценом и метилоктеном).
При 20оС происходит только полимеризация алкенов, при 50оС одновременно протекают реакции алкиллирования и полимеризации, при 80 – 100оС - преимущественно происходило алкилирование метилциклогексана. При алкилировании метилциклогексана высшими первичными неразвлетвленными алкенами C9H18 и C12H24 образовались метилнонил- и метилдодецилзамещенные циклогексана с преимущественно неразвлетвленными радикалами. С наибольшим выходом получались 1,3- дизамещенные циклогексана. Ниже даны показатели преломления продуктов алкиллирования циклогексана:
Метилнонилциклогексан 1,4472
Метилдодецилциклогексан 1,4518
Метилизододецилциклогексан 1,4672
Интересен процесс алкиллирования адамантана с получением моно-, ди- и полизамещенных циклоалканов. Адамантан взоимодействует с алканами нормального и изостроения в присутствии галогенидов алюминия при 40 – 160оС с замещением по третичному углеродному атому адамантанового ядра. В этих условиях при массовом соотношении между адамантаном, галогенидом алюминия и алканом 1 :1 :2,5 выход продуктов алкилирования достигал 80 – 100%. При алкиллировании адамантана 2,2,4 – триметилпентаном при 50оС в течение 15 мин. Образовывались изомерные 1- - бутиладаманты и небольшое число изомеров дибутиладамантана. Механизм реакции включал взаимодействие адамантана с фрагментами, образующимися при расщеплении молекул алкана. Одновременно наблюдал изомеризация, деструкция алкильных радикалов.
Возможно радиационно – химическое получение виниладамантан при газофазном взаимодействии адамантана с ацетиленом под действием y-излучения Co при 270 –360оС или при жидкофазном взаимодействии реагентов при комнатной температуре в растворителе.
Таким образом, содержащиеся в нефтях циклоалканы обладают сложным составом и строением, способны к многочисленным превращениям. Подробно исследованы реакции циклогексана, алкилциклогексанов и адамантана для получения их производных.
Лекция "16 Тесты и приложения" также может быть Вам полезна.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
1. Гельперин Н.И. Основные процессы и аппараты химической технологии - М.: Химия, 1981
2. Кувшинский М.Н.,Соболева А.П. Курсовое проектирование по предмету “Процессы и аппараты химической промышленности”. М.: Высшая школа, 1980
3. Основные процессы и аппараты химической технологии: Пособие по проектированию/Г.С. Борисов, В.П. Брыков, Ю.И. Дытнерский и др. Под ред. Ю.И. Дытнерского, М.:Химия, 1991
4. Павлов К.Ф., Романков П.Г., Носков А.А. Примеры и задачи по курсу процессов и аппаратов химической технологии. Учебное пособие для вузов/Под ред. чл.-корр. АН СССР П.Г. Романкова. Л.:Химия, 1987
5. Эрих В.Н. и др. Химия нефти и газа. Л.:Химия, 1972.





















