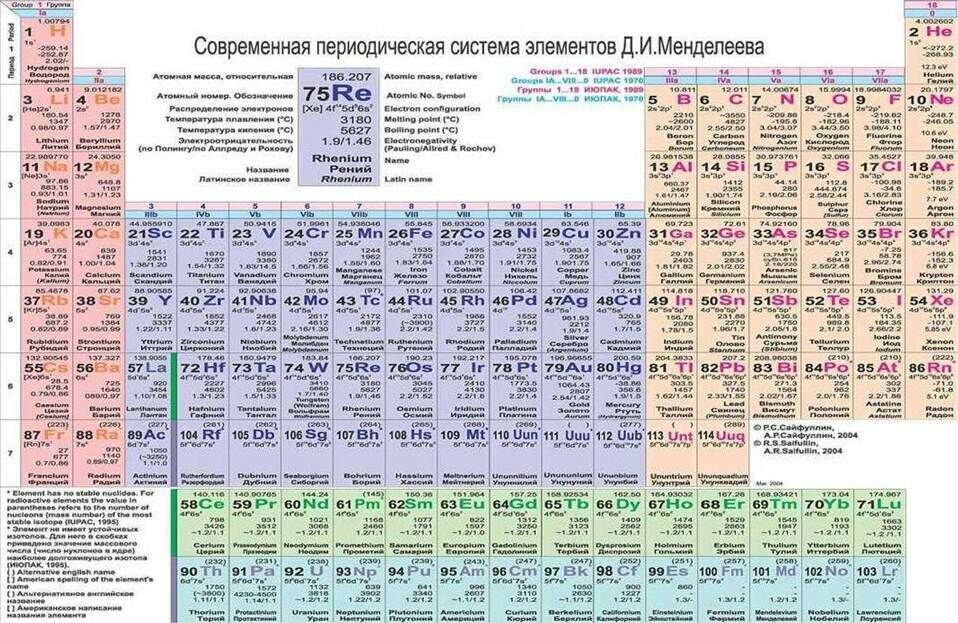
Периодическая система элементов Д.И. Менделеева
1.4. Периодическая система элементов Д.И.Менделеева.
Периодический закон открыт Д.И.Менделеевым в 1869 году.
Современная формулировка периодического закона:
Периодическое изменение свойств элементов и их соединений зависит от периодически повторяющейся подобной структуры электронной оболочки их атомов.
Эта формулировка раскрывает причину периодического изменения свойств элементов.
Наглядным выражением периодического закона является периодическая система элементов.
В периодической системе каждый элемент имеет свой порядковый номер, смысл которого теперь совершенно ясен: этот номер равен заряду ядра атома и числу электронов в оболочке атома.
Периодическая система в наиболее яркой форме отражает взаимосвязь всех химических элементов. Химические элементы, являясь качественно отличными друг от друга индивидуальными субстанциями, в то же время представляют в свой совокупности упорядоченное множество, подчиненное внутренней взаимосвязи всех элементов между собой.
Современный вариант периодической системы утвержден Международным союзом по теоретической (чистой) и прикладной химии – ИЮПАК – в 1989 году.
Рекомендуемые материалы
Система элементов слагается из периодов (горизонтальные строки) и групп (вертикальные столбцы).
Периодов в системе семь: 1 – 3 –малые, остальные – большие, седьмой – не завершен. Номер периода указывает на число уровней в атоме данного элемента.
Групп в системе - 18, они обозначаются арабскими цифрами. Группы объединяют элементы по признаку химического сходства. Многие группы имеют тривиальные названия, так, элементы первой группы называются щелочными металлами, элементы второй группы (начиная с кальция) – щелочноземельными металлами, элементы 16-ой группы – халькогенами, элементы 17-ой группы – галогенами.
Информация в лекции "Технические средства технологической среды информационной системы" поможет Вам.
В системе можно выделить четыре области, соответствующие s-, p-, d- и f-элементам.
Другие особенности рассматриваемого варианта периодической системы: дву(три) язычность с дополнительными латинскими названиями (отличающимися от английских), наличие альтернативных англо-американских [Na, K, W, Hg], и американских [Al, Cs, S] названий. В таблицу включены утвержденные ИЮПАК в 1997 г. названия элементов с № 101 по 109, исправлены атомные массы.
В предложенную систему для каждого элемента введены также две альтернативные величины электроотрицательности (ЭО) атомов и основные физические параметры соответствующих простых веществ (температуры плавления и кипения). Использование данных по электроотрицательности важно, в частности, для исправления устаревших ошибочных названий и написания формул бинарных соединений. К примеру, следующие водородные соединения элементов второго периода H4C, H3N, H2O, HF согласно значениям ЭО (для водорода – 2,1 – 2,2; для других элементов – от 2,5 для углерода до 4 для фтора) являются соответственно карбидом, нитридом, оксидом и фторидом водорода. В соответствии с этим приведенные написания формул аммиака и метана более справедливы, нежели традиционные (NH3 и CH4).