Второе начало термодинамики
Второе начало термодинамики:
Теплота не может переходить от менее нагретого тела к более нагретому телу.
Рассмотрим два резервуара в изолированной системе.
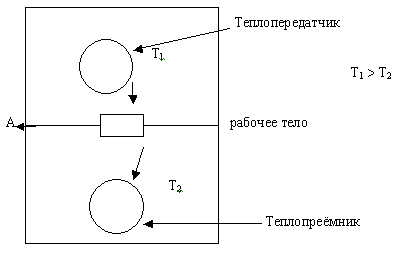
По мере перекачки энергии горячий резервуар охлаждается, а холодный нагревается. Следовательно, разность температур резервуаров уменьшается в течение всего периода времени, когда совершается работа.
Это означает, что количество энергии, которое может быть потрачено на работу (оно зависит от разности температур), должно всё время уменьшаться.
Энергия, которая уже перешла от теплопередатчика к приёмнику и превратилась в работу, называется связанной, или недоступной энергией, так как превратиться в работу она не может.
Для обозначения этой связанной, или недоступной, энергии Клаузиус ввёл следующую термодинамическую функцию, которую назвал энтропией  S (превращение).
S (превращение).
Энтропия - отношение теплоты к температуре, при которой происходит переход энергии
Рекомендуемые материалы
S = Q/T Дж/моль к.
Физический смысл энтропии настолько сложен, что долгое время не был объяснён. Объяснил его Больцман. Он назвал энтропию термодинамической вероятностью существования системы, то - есть данному макросостоянию системы отвечает множество микросостояний.
Под микросостоянием системы понимается скорость и траектория каждой микрочастицы, составляющей систему, а также взаимное положение микрочастиц, число их столкновений и т.д.
Энтропия по Больцману : S = K · lnW,
где
29 Службы занятости населения - лекция, которая пользуется популярностью у тех, кто читал эту лекцию.
W - вероятность состояния данной системы,
K - постоянная Больцмана.
Энтропия - мера неупорядоченности системы.
Определяется и рассчитывается абсолютная энтропия, приведённая к нормальным условиям.
Положительной энтропией обладают все реальные системы.
C (алмаз) - S0(c) = +2,38 Дж/моль к.




















