Закон распределения скоростей молекул
Закон распределения скоростей молекул.
Исходя из представлений статистики, в газе могут возникнуть условия, при которых отдельные молекулы могут приобретать большую скорость, чем статистическое большинство. Количество подобных «горячих» молекул расчитывается по специальным статистическим функциям. Существуют различные статистические функции: Ферми-Дирака и Бозе-Энштейна (для систем, в которых проявляются квантово-зимические эффекты); Больцмана-Максвелла – наиболее общая функция, применимая как для молекул, так и для коллоидных частиц. Существуют различные формы записи этой функции, одна из которых:
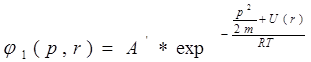
Эта функция для частиц, движущихся по классическим законам механики во внешнем потенциальном поле U(r) (напр. Силы тяжести, центробежной силы и т.д.)
j1(p,r) – функция распределения скоростей частиц по импульсам p и координатам r.;
А’ – множитель нормировки;
k,T – постоянная Больщмана (R/Na=1,38*10-23) и абсолютная температура соотв.;
Существует и другая форма записи этой функции:
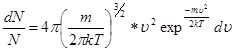
Рекомендуемые материалы
Где N – общее число частиц,
dN/N - доля молекул, движущихся со скоростями в интервале от v до v+dv
В лекции "58 Хроническая гашишная наркомания" также много полезной информации.
Эта функция имеет графическое представление.
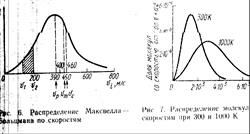
График соотвествует температуре Т и общему числу молеул N
Площадь, ограничеснная кривой, осью оасцисс и двумя линиями. Параллельными оси ординат, с абсциами v1 и v2 равна числу молекул, скорость которых заключесна между v1 и v2. Скорость vp, соответствующая саксимуму на кривой, - наиболее вероятная скорость: этой скоростью обладает большинство молеул. С понижением температуры максимум кривой становистя более узким, с повышением – более широким и сдвинутым в сторону больших скоростей.
Из этих графиков хорошо видно, что в любой системе около 10% молекул имеет скорости гораздо выше средней – это «горячие» молекулы, обладающих большей энергией и, следовательно, наиболее реакционоспособные. Обычно скорости молекул газов при 20оС лежат в пределах 200-500м/с, и лишь водород обладает скоростью 1750 м/с.
Однако для вступления в химическую реакцию молекуле неообходимо обладать совершенно определенной кинетической энергией, которая, как правило, выше среднего значения кинетической энергии остальных частиц. Эта избыточная кинетич. энергия называется энергией активации. Естественно, с ростом температуры средний уровень кин. энергии приближается к величине энергии активации, поэтому все хим. реакции с ростом температуры значительно ускоряются



















