Фазовые превращения в дисперсных системах, элементы теории жидкокристаллического состояния
9. Фазовые превращения в дисперсных системах, элементы теории жидкокристаллического состояния; термодинамика и кинетика фазовых переходов в многокомпонентных смесях
На рис. 18 приведена схема стадий фазовых превращений в дисперсных системах в виде зависимости изменения структурного параметра — напряжения сдвига нефтяной дисперсной системы oт температуры. В общем случае выделяется три основных участка существования системы: дисперсная - зоны 1 - 7 и 8 - 14 и условно-молекулярный раствор - зона 7 - 8. При этом система претерпевает следующие превращения:
I – связанно-дисперсное состояние (гель, студень) – зоны 1-2-3;
II – свободнодисперсное состояние (золь) – зоны 3-4-6-6-7;
III – условно-молекулярный раствор – зона 7-8:
IV – свободнодисперсное состояние (золь) – зоны 8-9-10-11-12;
V – связанно-дисперсное состояние (гель, твердая пена) - зоны 12-13-14.
На участках 1-7 и 8-14 в системе происходят структурные превращения, обусловливающие различие конфигураций элементов пространственной структуры, и соответственно проявление системой принципиально новых физико-механических и физико-химических свойств. Изменяется прочность структурных образований, химический состав, порядок расположения молекул, межмолекулярные силы взаимодействия и т.п. Например, можно предположить, что участок 1-3 включает зону упруго-хрупких и упруго-пластичных гелей. На участке 3-7 могут проявляться зоны кинетически неустойчивого состояния золя или кинетически устойчивого состояния. На участке 1-7 могут проявляться эффекты плавления и стеклования.
Точки переходов, условно представленные на рисунке, являются характеристическими для каждой конкретной или для группы подобных нефтяных дисперсных систем. На участках 1-7, 7-8, 8-12 преобладают физически обратимые, на участке 12-13-14 начинают проявляться в большей степени физико-химические и химические необратимые превращения. В то же время на участке 1-7 состав нефтяной дисперсной системы, как правило, не изменяется, а начиная с точки 7, система может терять некоторые компоненты, вследствие, например, испарения. Указанные процессы активируются при повышении температуры, и на участке 8–14 система приобретает совершенно новые свойства, по сравнению с исходным состоянием. Некоторые перегибы на участках 8–14 обязаны конфигурационным превращениям, структурным рекомбинациям, иммобилизационным и другим эффектам, проявляющимся при повышении температуры.
Рекомендуемые материалы
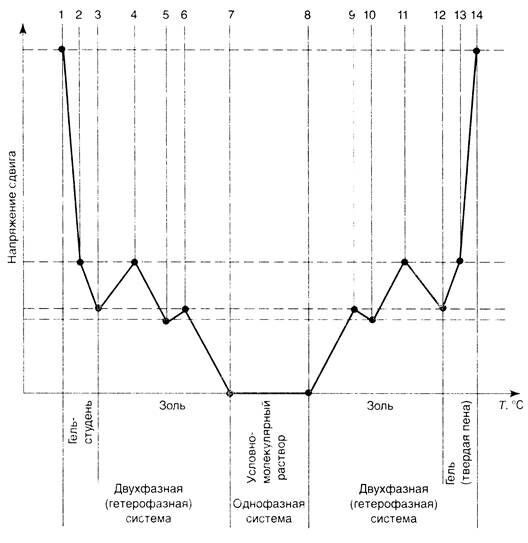
Рис. 18. Стадии коллоидно-химических превращений нефтяной дисперсной системы
при температурных фазовых переходах
Нефтяные продукты, в частности полимеры, могут образовывать жидкие кристаллы - особое состояние ряда органических веществ, в которых они обладают реологическими свойствами жидкости – текучестью, но сохраняют определенную упорядоченность в расположении молекул и анизотропию ряда физических свойств, характерную для твердых кристаллов. Жидкие кристаллы образуются при нагревании некоторых твердых кристаллов: сначала происходит фазовый переход в жидкие кристаллы и далее плавление жидких кристаллов в обычную анизотропную жидкость
Коллоидные системы [коллоиды, высокодисперсные (микрогетерогенные) системы] представляют собой дисперсные системы с частицами от 10-7 до 10-5 см. Изучение коллоидных частиц, занимающих промежуточное положение между молекулами, находящимися в постоянном движении в истинных растворах, и крупными структурными образованиями в высокоструктурированных объектах, практически неподвижными в отсутствие внешнего воздействия, показало, что между молекулярно-кинетическими свойствами истинных растворов и коллоидных систем нет качественной разницы, а различия носят только количественный характер.
При переходе системы от молекулярного состояния к надмолекулярному молекулы или надмолекулярные структуры взаимодействуют друг с другом, что сопровождается выделением или поглощением тепла. Значения тепловых эффектов позволяют оценить тип взаимодействий и степень прочности НДС. Суммарный тепловой эффект взаимодействия при химическом агрегировании во много раз больше суммарного теплового эффекта при физическом агрегировании.
Температура по-разному влияет на структурно-механическую прочность системы. При повышении температуры структурно-механическая прочность снижается и исчезает, когда система переходит в состояние молекулярного раствора. При дальнейшем повышении температуры сплошные структурные единицы появляются в системе вновь, что приводит к увеличению структурно-механической прочности системы.
В лекции "ДАНТЕ Алигьери" также много полезной информации.
Температура влияет на структурно-механическую прочность системы и на ее устойчивость против расслоения. Под устойчивостью НДС понимается способность дисперсной фазы сохранять в течение определенного времени равномерное распределение ССЕ в дисперсионной среде. Различают термодинамическую и кинетическую устойчивость НДС.
Термодинамически неустойчивая система может быть кинетически устойчива. Обычно в реальных дисперсных системах расслоение происходит очень медленно вследствие высокой вязкости и низких скоростей диффузии ВМС (система кинетически устойчива). Если время до расслоения значительно больше времени, в течение которого определяют устойчивость системы, то такую систему можно считать кинетически устойчивой (метастабильной). В противном случае система и термодинамически, и кинетически неустойчива.
Неустойчивость систем оказывает влияние на протекание в заводских условиях целевых и побочных химико-технологических процессов и вызывает в ряде случаев необходимость принятия соответствующих технических мер (например, для защиты нефтезаводами аппаратуры и оборудования от отложений кокса). Укрупнение частиц дисперсной фазы за счет их слипания под влиянием межмолекулярного взаимодействия друг с другом с потерей кинетической устойчивости и последующим разделом фаз называется коагуляцией. Этот процесс состоит из скрытой и явной стадий.
На первой (скрытой) стадии до начала расслоения ассоциаты укрупняются. Укрупненные частицы выпадают в осадок на второй (явной) стадии. Под действием сил Ван-дер-Ваальса, являющихся универсальными и проявляющихся во всех агрегатных состояниях вещества, частицы слипаются друг с другом.
Силы Ван-дер-Ваальса складываются из ориентационных, индукционных и дисперсионных сил взаимодействия..
Ориентационное взаимодействие обусловливается наличием двух полярных молекул, причем с увеличением температуры энергия этого взаимодействия снижается. Взаимодействие двух молекул, одна из которых является постоянным диполем, а в другой диполь наводится первой, называется индукционным; величина энергии индукционного взаимодействия не зависит от температуры. Дисперсионное взаимодействие наблюдается как между полярными, так и неполярными молекулами; оно вызвано взаимным возмущением электронных орбиталей, в результате чего образуются два мгновенных диполя. Соотношение всех перечисленных видов взаимодействий зависит от степени полярности компонентов НДС. В системе слабополярных молекул основными являются силы дисперсионного взаимодействия, а с увеличением полярности возрастают силы ориентационного взаимодействия.



















