Квантовомеханическая теория атома водорода. Уравнение Шредингера для атома водорода, анализ его решения
Квантовомеханическая теория атома водорода. Уравнение Шредингера для атома водорода, анализ его решения. Собственные значения энергии электрона в атоме. Потенциал ионизации
Уравнение Шредингера для атома водорода:
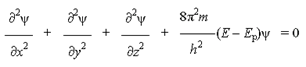
где ψ - волновая функция (аналог амплитуды для волнового движения в классической механике), которая характеризует движение электрона в пространстве как волнообразное возмущение; x, y, z - координаты, m - масса покоя электрона, h - постоянная Планка, E - полная энергия электрона, Ep - потенциальная энергия электрона.
Анализ решения уравнения Шредингера дает следующие результаты:
1. Электрон в атоме может иметь только определенные дискретные (квантованные) значения энергии, которые совпадают с выражением
E=-(Z2me4/8ε02h2n2),
где n – главное квантовое число.
2. Орбитальный момент импульса L электрона в атоме также может принимать лишь ряд дискретных значений
Вам также может быть полезна лекция "Механизмы процесса восприятия".
L=(h/2π)√l(l+1),
Где l – орбитальное квантовое число.
3. Проекция орбитального момента импульса Lz на выбранное направление OZ (например, направление внешнего магнитного поля) тоже квантуется
Lz=(h/2π)m,
где m – магнитное квантовое число.
Потенциал ионизации - разность электрических потенциалов, ускоряющая электрон до энергии, равной работе ионизации. Потенциал ионизации измеряется в вольтах и является индивидуальной характеристикой вещества. Различают:
- первый потенциал ионизации, позволяющий оторвать один электрон от нейтрального невозбужденного атома;
- второй потенциал ионизации, позволяющий оторвать два электрона;
- третий потенциал ионизации, позволяющий оторвать два электрона и т.д.



















