Электрохимические процессы
Электрохимические процессы.
При соприкосновении металла с раствором собственной соли – электролитом, на поверхности металла адсорбируются компоненты раствора. Учитывая, что над поверхностью металла присутствует электронный газ, адсорбированные ионы становятся доступными для взаимодействия с электронным газом металла. Электроны могут принимать ионы самого металла, в результате чего протекают процессы образования и разряда ионов металла. Как правило, в высококонцентрированных растворах преобладает процесс выделения ионов металла из раствора на поверхность. При этом поверхность металла заряжается положительно, что препятствует дальнейшему выделению металла из раствора. В разбавленных растворах солей преобладает обратный процесс перехода металла из объема металла в раствор – поверхность металла заряжается отрицательно.
Все описанные процессы сопровождаются переносом электрона из одной фазы в другую и характеризуются межфазным скачком потенциала.
Межфазный скачек потенциала – электрическая разность потенциала на границе раздела фазы, определяется работой переноса единичного заряда.
Переход электрона из одной фазы в другую подразделяют на два этапа: 1) переход заряда из бесконечности в вакууме в точку А, находящуюся также в вакууме на расстоянии 10-5-10-7 м от поверхности фазы (a) (работа перехода - внешний потенциал фазы ya) ; 2) перенос заряда из точки А в точку А” внутри фазы (a) (работа переноса – поверхностный потенциал ca).
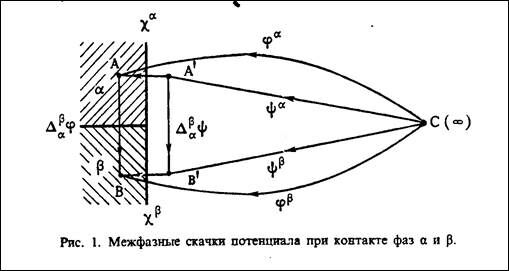
jb и ja - внутренний потенциал фаз b и a;
ca- поверхностный потенциал;
ya- внешний потенциал фазы
Рекомендуемые материалы
Возникновение поверхностного потенциала ca обусловлено причинами:
В случае переноса заряда из точки А’ (10-5-10-7) в металл (фаза a) поверхностный потенциал возникает потому, что электронный газ выходит за пределы кристаллической решетки металла и создает тем самым пространственное разделение заряда. На преодоление образовавшегося двойного электрического слоя и расходуется работа, равная по величине поверхностному потенциалу.
В случае переноса заряда из точки А’ (10-5-10-7) в электролит, заряду приходится преодолевать ДЭС, образованный молекулами электролита. На межфазной границе все молекулы полярного растворителя находятся в ориентированном состоянии, т.к. на межфазной границе всегда существует нескомпенсированность полярностей сред. Ориентация полярных молекул растворителя приводит к пространственному разделению зарядов (на расстояния, соизмеримые с размером самих молекул) и возникновению разности потенциалов.
Перенос заряда из точки А фазы a в точку В фазы b - вольта-потенциал; перенос заряда из точки А* фазы a в точку В* фазы b - гальвани-потенциал.
Состояние заряженной частицы в системе характеризуют термодинамическим параметром – электрохимическим потенциалом. Но, как и в случае с энтальпией, вместо электрохимических потенциалов обычно используют разность электрохимических потенциалов, которая определяется через химические потенциалы заряженной частицы i в фазах a и b:
m*ib - m*ia = (mib - mia)+ziF(jb-ja)
В лекции "Функции управления и структура туристско-экскурсионной организации" также много полезной информации.
где mib и mia - химические потенциалы частицы в фазах a и b,
zi – зарядовое число этой частицы;
F – число Фарадея;
jb и ja - внутренний потенциал фаз b и a соответственно, ja = ya+ca; jb = yb+cb;
По достижении состояния равновесия на поверхности металла образуется плоскопараллельный (в первом приближении) двойной электрический слой, состоящий из заряженной поверхности металла с одной стороны, и адсорбированных ионов металла – с другой. Однако образование ДЭС – результат наличия разности химических потенциалов иона металла внутри металла и раствора. Тогда общий потенциал системы будет являться суммой внутреннего потенциала металла ja и потенциала двойного электрического слоя e. Можно подобрать раствор такой концентрации, что разность хим.потециалов будет равна нулю. Тогда общий потенциал системы будет определяться только величиной ja. Раствор такой концентрации – нулевой раствор, а получаемый в этом случае потенциал – потенциал нулевого заряда.
Измеряемая разность потенциалов между двумя различными металлами, помещенными в свои нулевые растворы (т.е. разность между потенциалами их нулевых зарядов) равна разности внутренних потенциалов фаз Djba. По-другому Djba называют контактным потенциалом eк.




















