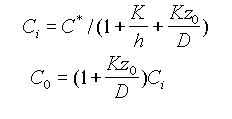Оксидирование кремния
Окисление кремния
Воздействие кислорода на кремний приводит к окислению его поверхности и образованию диоксида кремния (SiO2).
Диоксид кремния обладает уникальным набором свойств (табл. 1), благодаря которым кремний прочно занимает лидирующее положение среди полупроводниковых материалов.
Структура диоксида кремния
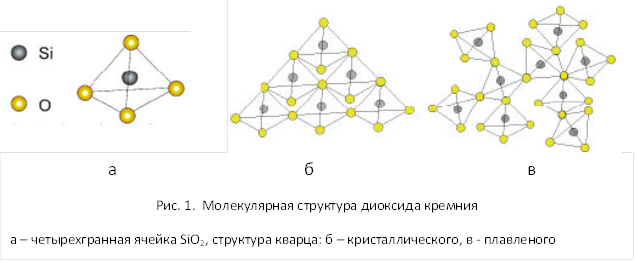
Молекулярная структура SiO2 имеет вид четырехгранной ячейки (рис.1, а), в которой атом кремний Si находится в центре тетраэдра из четырех атомов кислорода О, а атомы кислорода – по углам тетраэдра, связывая ячейки между собой. При этом каждый атом кислорода соединен с двумя атомами кремния.
Возможны две схемы соединения ячеек SiO2 с образованием соответствующих материалов.
1. Кристаллический кварц - ячейки выстроены в виде кристаллической структуры (рис.1, б).
2. Аморфный плавленый кварц (кварцевое стекло) - ячейки соединяются бессистемно (рис.1, в).
Рекомендуемые материалы
В качестве технологических слоев используется аморфный диоксид кремния SiO2, в котором не все кристаллические ячейки соединены атомами кислорода. Поэтому его структура менее упорядочена и плотность (2,3 г/см3) меньше, чем у кристаллического кварца (2,65 г/см3).
Свойства диоксида кремния SiO2
1. Из-за высокого сродства к кислороду поверхность кремния уже при комнатной температуре покрыта пленкой оксида толщиной 50…100 Ǻ. Это обеспечивает предельно плотную (на молекулярном уровне) и стабильную во времени связь слоя диоксида кремния с исходной поверхностью кремниевой пластины.
Для увеличения ее толщины оксида необходима термическая стимуляция окисления, поэтому технологические слои толщиной 200…1500 нм получаются термическим оксидированием кремния.
2. Диоксид кремния являются отличными изолятором: его удельное сопротивление лежит в диапазоне 1013 …1017 Ом∙см, а электрическая прочность составляет 107 В/см.
 |
3. Используемый в качестве технологических слоев аморфный SiO2 очень конформен – легко повторяет рельефную структуру подложки
4. Слои SiO2 противостоят большинству химических реактивов, применяемых при обработке кремния, и поэтому могут использоваться в качестве маски для его локальной обработки.
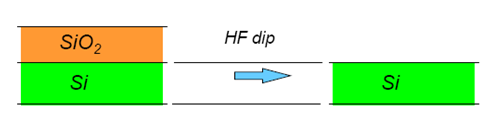
В то же время, существуют травители, например HF, которые селективно стравливают SiO2, не воздействуя при этом на кремний. Аналогичный результат можно получить, применяя плазменное травление
 |
5. Диоксид кремния блокирует диффузию основных легирующих элементов (B, P, As), а также нежелательных примесей и поэтому незаменим в качестве маски для локального легирования кремния.
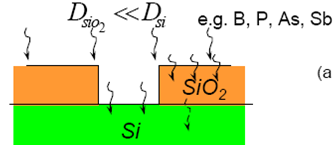
6. SiO2 стабилен при высоких температурах (до 1600 оС), применяемых в технологических процессах изготовления интегральных микросхем.
Основными функциями SiO2 в микротехнологии являются:
•
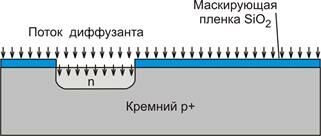 |
маскирование легирующих примесей;
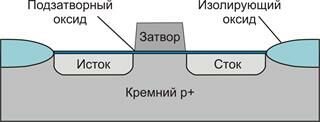
• электрическая изоляция.
 |
Получение диоксида кремния
Пленки SiO2 в микротехнологии получают путем окисления кремния различными способами:
· термическое окисление (сухое, влажное);
· анодное окисление;
· пиролитическое окисление;
· плазмохимическое окисление.
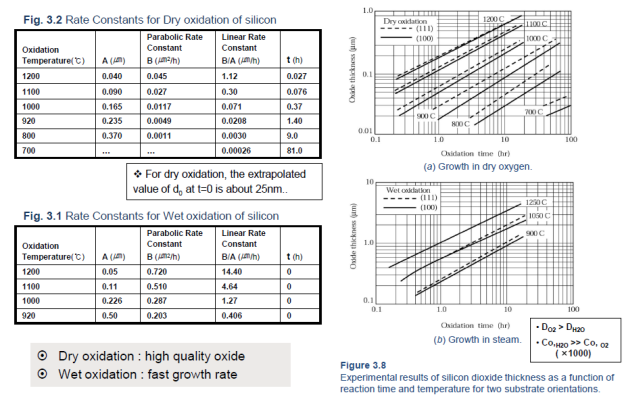
Наиболее качественный оксид для основных применений в микротехнологии получают термическим окислением.
Термическое окисление
Термическое окисление – наиболее распространенный метод получения качественных слоев SiO2 нагревом кремниевых пластин в окислительной атмосфере.
Высокая температура (1000 -- 1200 оС) процесса характерна и для других операций микротехнологии, например, разгонки примеси при диффузии. Поэтому термическое окисление легко встраивается в общий цикл обработки пластин, совмещается во времени с операциями диффузии и выполняется на том же технологическом оборудовании.
Окисление поверхности кремния может проводится при использовании:
- сухого кислорода: Si + O2 = SiO2
- влажного кислорода (паров воды): Si + 2H2O = SiO2 + 2H2
Схемы проведения процессов показаны на рис. 2.
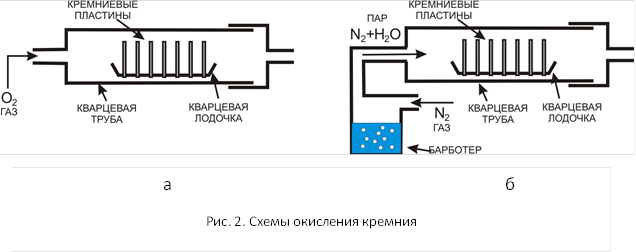
Стадии оксидирования
 |
При термическом оксидировании кислород взаимодействует с кремнием, диффундируя через слой SiO2, поскольку коэффициент диффузии O2 в SiO2 во много раз больше, чем аналогичный коэффициент диффузии Si в SiO2.
Объемная плотность образующегося SiO2 (2,3х1022 мол/см3) примерно в 2 раза меньше, чем у кремния (5х1022 мол/см3).
Поэтому из молекул кремния, содержащихся в слое толщиной 1 мкм, образуется слой диоксида толщиной 2,17 мкм.
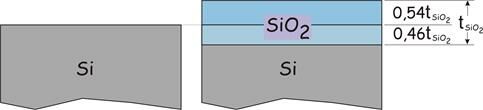 |
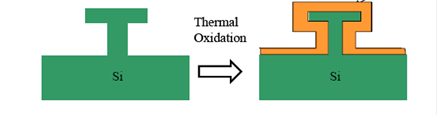
Часть слоя SiO2 врастает в исходную поверхность кремниевой пластины, а часть – нарастает над ней.
Заметим, что объемная плотность образующегося диоксида (2,3х1022 молекул/см3) более чем в 2 раза меньше, чем у кремния (5х1022 молекул/см3).
Поэтому из молекул кремния, содержащихся в слое толщиной 1 мкм, образуется слой диоксида толщиной 2,17 мкм. Частично этот слой внедряется в исходный кремний, а частично нарастает над ним (рис. ), следуя определенному соотношению.
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________
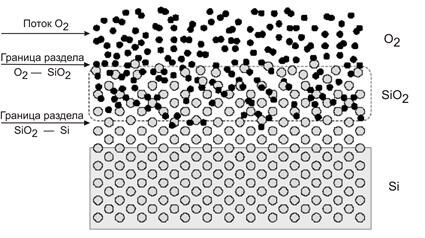
Таким образом, в процессе термического оксидирования можно выделить следующие стадии, характеризуемые соответствующими скоростями:
· Молекулы кислорода или паров воды подаются в виде газового потока к поверхности кремниевых пластин.
· Далее молекулы диффундируют через уже имеющуюся на поверхности кремния оксидную пленку
· Реакция окисления происходит на границе раздела Si-SiO2. Слой SiO2 растет как за счет врастания в кремний, так и нарастания над его исходной поверхностью.
Введем следующие важные понятия:
· Концентрация — число молекул в единице объёма, см-3
· Поток — число частиц, проходящих через единицу площади в единицу времени, см-2с-1
Модель роста оксида Дила-Гроува (Deal-Grove)
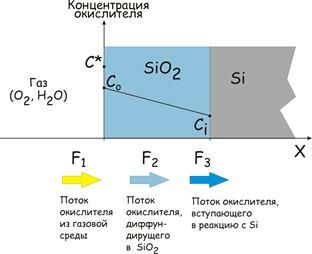
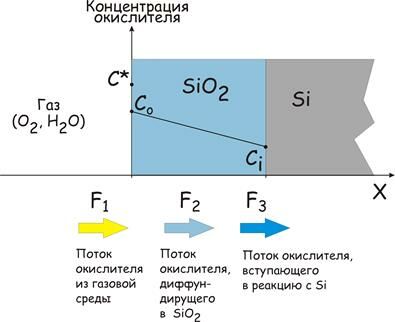
Выводы предыдущего раздела позволяют рассмотреть в процессе термического окисления три потока молекул кислорода (рис. ).
1. Поток молекул из газовой среды к внешней поверхности пластины, на которой в начальной стадии происходит реакция (кислорода с кремнием), а затем – адсорбция кислорода на формирующемся оксиде - поток F1
2. Поток молекул, диффундирующих через оксид SiO2 к кремнию Si - поток F2
3. Поток молекул O2, вступающих в реакцию с Si на границе раздела SiO2 /Si - поток F3
 |
В равновесных условиях три рассмотренных потока равны между собой, при этом скорость реакции определяется самым медленным из них.
1. Поток F1 определяется разностью между _____(какой)____________ концентрацией C* окислителя, (где)________________ ________________ ________________ , и его концентрацией Сo _______________ _(где, на какой поверхности)________________ поверхности:
 , (1)
, (1)
где h - ________________ ________________ ________________ [см/с].
Явление, заключающееся в ________________ ________________ ________________ ________________ ________________ ________________ , получило название_______________. Другими словами __________________ можно определить как ________________ ________________ ________________ .
________________ ________________ ________________ ________________ ________________ ________________ ________________ ________________ ________________ ________________ ________________ ________________ ________________ ________________ ________________ ________________ ________________ ________________
Зависимость ________________ ________________ ________________
________________ ________________ ________________ ________________
________________ ________________ в________________ ________________
________________ ________________ описывается законом Генри:
 (3)
(3)
где Н – постоянная Генри, мера ________________ ________________
2. Поток F2 описывается законом Фика для диффузии в твердом теле:
 (6)
(6)
где D – коэффициент диффузии кислорода в окисный слой [см/с2],
Ci – концентрации окислителя в оксиде у границы раздела SiO2/Si,
Xo – толщина оксида.
Заметим, что C0 ¹ C*, поскольку не все молекулы кислорода, адсорбированные поверхностью оксида, проникнут внутрь оксида через его поверхность.
3. Поток F3 определяется химической реакцией на границе раздела SiO2/Si и пропорционален концентрации реагента:
 , (7)
, (7)
где kS – коэффициент скорости реакции
Выразим значения концентраций C*, С0 и Сi через известные параметры технологической среды.
Для равновесного состояния F1 = F2 = F3 .
Приравнивая F1 = F2 и F2 = F3 имеем:
 (8)
(8)
 (9)
(9)
Сначала преобразуем уравнение (9):
 (10)
(10)
Подставим полученные соотношения в уравнение (8). Учтем при этом выражение (3). Получим:
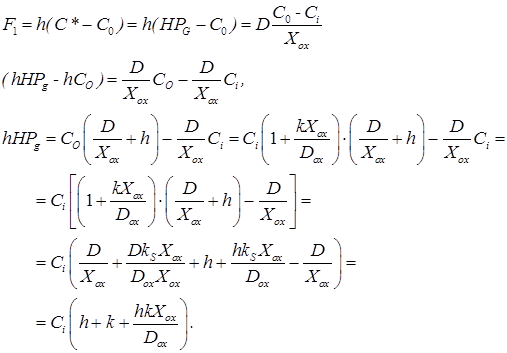
(11)
В итоге получаем:
 (12)
(12)
И, соответственно,
 (13)
(13)
Таким образом, поток окислителя к поверхности кремния можно записать в виде:
 (14)
(14)
Перейдем теперь к анализу скорости роста оксида, которую можно представить как
 (15)
(15)
Используя уравнение (14) получим
 (16)
(16)
Значения N1 равны: для сухого кислорода N1 = 2,3×1022 молекул/см3 и для паров воды N1 = 4,6×1022 молекул/см3.
Решение дифференциального уравнения (16) предусматривает следующие начальные условия.
Будем считать, что в начальный момент времени (t = 0) на поверхности кремния имеется исходный слой оксида толщиной Xo(0) = Xi.
Преобразуем уравнение (16) к виду:
 (17)
(17)
где 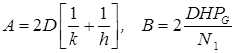
Для получения аналитической связи толщины оксида от времени оксидирования необходимо решить дифференциальное уравнение (17).
Перепишем его в виде:
 (18)
(18)
Интегрируя (18) в интервале от t=0 до t и учитывая, что при t=0 имеется начальная толщина оксида Xi получим:
 ,
,
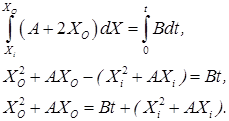
Итак, имеем:
 (19)
(19)
где  .
.
Время оксидирования на заданную толщину с учетом начального слоя можно представить как
 (20)
(20)
Решение квадратичного уравнения (19) дает следующую зависимость толщины оксида от времени:
 (21)
(21)
Проанализируем полученное выражение. При малых временах t, то есть
при выполнении условия
 или
или 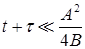
выражение (21) примет вид
 (22)
(22)
При больших временах, то есть при выполнении условия
 или
или 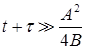
выражение (21) примет вид
 (23)
(23)
Таким образом, на начальной стадии окисления толщина оксидной пленки увеличивается со временем по линейному закону, а при больших временах окисления зависимость толщины от времени становится корневой.
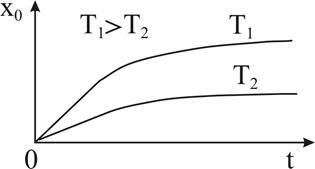 |
На рисунке представлены зависимости толщины слоя SiO2 от времени окисления при двух разных температурах. Видно, что температура значительно увеличивает скорость роста оксидного слоя.
Повышение скорости роста SiO2 с температурой объясняется увеличением коэффициента диффузии молекул окислителя в слое оксида и увеличением константы скорости химической реакции окисления на границе раздела SiO2 – Si.
Представленные на рисунке зависимости качественно описывают реальный процесс термического окисления кремния.
Что касается конкретных значений скорости роста слоя SiO2, то, например, при сухом окислении и температуре порядка 1300 °С для получения слоя толщиной 1 мкм требуется примерно 15 часов.
Если термическое окисление проводить в атмосфере водяного пара, то аналогичный слой при той же температуре можно получить примерно за 1час. Более высокая скорость объясняется меньшим эффективным диаметром молекул Н2О по сравнению с О2 и меньшей энергией активации диффузии молекул окислителя через растущий слой оксида.
Качество слоев, полученных тем и другим способом, будет разным. При влажном окислении полученные слои SiO2 обладают худшими электрическими и защитными свойствами, чем слои, полученные сухим окислением.
Поэтому обычно эти два способа комбинируют, тем самым удается получать слои SiO2 приемлемого качества с достаточно высокой скоростью.
Модель роста оксида Дила-Гроува (Deal-Grove)
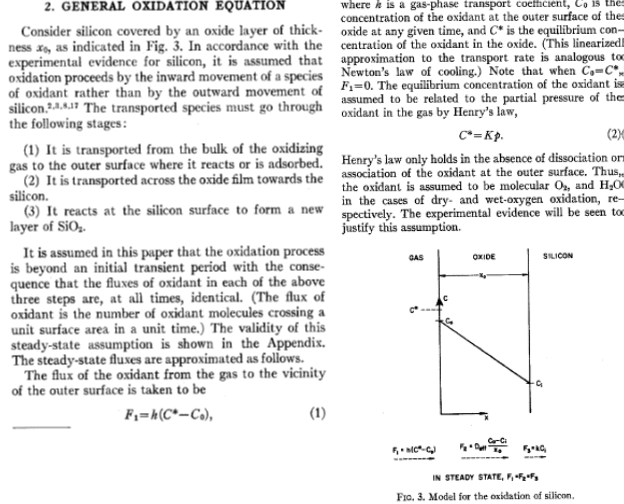
Выводы предыдущего раздела позволяют рассмотреть в процессе термического окисления три потока молекул кислорода (рис. ).
1. Поток молекул из газовой среды к внешней поверхности пластины, на которой в начальной стадии происходит реакция (кислорода с кремнием), а затем – адсорбция кислорода на формирующемся оксиде - поток F1
2. Поток молекул, диффундирующих через оксид SiO2 к кремнию Si - поток F2
3. Поток молекул O2, вступающих в реакцию с Si на границе раздела SiO2 /Si - поток F3
В равновесных условиях три рассмотренных потока равны между собой, при этом скорость формирования оксида определяется самым медленным из них.
|
Поток F1 определяется разностью между максимальной и реальной поверхностной концентраций окислителя: F1 = h(C* - C0), где C0 - поверхностная концентрация окислителя, h - коэффициент переноса. Значение концентрации окислителя C0 зависит от температуры, скорости газового потока и растворимости окислителя в SiO2. Для того чтобы определить скорость роста окисла, рассмотрим потоки окислителя в объеме окисла F2 и на его границе с кремнием F3. Согласно закону Фика, поток через объем окисла определяется градиентом концентрации окислителя: F2 = - D(dC/dz) = D(C0 - Ci)/z0, (1) где Ci - концентрация окислителя в молекулах на кубический сантиметр при z = z0, D - коэффициент диффузии при данной температуре, z0 - толщина окисла. Величина потока F3 на границе окисла с полупроводником зависит от постоянной K скорости поверхностной реакции и определяется как: F3= kCi (2) При стационарных условиях эти потоки равны, так что F3 = F2 = F1 = F. Следовательно, приравняв соотношения (1) и (2), можно выразить величины Ci и C0 через C*:
|

Процесс окисления происходит на границе Si - SiO2, поэтому молекулы окислителя диффундируют через все предварительно сформированные слои окисла и лишь затем вступают в реакцию с кремнием на его границе. Согласно закону Генри, равновесная концентрация твердой фазы прямо пропорциональна парциальному давлению газа P:
C* = HP, где
C* - максимальная концентрация окислителя в газе для данного значения давления P,
H - постоянный коэффициент Генри.
В неравновесном случае концентрация окислителя на поверхности твердого тела меньше, чем C*.
Приведем зависимость x02+Axo=Bt к линейному выражению с новыми переменными:
x0+A=B(t/x0) – разделили на x0
x0=B(t/x0)-А
Получили зависимость x0(t/x0).
Пусть y= x0; x= t/x0,
| t | 0,11 | 0,30 | 0,40 | 0,50 | 0,60 | у |
| x0 | 0,041 | 0,100 | 0,128 | 0,153 | 0,177 | |
| t/x0 | 2,680 | 3,000 | 3,125 | 3,270 | 3,390 | x |
Отметим точки х,у; соединим их (красный цвет на рисунке)
Т.к есть погрешность измерений при проведении эксперимента- апроксимируем этот график прямой (зеленый цвет на рисунке): соответствует формуле y=B*x-А
Пересечение прямой с осью у даст –А; тангенс угла наклона В=tg(w)
"4 Виды разверток" - тут тоже много полезного для Вас.
 Получим B≈0,19; А≈0,47
Получим B≈0,19; А≈0,47
Проверим, подставив в начальную формулу , для точки t=0,30; x0=0,100
x02+Axo=Bt
0,12+0,47* 0,1=0,19*0,3
0,057=0,057, выполняется
Ответ: B=0,19; А=0,47