Построение изотермы адсорбции
Построение изотермы адсорбции. Работа адорбции
Для процессов адсорбции Гиббс вывел уравнение адсорбции:
Г= -С/RT(ds/dC)
Уравнение связывает поверхностное натяжение s, количество адсорбированного вещества Г и концентрацию. Величину G= –(ds/dC) принято называть поверхностной активностью вещества. Тогда
Г = (С/RT)G
Это уравнение позволяет по экспериментальной кривой изотермы поверхностного натяжения построить изотерму адсорбции, для чего в нескольких точках изотермы поверхностного натяжения проводят касательные и определяют tg угла наклона по отношению к оси абсцисс (С). Величина тангенса угла наклона соответствует величине –(ds/dC) в данной точке, т.е. поверхностной активности. А отрезок Z (в единицах поверхностного натяжения, эрг/см2; дин/см2; Дж/см2) на оси ординат будет соответствовать произведению –С(ds/dC)=Z. Тогда
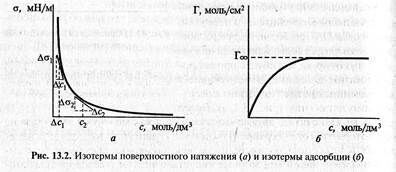
Г=Z/RT
Таким образом, каждой точке на кривой поверхностного натяжения соответствует точка кривой изотеры адсорбции.
Рекомендуемые материалы
Величину Гмах в уравнении Ленгмюра ( ) можно найти графически, преобразовав уравнение Ленгмюра в уравнение прямой. Для этого берут обратные величины элементов уравнения. Тогда
) можно найти графически, преобразовав уравнение Ленгмюра в уравнение прямой. Для этого берут обратные величины элементов уравнения. Тогда
1/Г=1/Гмах+1/С*[1/(Гмахk)]
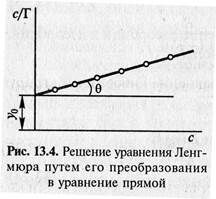
Откладывая 1/С на оси абсцисс, а 1/Г – на оси ординат – получаем прямую, которая отсекает на оси ординат величину 1/Гмах. Величина константы k определяется как tg угла наклона прямой по отношению к оси абсцисс:
tga=1/(kГмах)
Ощущения, виды и свойства ощущений - лекция, которая пользуется популярностью у тех, кто читал эту лекцию.
откуда k=Гмах/tga
Если откладывать на графике С/Г – С то сtg q=Г¥, а отрезок, отсекаемый на оси ординат y0=1/k Г¥ (рис. 13.4).
Полученные значения Г¥ позволяют вычислить молекулярные константы молекул ПАВ – площадь поперечного сечения молекул А0 и ее длину, равную толщине предельного монослоя d:
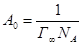
Длина молекулы вычисляется из соображения, что масса 1см2 поверхностного слоя равна m=dr (где r - плотность вещества ПАВ в жидком состоянии). Поскольку в то же время m=M Г¥, то
d= M Г¥/r.





















